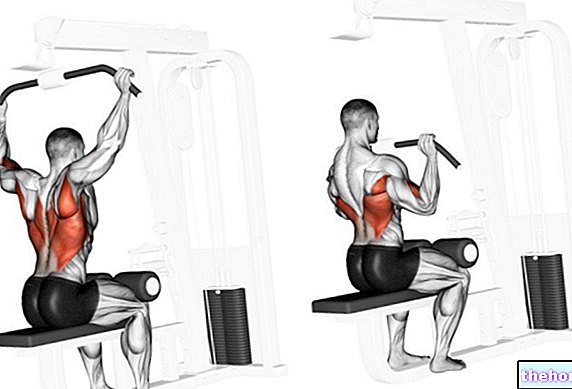
Som bekant transporterar röda blodkroppar (RBC) syre till vävnaderna och i uthållighetssporter, såsom cykling, längdskidåkning, etc. är syrekraven mycket höga.
Under en tid har därför strategier undersökts för att öka produktionen av RBC för att förbättra sportprestanda.
Den senaste strategin är baserad på erytropoietins (EPO) roll för att stimulera benmärgen att producera röda blodkroppar (RBC).
Rekombinant humant EPO (rHuEPO) och relaterade ämnen (t.ex. darbepoietin) används som dopning.
EPO har en relativt kort livslängd i kroppen medan dess stimulerande effekt kan vara upp till två veckor
d "syre1985 Lin och Jacobs klonade erytropoietingenen och utvecklade en transfekterad cellinje (CHO -celler) som kan producera rekombinant humant erytropoietin
Erytropoies och hypoxi
Erytropoies (produktion av nya röda blodkroppar) styrs av ett mycket känsligt återkopplingssystem, där en sensor på njurnivå känner av förändringar i syretillförseln.
Mekanismen är baserad på närvaron av en heterodimer transkriptionsfaktor (Hypoxia-inducerbar faktor, HIF-1) (HIF-1α och HIF-1β) som ökar uttrycket av erytropoietingenen.
HIF-1α är instabil i närvaro av syre och bryts snabbt ned av prolyl-hydroxylas med bidraget från von Hippel-Lindau-proteinet.
Under hypoxi är propyl-hydroxylas inaktivt och därför ackumuleras HIF-1α som aktiverar uttrycket av erytropoietin som stimulerar den snabba expansionen av erytroida progenitorer.
(men de första 27 delas upp under utsöndringen).
Det produceras huvudsakligen av peritubulära interstitiella celler i njurarna, under kontroll av en gen på kromosom 7.
Efter utsöndring binder erytropoietin i den hematopoetiska vävnaden (benmärg) till en receptor (EPO-R) som är belägen på ytan av erytroidfädern och internaliseras.
I närvaro av anemi eller hypoxemi ökar syntesen av EPO snabbt med mer än 100 gånger och ökar följaktligen överlevnad, spridning och mognad av benmärgsfaderceller också genom inhibering av apoptos (programmerad celldöd).
Normala nivåer av EPO i blodet är cirka 2-25 mU / ml, men kan öka 100-1000 gånger som svar på hypoxi.
Syresensormekanismen leder till avbrott i EPO -produktionen när antalet röda blodkroppar och / eller tillförsel av syre till vävnaderna återgår till jämvikt
Återkopplingsmekanismen säkerställer tillräcklig produktion av RBC för att förhindra anemi och vävnadshypoxi, men inte för hög för att leda till polycytemi med överdriven blodviskositet och därmed kardiovaskulära risker.
Överproduktionen av EPO som leder till polycytemi (sekundär för att skilja sig från polycytemia vera eller primär: myeloproliferativ störning där EPO-oberoende kloner av stamceller förökas med en ökning av både RBC och granulocyter och trombocyter) kan bero på hjärt- eller andningssjukdomar, från höjd , från hinder för blodflöde till EPO-produktionsplatsen, från EPO-producerande tumörer.
Vid sekundär polycytemi är EPO -nivåerna generellt höga, men de kan också vara normala på grund av en ökad omsättning.
Det är känt att de genetiska skillnader som finns mellan idrottare kan vara ett element på grundval av de olika prestationskapaciteterna.
Bland de möjliga genetiska skillnaderna kan vissa beröra erytropoes i allmänhet och specifikt erytropoietin.
Ett exempel är historien om den finska längdåkaren Eero Mäntyranta, dubbelguldmedaljör vid OS 1964 i Innsbruck.
Han föddes med en Epo-genmutation (uttryckt på receptornivå) som ökade hans syreförmåga med röda blodkroppar med 25-50%.
Detta parafysiologiska tillstånd kan reproduceras genom genmanipulation.
Antalet EPO-receptorer varierar i de olika cellerna i erytrocytlinjen.Maximum uppstår i CFU-E, antalet minskar när differentiering och mognad av erytrocytcellerna fortskrider EPO.
EPO -receptorer har också identifierats på myocyter, endotelceller, CNS, äggstockar och testiklar.
EPO anses därför spela en fysiologisk roll i hjärt- och hjärnutveckling.
EPO skyddar hjärt- och nervvävnader från inflammation och ischemisk skada: både genom direkt stimulering av nerv- och hjärtceller och indirekt genom att mobilisera endotelceller, vilket främjar nyvaskularisering.
) med avseende på den fysiologiska EPO, som dock återspeglas i molekylens kemiska och fysiska beteende, till exempel finns det skillnader i den elektriska laddningen.För ergogena ändamål används rHuEPO med injicerbara administrationer var 2-3: e dag, i 3-4 veckor, i samband med järnpreparat. Faktum är att vid förhållanden med erytropoietinstimulering blir det nödvändigt att få syntetiserat hemoglobin hos idrottare med en mycket högre hastighet än vanligt och detta kräver en tillräcklig tillförsel av järn för att upprätthålla erytropoetisk effektivitet. Halveringstid i.v. 8,5 timmar.
När underhållsfasen har uppnåtts kan intaget ske vid lägre doser, vilket är svårare att identifiera vid dopningskontroller.
Darbepoietin
Mer stabil än EPO, med längre halveringstid (i.v. 25,3 timmar) och större effekt; det är lättare att identifiera på grund av dess strukturella egenskaper som skiljer sig från den endogena mänskliga produkten och på grund av dess lägre clearance
Terapeutisk användning av erytropoietin (epoetin; Eprex®, Globuren®, Neorecormon®; darbepoetin: Aranesp®, Nespo®)
- Anemi vid kronisk njursvikt
- Zidovudinanemi (anti-HIV)
- "Eldfast" anemi
- Anemi efter kemoterapi mot cancer
- Patologiska brister i EPO
- Myelom
- Myelodysplastiska syndrom.
Snabbt och kontinuerligt utveckla forskning om erytropoietin:
Produkter som efterliknar EPO: s aktivitet
Små peptider eller icke-peptidföreningar som kan binda, aktivera dem, till EPO-receptorerna (Science 1996; 273: 458. Proc Natl Acad Sci USA 1999; 96: 12156)
Nyligen, till exempel i in vitro-experiment, har silkesmaskhemolymf visat sig hämma apoptos av EPO-producerande celler genom att öka EPO-produktionen med 5 gånger (Biotechnol Bioeng 2005; 91: 793)
(hematokrit uttryckt i procent), hemoglobinnivåer, antal retikulocyterVid cykling leder hematokritmätningar över 50% till suspension. Värden över 50% misstänks av IOC
Internationella skidförbundet har infört en hemoglobingräns på 18,5 g / dL hos män och 16,5 g / dL hos kvinnor, om den hittas före en tävling kan idrottaren inte delta för att bevara sin hälsa.
Det bör understrykas att hematokrit- och hemoglobinvärden kan variera från idrottare till idrottare och som svar på samma övning. Idealet är att ha den hematologiska profilen för varje idrottare över tiden:
undersökningarna för att identifiera användningen av EPO har sträckt sig till olika sporter och uppenbarligen till OS
Marco Pantani diskvalificerades från Tour of Italy för ett hematokritvärde på 52%
År 2003 testade den kenyanska medeldistanslöparen Bernard Lagat (näst bästa tid någonsin på 1500 m) positivt (forskning av rHuEPO i urinen) för EPO-intag före VM i friidrott i Paris (där han inte kunde delta) efterföljande mot- analyser rensade honom dock. Detta fall visade behovet av att söka mer tillförlitliga tester.
En ny direkt isoelektrisk metod har nyligen utvecklats (med bra resultat) för att skilja exogent från endogent EPO i urinprov, utvecklat i det franska laboratoriet i Chatenay-Malabry (Nature 2000; 405: 635; Anal Biochem 2002; 311: 119; Clin Chem 2003; 49: 901). Det var möjligt att identifiera exogent EPO även efter 3 dagar från intaget
(Incidens 1-30%). Mekanismen är inte helt förstådd, "EPO har en" vasokonstriktiv verkan och kronisk exponering orsakar resistens mot kväveoxidets vasodilaterande verkan. Slutligen främjar EPO tillväxten av glatta muskelceller i kärlen med vaskulär ombyggnad och hypertrofi som kan bidra till underhåll av hypertoni [Am J Kidney Dis 1999; 33: 821-8]).
Benvärk (icke-svår, övergående, hög förekomst = 40%).
Kramper (på grund av snabb ökning av blodviskositeten och hypoxisk vasodilatationsförlust med följd ökad vaskulär resistens).
Huvudvärk.
Tromboemboliska fenomen (PE, MI, stroke), alla relaterade till blodhyperviskositet.
Anemi efter behandling på grund av minskad endogen EPO-produktion.
Ren röda blodkroppar (anti-EPO-antikroppsbildning?).
Myeloproliferativa störningar (djurstudier, långtidsbehandlingar?).
Skador från erytropoietin som dopning
Uppgifterna om biverkningarna av erytropoietin som anges ovan härrör nästan uteslutande från terapeutiska behandlingar hos patienter med underliggande sjukdomar
Det finns inga studier om skadan av erytropoietin som används som dopning på friska idrottare
En studie av idrottare som fick EPO i 6 veckor fann en signifikant ökning av systoliskt blodtryck som svar på sub-maximal träning.
Antalet dödsfall bland belgiska och nederländska cyklister mellan 1987 och 1990 har varit relaterat till användningen av EPO (Gambrell och Lombardo. Läkemedel och dopning: bloddopning och rekombinant humant erytropoietin. I: Mellion, M.B. (red.): Idrottsmedicinhemligheter. Philadelphia: Hanley & Belfus, 1994, s. 130-3)
Det är inte fel att tro att de biverkningar som ses hos patienter också kan förekomma hos friska idrottare om än med en lägre förekomst.