Aktiva ingredienser: propiverin (propiverinhydroklorid)
Mictonorm 45 mg kapslar med modifierad frisättning
Varför används Mictonorm? Vad är det för?
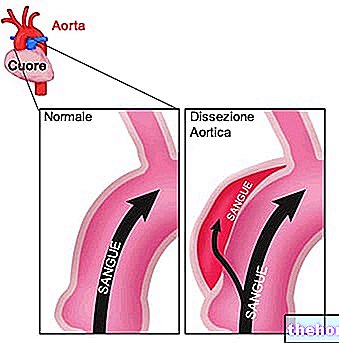
Mictonorm används för att behandla personer som har svårt att kontrollera blåsan på grund av överdriven blåsaktivitet eller som har problem med ryggmärgen. Mictonorm innehåller den aktiva substansen propiverinhydroklorid. Detta ämne hindrar blåsan från att dra ihop sig och ökar. Volymen den kan hålla. Mictonorm används för att behandla symptom på överaktiv urinblåsa. Det är en kapsel med modifierad frisättning som tas en gång om dagen.
Kontraindikationer När Mictonorm inte ska användas
Ta inte Mictonorm
Ta inte Mictonorm om du är allergisk (överkänslig) mot propiverinhydroklorid eller något annat innehållsämne i Mictonorm.
Ta inte Mictonorm om du har något av följande tillstånd:
- tarmobstruktion
- obstruktion av urblåsningsvägarna (urinering)
- myasthenia gravis (en sjukdom som orsakar muskelsvaghet)
- misslyckande i musklerna som styr tarmrörelser (tarmatoni)
- svår tarminflammation (ulcerös kolit) som kan orsaka diarré som innehåller blod och slem och smärta i buken
- giftig megakolon (en sjukdom med förstorad tarm)
- ökat tryck inuti ögat (okontrollerat glaukom med vinkelstängning)
- måttlig eller svår leversjukdom
- snabb och oregelbunden hjärtslag
Försiktighetsåtgärder vid användning Vad du behöver veta innan du tar Mictonorm
Innan behandling med Mictonorm, tala om för din läkare om du lider av:
- skador på nerverna som kontrollerar blodtryck, hjärtfrekvens, tarm- och blåsrörelser och andra kroppsfunktioner (autonom neuropati)
- njursjukdom
- leversjukdom
- allvarligt hjärtsvikt
- förstoring av prostata
- halsbränna och matsmältningsbesvär på grund av återflöde av magsaft i halsen (hiatal bråck med refluxesofagit)
- oregelbunden hjärtrytm
- snabba hjärtslag
Om du har något av dessa tillstånd, kontakta din läkare som berättar vad du ska göra.
Interaktioner Vilka läkemedel eller livsmedel kan förändra effekten av Mictonorm
Tala om för din läkare om du tar eller nyligen har tagit något av följande läkemedel som kan interagera med Mictonorm:
- antidepressiva medel (t.ex. imipramin, klomipramin och amitriptylin),
- sömntabletter (t.ex. bensodiazepiner),
- antikolinergika som tas via munnen eller ges genom injektion (används rutinmässigt för att behandla astma, magkramper, ögonproblem eller urininkontinens),
- amantadin (används för att behandla influensa och Parkinsons sjukdom)
- neuroleptika som promazin, olanzapin, quetiapin (läkemedel som används för att behandla psykotiska störningar som schizofreni eller ångest)
- beta-stimulantia (används vid behandling av astma)
- kolinergika (t.ex. karbachol, pilokarpin)
- isoniazid (tuberkulosmedicin)
- metoklopramid (används för att behandla illamående och kräkningar)
Det är dock möjligt att du fortfarande kan ta Mictonorm. Din läkare kommer att avgöra vad som är bäst för dig.
Tala om för din läkare eller apotekspersonal om du tar eller nyligen har tagit andra läkemedel, även receptfria sådana.
Varningar Det är viktigt att veta att:
Graviditet, amning och fertilitet
Ta inte Mictonorm om du är gravid, tror att du kan vara gravid eller planerar att bli gravid eller om du ammar.
Köra och använda maskiner
Ibland kan Mictonorm orsaka dåsighet och dimsyn. Kör inte fordon eller använd maskiner om du är dåsig och har suddig syn.
Viktig information om några av ingredienserna i Mictonorm
Mictonorm innehåller laktos (ett socker). Om din läkare har fått veta att du inte tål vissa sockerarter, kontakta din läkare innan du tar detta läkemedel.
Dos, metod och administreringstid Hur man använder Mictonorm: Dosering
Ta alltid Mictonorm enligt läkarens anvisningar. Kontakta din läkare eller apotekspersonal om du är osäker.
Ta kapseln vid samma tidpunkt varje dag. Svälj kapseln hel med ett glas vatten. Krossa inte eller tugga inte kapslarna. Du kan ta dem med eller utan mat.
Vuxna och äldre: Den vanliga dosen Mictonorm är en kapsel om dagen.
Mictonorm rekommenderas inte för barn.
Om du har glömt att ta Mictonorm
Oroa dig inte. Ta bort den dosen helt. Ta sedan din nästa dos vid rätt tidpunkt. Ta inte en dubbel dos för att kompensera för en glömd dos.
Överdosering Vad du ska göra om du har tagit för mycket Mictonorm
Om du av misstag har tagit mer än den föreskrivna dosen, kontakta närmaste akutmottagning eller kontakta genast din läkare eller apotekspersonal. Kom ihåg att ta med dig förpackningen och eventuella kvarvarande kapslar.
Biverkningar Vilka är biverkningarna av Mictonorm
Liksom alla läkemedel kan Mictonorm orsaka biverkningar men alla användare behöver inte få dem.
Alla läkemedel kan orsaka allergiska reaktioner, men allvarliga allergiska reaktioner är mycket sällsynta. Följande symtom är de första tecknen på sådana reaktioner:
- plötslig väsande andningssvårigheter eller yrsel, svullnad i ögonlocken, ansikte, läppar eller hals
- skalning och blåsbildning av hud, mun, ögon och könsorgan
- Hela kroppen utslag Ta inte kapslarna längre och kontakta din läkare omedelbart om du märker något av dessa symtom under behandlingen.
En akut attack av glaukom är möjlig. I detta fall kommer patienten att se färgade ringar runt lamporna eller känna intensiv smärta i och runt det ena eller andra ögat. Om detta händer, kontakta läkare omedelbart..
Följande biverkningar har också observerats:
Mycket vanliga (kan förekomma hos fler än 1 av 10 personer)
- torr mun
Vanliga (kan förekomma hos upp till 1 av 10 patienter)
- synfel och svårigheter att fokusera
- Trötthet
- huvudvärk
- smärta i buken
- matsmältningsproblem
- förstoppning
Mindre vanliga (kan förekomma hos upp till 1 av 100 personer)
- illamående och kräkningar
- yrsel
- tremor - oförmåga att tömma urinblåsan (urinretention) - rodnad - smakförändringar - lågt blodtryck med sömnighet
Sällsynta (kan förekomma hos upp till 1 av 1000 användare)
- utslag
Mycket sällsynta (kan förekomma hos upp till 1 av 10 000 personer)
- uppfattning om hjärtslag - rastlöshet och förvirring
Ingen känd frekvens (kan inte beräknas utifrån tillgängliga data)
- overkliga känslor (hallucinationer)
- talstörningar
- snabbare puls
- klia
- svårt att kissa
Rapportering av biverkningar
Tala med din läkare eller apotekspersonal om du får några biverkningar. Detta inkluderar eventuella biverkningar som inte nämns i denna bipacksedel. Du kan också rapportera biverkningar direkt via det nationella rapporteringssystemet på www.agenziafarmaco.it/it/responsabili Genom att rapportera biverkningar kan du hjälpa till att tillhandahålla mer information om läkemedlets säkerhet.
Giltighetstid och lagring
Förvaras utom syn- och räckhåll för barn.
Använd inte Mictonorm efter utgångsdatumet som anges på blistret eller flaskan och på kartongen efter EXP. Utgångsdatumet avser sista dagen i månaden.
Blister: Förvaras vid högst 25 ° C. Förvara i originalförpackningen för att skydda kapslarna mot fukt.
Flaska: håll flaskan tätt stängd.
Flaskans stabilitet efter första öppnandet: 100 dagar.
Annan information
Vad Mictonorm innehåller
Den aktiva ingrediensen är propiverinhydroklorid. Varje kapsel innehåller 45 mg propiverinhydroklorid med modifierad frisättning.
Övriga innehållsämnen är citronsyra, povidon, laktosmonohydrat, talk, trietylcitrat, magnesiumstearat, metakrylsyra-metylmetakrylatsampolymer (1: 1), metakrylsyra-metylmetakrylatsampolymer (1: 2), ammoniummetakrylatsampolymer typ A, ammoniummetakrylatsampolymer typ B, gelatin, titandioxid E171, röd järnoxid E172, gul järnoxid E172.
Hur Mictonorme ser ut. Förpackningens innehåll
Mictonorm kapslar är orange och innehåller vita till benvita pellets.
De är tillgängliga i
- kartonger innehållande 14, 20, 28, 30, 49, 50, 56, 60, 84, 98, 100, 112, 168 eller 280 kapslar
- flaskor innehållande 10, 14, 20, 28, 30, 49, 50, 56, 60, 84, 98 eller 100 kapslar Polyetenflaskan med ett skruvlock av polypropen innehåller hygroskopisk kiselgel.
Alla förpackningsstorlekar kanske inte marknadsförs.
Bipacksedel: AIFA (Italian Medicines Agency). Innehåll publicerat i januari 2016. Den information som finns finns kanske inte uppdaterad.
För att få tillgång till den senaste versionen är det lämpligt att gå till AIFA (Italian Medicines Agency) webbplats. Ansvarsfriskrivning och användbar information.
01.0 LÄKEMEDLETS NAMN
MICTONORM 45 MG MODIFIERADE UTSLÄPPSKAPSULER
02.0 KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING
Varje kapsel innehåller 45 mg propiverinhydroklorid, motsvarande 40,92 mg propiverin.
Hjälpämnen: laktosmonohydrat (8,5 mg), för fullständig förteckning över hjälpämnen, se avsnitt 6.1.
03.0 LÄKEMEDELSFORM
Kapsel med modifierad frisättning, hård.
Storlek 2 orange kapslar som innehåller vita till benvita pellets.
04.0 KLINISK INFORMATION
04.1 Terapeutiska indikationer
Symtomatisk behandling av urininkontinens och / eller ökad urinfrekvens och brådska hos patienter med överaktivt urinblåsersyndrom eller detrusoröveraktivitet av neurologiskt ursprung (detrusorhyperreflexi) på grund av ryggmärgsskada.
04.2 Dosering och administreringssätt
Kapslar för oral användning.
Kapslarna får inte krossas eller tuggas.
De rekommenderade dagliga doserna är:
Vuxna: en kapsel (= 45 mg propiverinhydroklorid) en gång dagligen. Standard rekommenderad dos är en propiverin 30 mg kapsel med modifierad frisättning en gång om dagen eller en propiverin 15 mg tablett två gånger om dagen, som kan ökas till en 15 mg tablett tre gånger om dagen. Vissa patienter kan redan svara på en dos på 15 mg per dag.
Hos patienter där behandling med propiverin 15 mg tabletter indikeras tre gånger dagligen kan 15 mg tabletten tre gånger dagligen ersättas med Mictonorm 45 mg kapslar med modifierad frisättning en gång dagligen.
Den maximala dagliga dosen är en kapsel med modifierad frisättning av Mictonorm 45 mg per dag.
Äldre: Det finns i allmänhet ingen specifik dosering för äldre (se avsnitt 5.2).
Pediatrisk population: På grund av brist på data bör denna produkt inte användas till barn.
Försiktighet bör iakttas och läkaren bör noggrant övervaka patienter för eventuella biverkningar under följande förhållanden (se avsnitt 4.4, 4.5, 5.2).
Användning till patienter med nedsatt njurfunktion
Försiktighet bör iakttas vid behandlingen av denna patientgrupp. Hos patienter med allvarligt nedsatt njurfunktion (kreatininclearance svår njurinsufficiens.
Användning till patienter med nedsatt leverfunktion
Ingen dosjustering krävs hos patienter med lätt nedsatt leverfunktion; behandlingen bör dock ske med försiktighet. Inga studier har utförts på användning av propiverinhydroklorid hos patienter med måttligt eller allvarligt nedsatt leverfunktion.Det rekommenderas därför inte för dessa patienter (se avsnitt 5.2).
Patienter som får samtidig behandling med läkemedel som är potenta hämmare av CYP3A4 i kombination med metimazol
Hos patienter som genomgår behandling med potenta flavininnehållande monooxygenas (FMO) -hämmare, såsom metimazol, i kombination med potenta CYP 3A4 / 5-hämmare, bör behandlingen börja med en dos på 15 mg / dag. Dosen kan titreras till en högre. Men försiktighet bör iakttas och läkaren bör noggrant övervaka dessa patienter för eventuella biverkningar (se avsnitt 4.5, 5.2).
Det finns inga kliniskt relevanta effekter av mat på propiverins farmakokinetik (se avsnitt 5.2). Därför finns det inga särskilda rekommendationer om intag av propiverin i förhållande till mat.
04.3 Kontraindikationer
Läkemedlet är kontraindicerat hos patienter som har visat överkänslighet mot den aktiva substansen eller mot något hjälpämne och hos patienter som lider av någon av följande störningar:
- tarmobstruktion
- betydande hinder för urinblåsans utflöde med risk för urinretention
- myasthenia gravis
- tarmatoni
- svår ulcerös kolit
- giftigt megakolon
- okontrollerat glaukom med vinkelstängning
- måttligt eller svårt nedsatt leverfunktion
- takyarytmier
04.4 Särskilda varningar och lämpliga försiktighetsåtgärder vid användning
Läkemedlet ska användas med försiktighet till patienter som lider av:
- autonom neuropati
- nedsatt njurfunktion (se avsnitt 4.2)
- nedsatt leverfunktion (se avsnitt 4.2)
Efter administrering av detta läkemedel kan symptomen på följande sjukdomar förvärras:
- allvarlig hjärtsvikt (NYHA IV)
- förstorad prostata
- hiatal bråck med refluxesofagit
- hjärtarytmi
- takykardi
Propiverin, liksom andra antikolinergika, inducerar mydriasis. Därför kan risken för att framkalla akut vinkelstängningsglaukom ökas hos predisponerade individer med smala främre kammarvinklar. Läkemedel som tillhör denna klass, inklusive propiverin, har rapporterats framkalla eller utlösa akut snävvinklad glaukom.
Innan behandling påbörjas bör pollakiuri och nocturia på grund av njursjukdom eller hjärtsvikt samt organiska urinblåssjukdomar (t.ex. urinvägsinfektioner, maligna tumörer) uteslutas.
Denna produkt innehåller laktosmonohydrat. Patienter med sällsynta ärftliga störningar av galaktosintolerans, Lapp-laktasbrist eller glukos-galaktosmalabsorption bör inte ta detta läkemedel.
04.5 Interaktioner med andra läkemedel och andra former av interaktion
-En ökning av effekterna av propiverin har observerats efter samtidig administrering med tricykliska antidepressiva medel (t.ex. imipramin), lugnande medel (t.ex. bensodiazepiner), antikolinergika (vid administrering systemiskt), amantadin, neuroleptika (t.ex. fenotiaziner)) och beta-adrenerga agonister ( beta-sympatomimetika).
- En minskning av effekterna hittades efter samtidig användning av kolinerga läkemedel.
- Hos patienter som behandlas med isoniazid propiverin minskar blodtrycket.
- Prokinetikens aktivitet som metoklopramid kan å andra sidan minskas.
- Farmakokinetiska interaktioner med andra läkemedel som metaboliseras av cytokrom P450 3A4 (CYP 3A4) är möjliga. En mycket uttalad ökning av koncentrationen av dessa läkemedel förväntas dock inte, eftersom effekterna av propiverin är blygsam i jämförelse med klassiska enzymhämmare (t.ex. ketokonazol eller grapefruktjuice). Propiverin kan betraktas som en svag inhibitor av cytokrom P450 3A4. Farmakokinetiska studier har ännu inte utförts med patienter som får kraftiga CYP 3A4 -hämmare, såsom azol -svampmedel (t.ex. ketokonazol, itrakonazol) eller makrolidantibiotika (t.ex.erytromycin, klaritromycin).
Patienter som får samtidig behandling med läkemedel som är potenta hämmare av CYP3A4 i kombination med metimazol
Hos patienter som genomgår behandling med potenta flavininnehållande monooxygenas (FMO) -hämmare, såsom metimazol, i kombination med potenta CYP 3A4 / 5-hämmare, bör behandlingen börja med en dos på 15 mg / dag. Dosen kan ökas. Men försiktighet bör iakttas och läkaren bör noggrant övervaka dessa patienter för eventuella biverkningar (se avsnitt 4.2).
04.6 Graviditet och amning
I toxikologiska studier på råttor observerades inga effekter på manlig och kvinnlig fertilitet eller reproduktionsbeteende.
Inga kliniska data finns tillgängliga om användning av propiverinhydroklorid hos gravida eller ammande kvinnor. Djurstudier har visat reproduktionstoxicitet (se avsnitt 5.3) De potentiella riskerna för människor är okända.
Läkemedlet utsöndras i mjölk från däggdjur. En risk för nyfödda kan inte uteslutas. Läkemedlet ska därför inte ges till gravida eller ammande kvinnor.
04.7 Effekter på förmågan att framföra fordon och använda maskiner
Inga studier har gjorts om förmågan att framföra fordon och använda maskiner.
Propiverinhydroklorid kan orsaka dåsighet och dimsyn. Detta kan försämra patientens förmåga att utföra aktiviteter som kräver uppmärksamhet, till exempel att köra fordon eller använda maskiner, eller att utföra farligt arbete under behandling med detta läkemedel.
Lugnande medel kan öka sömnigheten som orsakas av propiverinhydroklorid.
04.8 Biverkningar
Inom systemorganklassen listas biverkningar i frekvensordning enligt följande konvention:
Mycket vanliga (≥1 / 10)
Vanliga (≥1 / 100,
Mindre vanliga (≥1 / 1000 till
Sällsynta (≥1 / 10.000,
Mycket sällsynt (
Ingen känd frekvens (kan inte beräknas utifrån tillgängliga data)
Alla biverkningar är övergående och avtar efter dosreduktion eller behandlingstopp inom högst 1 - 4 dagar.
Störningar i immunsystemet
Sällsynta: överkänslighet
Psykiatriska störningar
Mycket sällsynta: rastlöshet, förvirring
Ingen känd frekvens: hallucinationer
Nervsystemet
Vanlig: huvudvärk
Mindre vanliga: darrningar, yrsel, dysgeusi
Ögonbesvär
Vanliga: boendeavvikelser, boendestörningar, nedsatt syn
Hjärtpatologier
Mycket sällsynta: hjärtklappning
Vaskulära patologier
Mindre vanliga: minskat blodtryck med sömnighet, rodnad
Gastrointestinala störningar
Mycket vanligt: muntorrhet
Vanliga: förstoppning, buksmärtor, dyspepsi
Mindre vanliga: illamående / kräkningar
Hud och subkutan vävnad
Sällsynta: hudutslag
Njurar och urinvägar
Mindre vanliga: urinretention
Allmänna störningar och tillstånd på administreringsstället
Vanligt: trötthet
Leverenzymer bör övervakas under långtidsbehandling, eftersom en reversibel förändring av dessa enzymer sällan är möjlig. Övervakning av intraokulärt tryck rekommenderas hos patienter med risk att utveckla glaukom.
Särskild uppmärksamhet bör ägnas åt den kvarvarande urinvolymen i närvaro av urinvägsinfektioner.
Erfarenhet efter godkännande
Följande spontant rapporterade händelser härrör från erfarenhet efter godkännande, frekvensen är okänd (kan inte beräknas från tillgängliga data): talstörningar, takykardi, klåda och urinblåsa och urinrörssymtom.
Rapportering av misstänkta biverkningar
Rapportering av misstänkta biverkningar som inträffar efter godkännande av läkemedlet är viktigt eftersom det möjliggör kontinuerlig övervakning av nytta / riskbalansen för läkemedlet. Vårdpersonal uppmanas att rapportera alla misstänkta biverkningar via det nationella rapporteringssystemet. "Adress www. agenziafarmaco.gov.it/it/responsabili.
04.9 Överdosering
Symtom:
En överdos med muskarinreceptorantagonisten propiverin har potential att orsaka allvarliga antikolinerga effekter som kännetecknas av perifera symptom och störningar i centrala nervsystemet, såsom:
- svår muntorrhet
- bradykardi som kan leda till takykardi
- mydriasis och boendestörningar
- urinretention, hämning av tarmmotilitet
- rastlöshet, förvirring, hallucinationer, förvirring
yrsel, illamående, talstörningar, muskelsvaghet
En 5-årig pojke som intog 330 mg (12,69 mg / kg kroppsvikt) propiverinhydroklorid upplevde agitation, hallucinationer, nedsatt syn, mydriasis och ostadig gång. Patienten hade behandlats med aktivt kol och en bensodiazepin. Barnet hade återhämtat sig helt.
Behandling:
- Vid överdosering med propiverinhydroklorid ska patienten behandlas med en suspension av aktivt kol med mycket vatten.
- Magsköljning bör endast övervägas med "försiktighetsintubation", användning av ett välsmord rör (torra slemhinnor) och om det utförs inom en "timme" efter intag av propiverin. Kräkningar ska inte framkallas.
- Tvingad diures eller hemodialys är inte effektiva för att öka renal eliminering.
- Vid allvarliga centrala antikolinerga effekter som hallucinationer eller uttalad upphetsning kan administrering av fysostigmin försökas.
- Kramper eller uttalad excitation: behandling med bensodiazepiner.
- Andningssvikt: behandling med artificiell andning.
- Urinretention: behandling med kateterisering.
- Mydriasis: behandling med pilokarpina ögondroppar och / eller mörkare i patientens rum.
05.0 FARMAKOLOGISKA EGENSKAPER
05.1 Farmakodynamiska egenskaper
ATC -kod: G04B D06.
Farmakoterapeutisk grupp: antispasmodika i urinen.
Handlingsmekanism
Hämning av kalciuminflödet och modulering av intracellulärt kalcium i urinblåsans glatta muskelceller, vilket resulterar i en spasmolytisk effekt på muskelfibrer.
Hämning av efferenta anslutningar av bäckennerven på grund av den antikolinerga verkan.
Farmakodynamiska effekter
I djurmodeller orsakar propiverinhydroklorid en dosberoende minskning av intravesikalt tryck och en ökning av blåsans kapacitet.
Effekten beror på summan av de farmakologiska egenskaperna hos propiverin och tre aktiva urinmetaboliter, vilket visas i experiment som utförts med isolerade detrusorfibrer av humant och animaliskt ursprung.
05.2 Farmakokinetiska egenskaper
Absorption
Efter oral administrering av Mictonorm 45 mg kapslar absorberas propiverin från mag-tarmkanalen och når sin maximala plasmakoncentration efter 9-10 timmar. Den genomsnittliga absoluta biotillgängligheten för Mictonorm 45 mg kapslar är 59,5 ± 23,3% (aritmetiskt medelvärde ± SD för AUC0- ¥ (per os) / AUC0- ¥ (i.v.)).
Matintag påverkar inte propiverins farmakokinetik.
Biotillgängligheten för propiverin efter måltiden befanns vara 99% jämfört med administrering i fastande tillstånd.
Administrering av kapseln med modifierad frisättning resulterar i genomsnittliga Cmax-koncentrationer av propiverin på cirka 70 ng / ml, uppnådda inom 9,5 timmar efter administrering.
Distribution
Efter administrering av Mictonorm 45 mg kapslar uppnås steady state efter fyra till fem dagar, vid en högre koncentration än efter engångsdos (C -genomsnitt = 71 ng / ml). Det rapporterades att efter intravenös administrering av propiverinhydroklorid till 21 friska frivilliga varierade distributionsvolymen från 125 till 473 l (medelvärde 279 l), vilket innebär att en stor andel av tillgängligt propiverin distribueras till perifera fack. Plasmaproteinbindningen uppgår till 90 - 95% för modersubstansen och cirka 60% för huvudmetaboliten.
Farmakokinetiska egenskaper (geometriskt medelvärde, ± SD, intervall) för propiverin hos 10 friska frivilliga efter en enda administrering av Mictonorm 30 mg kapslar med modifierad frisättning och Mictonorm 45 mg kapslar med modifierad frisättning
Propeaders egenskaper vid steady state efter administrering av flera doser av Mictonorm 45 mg kapslar med modifierad frisättning en gång dagligen i 7 dagar till 24 friska frivilliga
PTF = minsta-maximala fluktuationer
Biotransformation
Propiverin metaboliseras i stor utsträckning av tarm- och leverenzymer. Den huvudsakliga metabola vägen involverar oxidation av piperidyl-N och förmedlas av CYP 3A4 och av det flavininnehållande monooxygenas (FMO) 1 och 3 och leder till bildandet av den mycket mindre aktiva N-oxidföreningen, vars plasmakoncentration kraftigt Fyra metaboliter har identifierats i urinen, varav tre är farmakologiskt aktiva och kan bidra till terapeutisk effekt.
In vitro kan en liten hämning av CYP 3A4 och CYP 2D6 detekteras, som uppträder vid koncentrationer över terapeutiska plasmakoncentrationer med 10 - 100 gånger (se avsnitt 4.5).
Eliminering
Efter administrering av en oral dos på 30 mg 14C-propiverinhydroklorid till friska frivilliga upptäcks 60% av radioaktiviteten i urinen och 21% i avföringen inom 12 dagar. Mindre än 1% av en oralt administrerad dos utsöndras oförändrat i urinen. Den genomsnittliga totala clearance efter administrering av en enda 30 mg dos är 371 ml / min (191 - 870 ml / min).
Linearitet / icke-linjäritet
Efter oral administrering av 10-45 mg propiverinhydroklorid, ökade Cmax och AUC0-? I linjärt samband med dos.
Egenskaper hos patienter
Nedsatt njurfunktion:
Allvarligt nedsatt njurfunktion förändrar inte signifikant kinetiken för propiverin och dess huvudsakliga metabolit, propiverin-N-oxid, vilket visas i en endosstudie på 12 patienter med kreatininclearance.
Leversvikt:
Liknande farmakokinetiska värden vid steady state hittades hos 12 patienter med lätt till måttligt nedsatt leverfunktion på grund av fet leversjukdom, jämfört med de som hittades i 12 friska kontrollpersoner. Inga data finns tillgängliga för allvarligt nedsatt leverfunktion.
Ålder:
När man jämförde plasmakoncentrationerna under steady state hittades inga skillnader mellan äldre patienter (60 - 85 år, genomsnitt 68 år) och friska unga försökspersoner. Förhållandet mellan moderföreningen och metaboliten förblir oförändrat hos äldre patienter, vilket indikerar att metabolisk omvandling av propiverin till dess huvudmetabolit, propiverin-N-oxid, inte är en begränsande eller relaterad faktor. "Ålder.
05.3 Prekliniska säkerhetsdata
I studier som utförts med långvarig oral administrering hos två däggdjursarter var den huvudsakliga behandlingsrelaterade effekten leverförändringar (inklusive en ökning av leverenzymer). Dessa kännetecknades av hepatisk hypertrofi och fettleverdegeneration. Fettleverdegeneration var reversibel vid slutet av behandlingen.
I djurstudier hittades förseningar i skelettillväxten hos avkomman efter oral administrering av höga doser av läkemedlet till gravida kvinnor. Under amning utsöndrades propiverinhydroklorid i bröstmjölk.
Inga mutagena effekter hittades. Carcinogenicitetsstudier som utförts på möss visade en ökad förekomst av hepatocellulära adenom och karcinom hos högdos hanhundar. Hepatocellulära adenom, renala adenom och urinblåsan papillom hittades hos hanråttor i cancerframkallande studier på råttor. Behandlade med höga doser, medan hos kvinnor polyper av endometrial stroma ökades med höga doser. Båda tumörer som hittades hos råttor och de som hittades hos möss ansågs vara artspecifika och därför inte kliniskt relevanta.
I toxikologiska studier på råttor observerades inga effekter på manlig och kvinnlig fertilitet eller reproduktionsbeteende.
06.0 LÄKEMEDELSINFORMATION
06.1 Hjälpämnen
Pellets
Citronsyra;
povidon;
laktosmonohydrat;
talk;
trietylcitrat;
magnesiumstearat;
metakrylsyra-metylmetakrylatsampolymer (1: 1);
metakrylsyra-metylmetakrylatsampolymer (1: 2);
ammoniummetakrylatsampolymer typ A;
ammoniummetakrylatsampolymer typ B.
Kapsel
Gelé;
titandioxid E171;
röd järnoxid E172;
gul järnoxid E172.
06.2 Oförenlighet
Inte relevant.
06.3 Giltighetstid
3 år.
Flaska:
Stabilitet efter första öppnandet: 100 dagar.
06.4 Särskilda förvaringsanvisningar
Blåsa:
Förvara i originalförpackningen för att skydda mot fukt.
Förvaras vid högst 25 ° C.
Flaska:
Håll flaskan väl tillsluten.
06.5 Förpackningens innehåll och förpackningens innehåll
Blister av PVC / PVDC och aluminium i förpackningar innehållande 14, 20, 28, 30, 49, 50, 56, 60, 84, 98, 100, 112, 168 eller 280 kapslar.
Polyetenflaskor med ett skruvlock av polypropen som innehåller en hygroskopisk kiselgel med 10, 14, 20, 28, 30, 49, 50, 56, 60, 84, 98 eller 100 kapslar.
Alla förpackningsstorlekar kanske inte marknadsförs.
06.6 Anvisningar för användning och hantering
Inga speciella instruktioner.
07.0 INNEHAVARE AV GODKÄNNANDE FÖR FÖRSÄLJNING
APOGEPHA Arzneimittel GmbH
Kyffhäuserstra? Och 27
01309 Dresden
Tyskland
08.0 NUMMER FÖR FÖRSÄLJNINGSTILLSTÅND
AIC n. 037768367 - "45 mg kapslar med modifierad frisättning" 14 kapslar i PVC / PVDC / AL -blister
AIC n. 037768379- "45 mg kapslar med modifierad frisättning" 20 kapslar i PVC / PVDC / AL-blister
AIC n. 037768381 - "45 mg kapslar med modifierad frisättning" 28 kapslar i PVC / PVDC / AL -blister
AIC n. 037768393 - "45 mg kapslar med modifierad frisättning" 30 kapslar i PVC / PVDC / AL -blister
AIC n. 037768405 - "45 mg kapslar med modifierad frisättning" 49 kapslar i PVC / PVDC / AL -blister
AIC n. 037768417 - "45 mg kapslar med modifierad frisättning" 50 kapslar i PVC / PVDC / AL -blister
AIC n. 037768429 - "45 mg kapslar med modifierad frisättning" 56 kapslar i PVC / PVDC / AL -blister
AIC n. 037768431 - "45 mg kapslar med modifierad frisättning" 60 kapslar i PVC / PVDC / AL -blister
AIC n. 037768443 - "45 mg kapslar med modifierad frisättning" 84 kapslar i PVC / PVDC / AL -blister
AIC n. 037768456 - "45 mg kapslar med modifierad frisättning" 98 kapslar i PVC / PVDC / AL -blister
AIC n. 037768468 - "45 mg kapslar med modifierad frisättning" 100 kapslar i PVC / PVDC / AL -blister
AIC n. 037768470 - "45 mg kapslar med modifierad frisättning" 112 kapslar i PVC / PVDC / AL -blister
AIC n. 037768482 - "45 mg kapslar med modifierad frisättning" 168 kapslar i PVC / PVDC / AL -blister
AIC n. 037768494 - "45 mg kapslar med modifierad frisättning" 280 kapslar i PVC / PVDC / AL -blister
AIC n. 037768506 - "45 mg kapslar med modifierad frisättning" 10 kapslar i PE -flaska
AIC n. 037768518 - "45 mg kapslar med modifierad frisättning" 14 kapslar i PE -flaska
AIC n. 037768520 - "45 mg kapslar med modifierad frisättning" 20 kapslar i PE -flaska
AIC n. 037768532 - "45 mg kapslar med modifierad frisättning" 28 kapslar i PE -flaska
AIC n. 037768544 - "45 mg kapslar med modifierad frisättning" 30 kapslar i PE -flaska
AIC n. 037768557 - "45 mg kapslar med modifierad frisättning" 49 kapslar i PE -flaska
AIC n. 037768569 - "45 mg kapslar med modifierad frisättning" 50 kapslar i PE -flaska
AIC n. 037768571 - "45 mg kapslar med modifierad frisättning" 56 kapslar i PE -flaska
AIC n. 037768583 - "45 mg kapslar med modifierad frisättning" 60 kapslar i PE -flaska
AIC n. 037768595 - "45 mg kapslar med modifierad frisättning" 84 kapslar i PE -flaska
AIC n. 037768607 - "45 mg kapslar med modifierad frisättning" 98 kapslar i PE -flaska
AIC n. 037768619 - "45 mg kapslar med modifierad frisättning" 100 kapslar i PE -flaska
09.0 DATUM FÖR FÖRSTA GODKÄNNANDE ELLER FÖRNYELSE AV GODKÄNNANDET
Datum för första godkännandet: 15 maj 2015
Datum för senaste förnyelse: 11 maj 2016
10.0 DATUM FÖR REVISION AV TEXTEN
05/2016