Aktiva ingredienser: Interferon beta-1a
AVONEX 30 mikrogram / 0,5 ml injektionsvätska, lösning
Avonex förpackningsinsatser är tillgängliga för förpackningsstorlekar:- AVONEX 30 mikrogram / 0,5 ml injektionsvätska, lösning
- AVONEX 30 mikrogram / 0,5 ml injektionsvätska, lösning, i förfylld injektionspenna
Varför används Avonex? Vad är det för?
Vad är AVONEX
Den aktiva substansen i Avonex är ett protein som kallas interferon beta-1a. Interferoner är naturliga ämnen som kroppen producerar för att skydda sig mot infektioner och sjukdomar. Proteinet i Avonex har exakt samma sammansättning som interferon beta som produceras av människokroppen.
Vad är AVONEX
Avonex används för att behandla multipel skleros (MS). Behandling med Avonex kan hjälpa dig att undvika att bli värre, även om det inte kan bota MS.
Var och en har en individuell variation av MS -symptom. Möjliga symptom inkluderar:
- Yrsel eller obalans, gångproblem, muskelstelhet och spasmer, trötthet, domningar i ansikte, armar eller ben
- Akut eller kronisk smärta, urinblåsa eller tarm, sexuella problem och synstörningar
- Svårt att tänka och koncentrera sig, depression.
MS tenderar också att blossa upp då och då: detta fenomen kallas återfall (återfall).
(Ytterligare information)
Avonex fungerar bäst när det tas regelbundet, en gång i veckan, samtidigt. Sluta inte ta Avonex utan att först tala med din neurolog.
Avonex kan hjälpa till att minska antalet återfall (återfall) du kan få och bromsa den inaktiverande utvecklingen av MS. Din läkare kommer att berätta för dig hur lång tid du ska ta Avonex eller när det är dags att sluta.
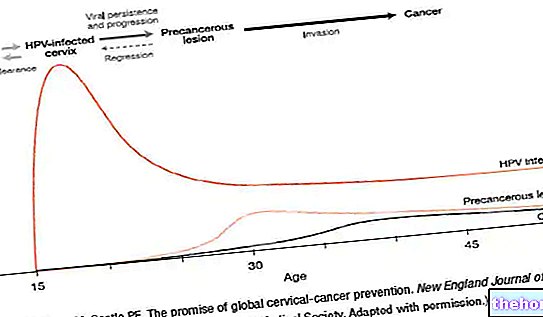
Hur AVONEX fungerar
Multipel skleros är associerad med skador på nerverna (hjärna eller ryggmärg). Vid MS reagerar immunsystemet genom att attackera myelin - den "isolerande" beläggningen som omger nervfibrer. Skador på myelin försämrar utbytet av meddelanden mellan hjärnan och andra delar av kroppen. Detta är vad som orsakar MS -symptom. Avonex verkar verkar vara att stoppa kroppens immunsystem från att attackera myelin.
Kontraindikationer När Avonex inte ska användas
Använd inte AVONEX:
- Om du är allergisk mot interferon beta eller något annat innehållsämne i detta läkemedel (anges i avsnitt 6)
- Om du är gravid, börja inte använda Avonex
- Om du har svår depression eller funderar på självmord.
Tala omedelbart för din läkare om du har någon av dessa omständigheter.
(Ytterligare information)
Avonex och allergiska reaktioner. Eftersom Avonex innehåller ett protein finns det en liten risk för en allergisk reaktion.
Mer om depression. Om du har svår depression eller har tankar på självmord, ska du inte använda Avonex. Om du har depression kan din läkare fortfarande förskriva Avonex, men det är viktigt att du berättar det för din läkare om du har drabbats av depression eller andra liknande humörstörningar.
Försiktighetsåtgärder vid användning Vad du behöver veta innan du tar Avonex
Varningar och försiktighetsåtgärder
Tala med din läkare innan du använder Avonex om du lider eller tidigare har lidit av följande problem:
- Depression eller humörproblem
- Tankar om självmord.
Du bör omedelbart rapportera eventuella humörsvängningar, självmordstankar, ovanliga känslor av sorg, ångest eller svaghet till din läkare.
- Epilepsi eller andra liknande sjukdomar som inte kontrolleras av läkemedel
- Allvarliga njur- eller leverproblem
- Låg mängd vita blodkroppar eller blodplättar, vilket kan öka risken för infektion, blödning eller anemi
- Hjärtproblem, som kan orsaka symtom som bröstsmärta (kärlkramp) särskilt efter fysisk aktivitet, svullna vrister, andfåddhet (hjärtsvikt) eller oregelbunden hjärtslag (arytmier).
Tala med din läkare om du har något av dessa tillstånd, eller om de blir värre när du använder Avonex.
Trombi (blodproppar) kan bildas inuti små blodkärl under behandlingen. Dessa tromber kan ha effekt på njurarna. Trombbildning kan uppstå flera veckor till flera år efter behandling med Avonex.
Din läkare kan besluta att kontrollera ditt blodtryck, blod (trombocyttal) och njurfunktion. Tala om för din läkare att du tar Avonex:
- Om du måste göra ett blodprov, eftersom Avonex kan ändra resultaten.
(Ytterligare information)
I vissa fall måste du berätta för din vårdpersonal att du använder Avonex. Om du till exempel ordinerar andra läkemedel eller behöver ta ett blodprov kan Avonex ändra effekten av läkemedlen eller testresultaten.
Interaktioner Vilka mediciner eller livsmedel kan förändra effekten av Avonex
Tala om för din läkare om du tar andra läkemedel, särskilt läkemedel mot epilepsi och depression. Avonex kan påverka eller påverkas av andra läkemedel. Detta gäller alla mediciner, inklusive receptfria.
Varningar Det är viktigt att veta att:
Graviditet och amning
Om du är gravid, börja inte använda Avonex.
- om du är i fertil ålder och sexuellt aktiv måste du använda tillräckligt preventivmedel när du tar Avonex.
- om du planerar att bli gravid eller bli gravid medan du använder Avonex, tala med din läkare för att diskutera om behandlingen ska fortsätta eller inte.
- om du redan är gravid eller tror att du är gravid, kontakta din läkare så snart som möjligt.
- om du tänker amma, tala med din läkare först.
Köra och använda maskiner
Om du känner dig yr, kör inte. Hos vissa människor orsakar Avonex yrseleffekt. Om detta händer dig, eller om du har andra biverkningar som kan påverka din förmåga, ska du inte köra bil eller använda maskiner.
Viktig information om några av ingredienserna i AVONEX
Detta läkemedel är i huvudsak "natriumfritt". Den innehåller mindre än 23 mg (1 mmol) natrium per veckodos.
Dos, metod och administreringstid Hur man använder Avonex: Dosering
Den rekommenderade dosen för vuxna och ungdomar 12 år och äldre.
En injektion av Avonex per vecka.
Försök att ta Avonex varje vecka, alltid samma dag och samtidigt.
Inte för barn
Avonex ska inte användas till barn under 12 år.
Om du har bestämt dig för att påbörja behandling med Avonex kan din läkare förse dig med ett Avostartclip -titreringskit. Avostartclip kläms fast på sprutan och låter dig gradvis öka dosen Avonex i början av behandlingen. Detta begränsar de influensaliknande symtomen som vissa människor upplever när de börjar använda Avonex. Din läkare eller sjuksköterska kommer att lära dig att använda Avostartclip -titreringssatsen.
(Ytterligare information)
Start av Avonex -terapi
Om du aldrig har tagit Avonex tidigare kan din läkare råda dig att gradvis öka dosen för att vänja dig vid effekterna av Avonex innan du tar hela dosen. Du kommer sannolikt att få ett Avostartclip -titreringskit, som är monterat på sprutan, vilket möjliggör administrering av en reducerad dos Avonex i början av behandlingen. Varje Avostartclip är endast för engångsbruk och måste sedan kasseras tillsammans med återstående Avonex. Fråga din läkare för mer information om hur du använder denna enhet.
Utför injektionen själv
Du kan injicera Avonex utan din läkares hjälp om du har fått veta hur du gör det.Instruktioner för injektion finns i slutet av denna bipacksedel (se avsnitt 7, Hur man injicerar AVONEX).
Om du har problem med att hantera sprutan, kontakta din läkare, som kan hjälpa dig.
(Ytterligare information)
Längst ner i bipacksedeln hittar du mer information om hur du injicerar Avonex.
Alternativ nål:
En injektionsnål ingår redan i Avonex -förpackningen. Din läkare kan ordinera en kortare, tunnare nål beroende på dina fysiska egenskaper. Tala med din läkare om du tror att så är fallet.
Om du har problem med att hantera sprutan, tala med din läkare om att använda ett lämpligt verktyg. Detta verktyg består av en hållare som är speciellt utformad för att underlätta injektionen av Avonex Hur länge du ska använda AVONEX Din läkare kommer att bestämma hur länge du behöver använda Avonex. Det är viktigt att fortsätta använda Avonex regelbundet. på råd från din läkare ..
Hur man injicerar AVONEX
Du måste redan ha fått instruktioner om hur du injicerar Avonex. Dessa anvisningar är bara en påminnelse. Fråga din läkare eller apotekspersonal om du har ytterligare frågor.
Val av injektionsstället
- Avonex injiceras i en muskel, till exempel en av de övre lårmusklerna. Det rekommenderas inte att injicera Avonex i skinkorna.
- Välj en annan injektionsplats varje vecka. Detta minskar risken för hud- eller muskelirritation.
- Välj inte hudområden med blåmärken, skador eller infektioner och injicera inte i ett öppet sår.
Förberedelse
- Ta bort ett förseglat fack från kylskåpet - Kontrollera utgångsdatumet på brickans lock. Använd inte produkten om den har gått ut. - Ta bort pappersluckan helt. Kontrollera att brickan innehåller en förfylld spruta och en injektionsnål (se figuren "Plastbrickans innehåll").
- Låt sprutan värmas upp - Låt sprutan stå i rumstemperatur i en halvtimme. Detta gör det bekvämare att injicera än att injicera direkt efter att den tagits ut ur kylskåpet. Varning: Använd inte externa värmekällor, till exempel varmt vatten, för att värma sprutan.
- Tvätta händerna noggrant med tvål och vatten och torka dem.
- Förbered alkoholservetter och plåster (medföljer ej) om du behöver dem. Leta efter en ren, hård yta för att lägga det material som behövs för injektionen. Placera brickan på den.
Förberedelse av injektionen
- Kontrollera vätskan i sprutan, den ska se klar och färglös ut. Om lösningen är grumlig eller färgad, eller om suspenderade partiklar är synliga, använd inte den förfyllda sprutan.
- Ta bort sprutlocket Sprutan har ett vitt skydd mot lock. Se till att locket är intakt och inte har öppnats. Om det ser ut som att locket har öppnats ska du inte använda sprutan. Håll sprutan med det vita locket uppåt. Böj locket i rät vinkel tills det sticker ut. Rör inte vid leden. Tryck inte på kolven.
- Fästa nålen Öppna nålen för att exponera leden. Behåll den skyddande omslaget på nålen. Tryck in nålen på sprutan. Vrid den medurs tills den klickar på plats. Varning: Se till att nålen är helt införd i sprutan, annars kan den läcka. Om du har blivit tillsagd att öka din Avonex -dos gradvis kan du behöva ett Avostartclip -titreringskit från din läkare. Fråga din läkare för mer information. Ta nu bort den skyddande förpackningen från nålen. Rotera inte den. Varning: Om du roterar det skyddande omslaget när du tar bort det kan du också av misstag ta bort nålen.
Utför injektionen
- Rengör och sträck injektionsstället. Om så önskas, använd en alkoholservett för att rengöra huden på det valda injektionsstället. Vänta tills huden har torkat. Sträck ut huden runt injektionsstället med en hand. Slappna av muskeln.
- Utför injektionen. Stick in nålen i muskeln med ett snabbt tryck vinkelrätt mot huden. Nålen ska gå hela vägen in. Tryck långsamt ned kolven tills sprutan är tom. Om du använder sprutan med Avostartclip får du en lägre dos Avonex. Sprutan töms inte.
- Dra ut nålen. Ta bort injektionsnålen genom att hålla huden ordentligt utsträckt eller komprimerad runt injektionsstället. Om du använder bomullspinnar med alkohol, placera en över injektionsstället. Om du vill, applicera en lapp på platsen. Injektion .
Kassera använt material på rätt sätt
Efter injektionen, lägg nålen och sprutan i en lämplig behållare (en behållare för vassa), inte i hushållsavfall. Om du har använt Avostartclip måste du kasta sprutan (och Avostartclip) efter injektion. Den oanvända delen av Avonex ska inte återanvändas. Papper och pinnar kan läggas i en vanlig papperskorg.
Överdosering Vad du ska göra om du har tagit för mycket Avonex
Om du injicerar för mycket
Du behöver bara ha en Avonex -injektion per vecka. Om du har haft mer än en "Avonex -injektion" på tre dagar, rådfråga din läkare eller apotekspersonal omedelbart.
Om du glömmer en injektion
Om du saknar den vanliga veckodosen, injicera en dos så snart som möjligt. Låt sedan en vecka gå innan din nästa Avonex -injektion. Fortsätt injektionerna denna nya dag varje vecka. Om det är en viss dag i veckan som du föredrar att injicera, be din läkare om instruktioner om hur du ska återföra injektionen till din önskade dag.
Injicera inte en dubbel dos för att kompensera för en glömd dos.
Biverkningar Vilka är biverkningarna av Avonex
Liksom alla läkemedel kan detta läkemedel orsaka biverkningar men alla användare behöver inte få dem.
(Ytterligare information)
Även om listan över möjliga biverkningar verkar oroande, kanske du inte upplever någon av dem.
Allvarliga biverkningar: uppsök läkare
Allvarliga allergiska reaktioner
Om det inträffar:
- Svullnad i ansikte, läppar eller tunga
- Andningssvårigheter
- Rodnad
ring din läkare omedelbart. Fortsätt inte använda Avonex förrän du har informerat din läkare.
Depression
Om du upplever symptom på depression:
- Ovanlig känsla av sorg, ångest eller känsla av värdelöshet
ring din läkare omedelbart.
Leverproblem
Om det inträffar:
- Gulning av huden eller ögonvitorna (gulsot)
- Utbredd klåda
- Illamående och kräkningar
- Lätt att få blåmärken ring din läkare omedelbart, eftersom det kan vara symptom på ett leverproblem.
Biverkningar som finns i kliniska prövningar
(Ytterligare information)
Biverkningar som finns i kliniska prövningar. Detta är biverkningar som rapporterats under tiden Avonex studerades. Siffrorna som visas är baserade på antalet personer som har rapporterat effekten och används för att ge en uppfattning om sannolikheten för att du också kan påverkas av den aktuella biverkningen.
Mycket vanliga biverkningar (drabbar minst 1 av 10 personer)
- influensaliknande symptom-huvudvärk, kroppsvärk, frossa eller feber: se influensaliknande symptom nedan
- huvudvärk.
Vanliga biverkningar (drabbar färre än 1 av 10 personer)
- Aptitlöshet
- Känsla av svaghet och trötthet
- Svårt att sova
- Depression
- Rodnad
- Rinnande näsa
- Diarre
- Illamående eller kräkningar
- Domningar eller stickningar i huden
- Erytem eller blåmärken
- Ökad svettning, nattliga svettningar
- Muskel- eller ledvärk, smärta i armar, ben eller nacke
- Muskelkramper, muskel- eller ledstelhet
- Smärta, blåmärken och rodnad på injektionsstället
- Förändringar i blodprovsresultat. Symtom du kan märka är trötthet, upprepade infektioner, blåmärken eller oförklarlig blödning.
Mindre vanliga biverkningar (drabbar färre än 1 av 100 personer)
- Håravfall
- Förändringar i menstruationscykeln
- Brännande känsla vid injektionsstället.
Sällsynta biverkningar (drabbar färre än 1 av 1000 personer)
- Andningssvårigheter.
- Njurproblem, inklusive ärrbildning, som kan minska njurfunktionen Om du får några eller alla dessa symtom: Skummande urin Trötthet Svullnad, särskilt i anklar och ögonlock, och viktökning. Tala om för din läkare eftersom det kan vara tecken på ett eventuellt njurproblem.
- Trombus (blodproppar) i små blodkärl som kan påverka njurarna (trombotisk trombocytopenisk purpura eller hemolytiskt uremiskt syndrom) Symtom kan vara ökade blåmärken, blödningar, feber, extrem svaghet, huvudvärk, yrsel eller yrsel Din läkare kommer sannolikt att hitta förändringar i ditt blod och din njurfunktion Om någon av dessa biverkningar stör dig, tala med din läkare.
Andra biverkningar
(Ytterligare information)
Dessa effekter har setts hos personer som använder Avonex, men det är inte känt vilken sannolikhet det är för dem att uppstå.
- Hypo- eller hypertyreos
- Nervositet eller ångest, känslomässig instabilitet, irrationella tankar eller hallucinationer (inbillade syner eller ljud), förvirring, självmordstankar
- Domningar, yrsel, anfall och migrän
- Medvetenhet om hjärtslag (hjärtklappning), snabb eller oregelbunden hjärtfrekvens, hjärtproblem med följande symtom: minskad träningsförmåga, oförmåga att ligga i sängen, andfåddhet eller svullna anklar
- Leverproblem, beskrivna ovan
- Nässelutslag eller vesikulära utslag, klåda eller uppblossning av psoriasis, om du har dem
- Svullnad eller blödning på injektionsstället eller bröstsmärta efter injektion
- Viktökning eller förlust
- Förändringar i laboratorietestresultat, inklusive leverfunktionstester.
Om någon av dessa biverkningar stör dig, tala med din läkare.
Oönskade effekter av injektionen
- Svimning: Din första injektion av Avonex kan ges av din läkare, eftersom det kan göra att du känner dig svag eller faktiskt kan få dig att svimma. Detta kommer sannolikt inte att hända mer än en gång.
- Omedelbart efter injektionen kan du uppleva muskelhypertoni eller svaghet - en återfallsliknande effekt av MS. Detta är sällsynt, inträffar bara vid injektionstillfället och går över strax efter. Denna biverkning kan dock uppstå när som helst efter att Avonex -behandlingen påbörjats.
- Om du märker någon irritation eller hudproblem efter injektionen, tala med din läkare.
Influensaliknande symptom
(Ytterligare information)
Tre enkla sätt att minska intensiteten av influensaliknande symptom:
- Injicera Avonex strax före sänggåendet. Så när biverkningar uppstår kommer du att sova.
- Ta paracetamol eller ibuprofen en halvtimme innan Avonex -injektionen och fortsätt att ta dem i ytterligare en dag. Få råd om lämplig dos från din läkare eller apotekspersonal.
- Om du får feber, drick mycket vatten för att hålla kroppen hydratiserad.
Efter att ha injicerat dosen Avonex känner vissa att de har influensa. Symtomen är:
- Huvudvärk
- Muskelvärk
- Frossa eller feber.
Dessa symtom härrör inte från en riktig influensa.
Av denna anledning ska han inte vara rädd för att smitta andra människor. Symtom av denna typ är vanligare i början av Avonex-behandlingen. Din läkare kan ge dig ett Avostartclip-titreringskit som gör att du gradvis kan öka din dos i början av behandlingen, vilket hjälper dig att begränsa influensaliknande symptom. När du fortsätter med injektionerna kommer de influensaliknande symptomen gradvis att avta.
Rapportering av biverkningar
Tala med din läkare eller apotekspersonal om du får några biverkningar. Detta inkluderar eventuella biverkningar som inte nämns i denna bipacksedel. Du kan också rapportera biverkningar direkt via det nationella rapporteringssystemet som anges i bilaga V. Genom att rapportera biverkningar kan du hjälpa till att ge mer information om säkerheten för detta läkemedel.
Giltighetstid och lagring
Förvara detta läkemedel utom syn- och räckhåll för barn.
Använd inte detta läkemedel efter utgångsdatumet som står på etiketten Utgångsdatumet avser den sista dagen i den månaden. C.
Förvara i originalförpackningen (förseglad plastbricka) för att skydda läkemedlet från ljus. Förvaras i kylskåp (mellan 2 ° C och 8 ° C). Frys inte.
Avonex kan också förvaras vid rumstemperatur (mellan 15 ° C och 30 ° C) i högst en vecka.
ANVÄND INTE Avonex om du märker att:
- den förfyllda sprutan är trasig.
- den förseglade plastbrickan är skadad eller öppen.
- lösningen verkar inte färglös eller om suspenderade partiklar är synliga.
- det manipuleringsskyddade locket är trasigt.
Kasta inga läkemedel i avloppsvatten eller hushållsavfall. Fråga din apotekare om hur du ska kasta läkemedel som du inte längre använder. Detta hjälper till att skydda miljön.
Sammansättning och läkemedelsform
Vad AVONEX
Den aktiva substansen är: interferon beta-1a, 30 mikrogram / 0,5 ml
Övriga innehållsämnen är: natriumacetat, trihydrat, isättika, argininhydroklorid, polysorbat 20 och vatten för injektionsvätskor.
Hur AVONEX ser ut och förpackningens innehåll
Avonex injektionsvätska, lösning består av färdiga injektioner.
Ett förpackning med Avonex innehåller fyra eller tolv färdiga (förfyllda) sprutor, var och en innehållande 0,5 ml klar, färglös vätska. Alla förpackningsstorlekar kanske inte marknadsförs. Varje spruta är förpackad i en behållare av förseglad plast. injektionsnål ingår också i varje förpackning.
Bipacksedel: AIFA (Italian Medicines Agency). Innehåll publicerat i januari 2016. Den information som finns finns kanske inte uppdaterad.
För att få tillgång till den senaste versionen är det lämpligt att gå till AIFA (Italian Medicines Agency) webbplats. Ansvarsfriskrivning och användbar information.
01.0 LÄKEMEDLETS NAMN
AVONEX 30 MCG / 0,5 ML INJEKTIONSLÖSNING
02.0 KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING
Varje 0,5 ml förfylld spruta innehåller 30 mikrogram (6 miljoner IE) interferon beta-1a.
Koncentrationen är lika med 30 mcg per 0,5 ml.
Med hjälp av Världshälsoorganisationens (WHO) internationella standard för interferon innehåller 30 mcg AVONEX 6 miljoner IE antiviral aktivitet. Aktiviteten relaterad till andra standarder är inte känd.
För fullständig förteckning över hjälpämnen, se avsnitt 6.1.
03.0 LÄKEMEDELSFORM
Injicerbar lösning.
Klar och färglös lösning.
04.0 KLINISK INFORMATION
04.1 Terapeutiska indikationer
AVONEX är indicerat för behandling av:
• Patienter som diagnostiseras med återfallande multipel skleros (MS). I kliniska prövningar kännetecknades detta av två eller flera akuta exacerbationer (återfall) under de tre föregående åren utan tecken på fortsatt progression mellan återfall; AVONEX bromsar utvecklingen av funktionshinder och minskar frekvensen av återfall.
• Patienter med en enda demyeliniserande händelse med en aktiv inflammatorisk process, om denna händelse är tillräckligt allvarlig för att kräva behandling med intravenösa kortikosteroider, har andra diagnoser uteslutits och om det har fastställts att patienter har hög risk att utveckla kliniskt definierad multipel skleros (se avsnitt 5.1).
AVONEX ska avbrytas hos patienter som utvecklar progressiv MS.
04.2 Dosering och administreringssätt
Behandlingen bör inledas under överinseende av en läkare med erfarenhet av behandling av sjukdomen.
Dosering
Vuxna: den rekommenderade dosen för behandling av återfallande MS -former är 30 mikrogram (0,5 ml lösning), administrerad genom intramuskulär (IM) injektion en gång i veckan (se avsnitt 6.6). Ingen ytterligare fördel visades genom administrering av en högre dos (60 mcg) en gång i veckan.
Titrering: För att hjälpa patienter att minska förekomsten och svårighetsgraden av influensaliknande symptom (se avsnitt 4.8) kan titrering utföras vid behandlingens början.
Titrering kan uppnås med antingen BIOSET eller förfylld spruta genom att starta behandlingen i ¼ veckodosintervall tills full dos (30 mcg / vecka) uppnås vid vecka 4.
Ett alternativt titreringsschema kan erhållas genom att påbörja behandling med cirka ½ dos AVONEX en gång i veckan innan den når hela dosen. För att uppnå tillräcklig behandlingseffekt bör en dos på 30 mikrogram per vecka uppnås och bibehållas efter den initiala titreringsperioden.
AVOSTARTCLIP Titration Kit har utformats för att endast användas med den förfyllda sprutan. Den kan användas för att uppnå ¼ eller ½ dossteg. Varje AVOSTARTCLIP ska användas en gång och sedan kasseras med AVONEX -innehållet kvar i sprutan.
Före injektionen och ytterligare 24 timmar efter varje injektion rekommenderas ett febernedsättande smärtstillande medel för att minska de influensaliknande symtomen i samband med administrering av AVONEX. Dessa symtom är vanligtvis närvarande under de första månaderna av behandlingen.
Pediatrisk population: Säkerhet och effekt för AVONEX hos ungdomar i åldern 12 till 16 år har ännu inte fastställts. För närvarande finns tillgängliga data beskrivna i avsnitt 4.8 och 5.1 men ingen rekommendation om dosering kan ges.
Säkerhet och effekt för AVONEX hos barn under 12 år har ännu inte fastställts. Det finns inga tillgängliga data.
Pensionärer: kliniska prövningar inkluderade inte tillräckligt med patienter i åldern 65 år och över för att avgöra om de svarar annorlunda än yngre försökspersoner. Baserat på sättet för clearance av den aktiva substansen finns det dock ingen teoretisk anledning till att dosjustering är nödvändig hos äldre patienter.
Administreringssätt
Platsen för intramuskulär injektion bör bytas varje vecka (se avsnitt 5.3).
Din läkare kan ordinera en nål med en diameter på 25 x 25 mm för patienter där det är lämpligt att använda denna nål för administrering av en intramuskulär injektion.
Det är för närvarande okänt hur länge patienten ska behandlas. Patienter ska kliniskt utvärderas efter två års behandling och beslutet om längre behandling ska fattas individuellt av den behandlande läkaren. Behandlingen ska avbrytas om patienten utvecklar kronisk progressiv MS.
04.3 Kontraindikationer
- Start av behandling under graviditet (se avsnitt 4.6).
- Patienter med historisk överkänslighet mot naturligt eller rekombinant interferon beta eller mot något hjälpämne som anges i avsnitt 6.1.
- Patienter med svår depression och / eller pågående självmordstankar (se avsnitt 4.4 och 4.8).
04.4 Särskilda varningar och lämpliga försiktighetsåtgärder vid användning
AVONEX ska administreras med försiktighet till patienter med nuvarande eller tidigare depressivt syndrom eller andra humörstörningar, särskilt patienter med tidigare självmordstankar (se avsnitt 4.3). Depression och självmordsidé är kända för att tillstånd förekommer oftare hos patienter med multipel skleros och i samband med användning av interferon. Patienter bör rådas att omedelbart rapportera alla symptom på depression och / eller självmordstankar till sin behandlande läkare.
Patienter med tecken på depression bör övervakas noga under behandlingen och behandlas på lämpligt sätt. Avbrytande av AVONEX -behandling bör övervägas (se även avsnitt 4.3 och 4.8).
AVONEX ska ges med försiktighet till patienter med anfall i anamnesen och till dem som behandlas med antiepileptika, särskilt om deras epilepsi inte kontrolleras tillräckligt av antiepileptika (se avsnitt 4.5 och 4.8).
Försiktighet bör iakttas och noggrann övervakning övervägas vid administrering av AVONEX till patienter med allvarligt nedsatt njur- och leverfunktion och till patienter med svår myelosuppression.
Trombotisk mikroangiopati (TMA): Det har rapporterats om TMA som manifesteras som trombotisk trombocytopen purpura (TTP) eller hemolytiskt uremiskt syndrom (HUS), inklusive dödliga fall med interferon-beta-produkter. Händelserna har rapporterats vid olika tidpunkter under behandlingsförloppet och kan inträffa från flera veckor till flera år efter behandlingens start med interferon-beta. De första kliniska egenskaperna inkluderar trombocytopeni, nystartad hypertoni, feber, symtom som påverkar centrala nervsystemet (t.ex. förvirring, pares) och nedsatt njurfunktion. Laboratoriefynd som tyder på förekomst av TMA inkluderar minskat antal trombocyter, ökat serumlaktatdehydrogenas (LDH) på grund av hemolys och närvaro av schistocyter (erytrocytfragmentering) vid blodprov. Följaktligen, om kliniska egenskaper hos TMA observeras, rekommenderas ytterligare testning av blodplättsnivåer, LDH i serum, blodprov och njurfunktion. Snabb behandling (med tanke på plasmautbyte) och omedelbar utsättning av Avonex rekommenderas.
Nefrotiskt syndrom - Fall av nefrotiskt syndrom med flera underliggande nefropatier har rapporterats under behandling med interferon -betaprodukter, inklusive kollapsande fokalsegmentell glomeruloskleros (FSGS), minimal förändringssjukdom, MCD), membranproliferativ glomerulonefrit (membranoproliferativ glomerulonefrit MPGN) och membranös glomerulopati MGN). Händelserna har rapporterats vid olika tidpunkter under behandlingens gång och kan inträffa efter flera års behandling med interferon beta. Periodisk övervakning av tidiga tecken eller symtom, såsom ödem, proteinuri och nedsatt njurfunktion, rekommenderas, särskilt hos patienter med ökad risk för njursjukdom. Nefrotiskt syndrom bör behandlas omedelbart och övervägande av avbrytande av AVONEX.
Efter marknadsföring av leverskada, inklusive förhöjda leverenzymer i serum, hepatit, autoimmun hepatit och leversvikt i samband med användning av interferon beta har rapporterats (se avsnitt 4.8). I vissa fall har sådana reaktioner inträffat. andra läkemedel som har associerats med leverskada Potentialen för ytterligare effekter av administrering av flera läkemedel eller andra hepatotoxiska medel (t.ex. alkohol) har inte fastställts. Patienter bör övervakas för tecken på leverskada och försiktighet bör iakttas när att använda interferoner samtidigt med andra läkemedel i samband med leverskada.
Patienter med hjärtsjukdomar som angina, kongestiv hjärtsvikt eller arytmi bör övervakas noggrant för att försämra sitt medicinska tillstånd under behandling med AVONEX. Influensaliknande symptom i samband med AVONEX-terapi kan vara stressande för patienter. Patienter med tillhörande hjärtfunktionsfunktioner.
Avvikelser i laboratoriedata kan inträffa vid användning av interferoner.Därför rekommenderas det, utöver de laboratorietester som normalt krävs för övervakning av MS -patienter, att utföra fullständiga och differentiella leukocyträkningar, trombocytantal under AVONEX -behandling. Och blodprov inklusive leverfunktion tester Patienter med myelosuppression kan kräva mer intensiv övervakning av blodvärden, med differential- och trombocytantal.
Patienter kan utveckla antikroppar mot AVONEX. Antikroppar från några av dessa patienter minskar aktiviteten av interferon beta-1a in vitro (neutraliserande antikroppar). Neutraliserande antikroppar är associerade med en minskning in vivo av de biologiska effekterna av AVONEX och potentiellt kan vara associerade med en minskning av klinisk effekt.Det uppskattas att förekomsten av neutraliserande antikroppsbildning uppnås efter 12 månaders behandling.Nya kliniska studier utförda på patienter som behandlats i upp till tre år med AVONEX föreslår att cirka 5% till 8% av dem utvecklar neutraliserande antikroppar.
Användningen av olika metoder för att bestämma serumantikroppar mot interferon begränsar möjligheten att jämföra antigenicitet mellan olika produkter.
04.5 Interaktioner med andra läkemedel och andra former av interaktion
Inga formella interaktionsstudier har utförts på människor.
Interaktionen mellan AVONEX och kortikosteroider eller med adrenokortikotropt hormon (ACTH) har inte studerats systematiskt.Kliniska studier tyder på att MS -patienter kan få AVONEX och kortikosteroider eller ACTH under återfall.
Interferoner har rapporterats minska aktiviteten hos hepatiska cytokrom P450-beroende enzymer hos människor och djur. Effekten av högdosadministrering av AVONEX på P450-beroende metabolism hos apor har utvärderats och inga förändringar i levermetaboliseringsförmågan har observerats. Försiktighet bör iakttas när AVONEX administreras i kombination med läkemedel som har ett smalt terapeutiskt index. Och vars "clearance" är till stor del beroende av det hepatiska cytokrom P450 -systemet, till exempel vissa klasser av antiepileptika och antidepressiva medel.
04.6 Graviditet och amning
Graviditet
Det finns begränsade data om användning av AVONEX under graviditet Tillgängliga data indikerar en möjlig ökad risk för spontan abort Inledande av behandling är kontraindicerad under graviditet (se avsnitt 4.3).
Kvinnor i fertil ålder måste använda lämpliga preventivmetoder. Patienter som blir gravida och de som planerar att bli gravida under behandling med AVONEX bör informeras om de potentiella riskerna och avbrytande av AVONEX -behandling bör övervägas (se avsnitt 5.3). Hos patienter med hög förekomst av återfall före behandlingens början bör risken för ett allvarligt återfall efter avbrott av AVONEX på grund av graviditet vägas mot en eventuell ökad risk för spontan abort.
Matdags
Det är inte känt om AVONEX utsöndras i bröstmjölk. På grund av risken för allvarliga biverkningar hos spädbarn som ammas måste beslut fattas om amning eller AVONEX -behandling ska avbrytas.
Fertilitet
Fertilitets- och utvecklingsstudier har utförts på rhesusapor med en besläktad form av interferon beta-1a. Anovulatoriska och abortiva effekter observerades hos studiedjur vid mycket höga doser (se avsnitt 5.3).
Det finns ingen information om effekterna av interferon beta-1a på manlig fertilitet.
04.7 Effekter på förmågan att framföra fordon och använda maskiner
Inga studier av AVONEX effekter på förmågan att framföra fordon och använda maskiner har utförts Rapporterade biverkningar som påverkar centrala nervsystemet kan ha en mindre effekt på förmågan att framföra fordon och använda maskiner hos känsliga patienter (se avsnitt 4.8).
04.8 Biverkningar
Den högsta förekomsten av biverkningar i samband med AVONEX-behandling är relaterad till influensaliknande symptom De vanligaste rapporterade influensaliknande symptomen är: muskelsmärta, feber, frossa, svettningar, asteni, huvudvärk och illamående Titrering av AVONEX vid behandlingens början visat en minskning av svårighetsgraden och förekomsten av influensaliknande symtom Influensaliknande symtom tenderar att vara mer uttalade vid behandlingens början och blir mindre frekventa med fortsatt behandling.
Efter injektion av produkten kan övergående neurologiska symtom uppträda, vilket kan likna en förvärring av MS. Övergående episoder av hypertoni och / eller svår muskelsvaghet som förhindrar frivillig rörelse kan uppstå när som helst under behandlingen. Dessa episoder är av begränsad varaktighet, tidsmässigt relaterade till injektionerna och kan återkomma efter efterföljande injektioner. I vissa fall är dessa symtom associerade med influensaliknande symptom.
Frekvensen av observerade biverkningar uttrycks i patientår enligt följande kategorier:
Mycket vanliga (≥1 / 10 patientår);
Vanliga (≥1 / 100,
Mindre vanliga (≥1 / 1000 till
Sällsynta (≥1 / 10.000,
Mycket sällsynt (
Ingen känd frekvens (kan inte beräknas utifrån tillgängliga data).
Patienttidsindex representerar summan av de enskilda tidsenheter som studiepatienten utsattes för AVONEX innan han upplevde biverkningen. Till exempel kan 100 årsår indikera 100 patienter som behandlats under ett år eller 200 patienter som behandlats i ett halvt år .
Följande tabell listar biverkningar från studier (kliniska och observationsstudier, med en uppföljningsperiod från två till sex år) och andra biverkningar som identifierats genom spontana användarrapporter, med okänd frekvens.
Inom varje frekvensklass rapporteras biverkningar i fallande svårighetsgrad.
* Klasseffekt för interferon-beta-produkter (se avsnitt 4.4)
+ Klasseffekt för interferoninnehållande läkemedel, se nedan Pulmonell arteriell hypertoni.
1 Reaktioner på injektionsstället har rapporterats, inklusive smärta, inflammation och mycket sällsynta fall av abscess eller cellulit som kan kräva operation.
2 Manifestationsfrekvensen är högre i början av behandlingen.
3 En synkopeepisod kan inträffa efter en AVONEX -injektion, men detta är vanligtvis en isolerad episod som vanligtvis inträffar i början av behandlingen och inte upprepas med efterföljande injektioner.
Pulmonell arteriell hypertoni
Fall av pulmonell arteriell hypertoni (PAH) har rapporterats för läkemedel som innehåller interferon beta. Händelserna rapporterades vid olika tidpunkter, inklusive flera år efter behandlingen påbörjades med beta -interferon.
Pediatrisk population
De få publicerade data tyder på att säkerhetsprofilen för ungdomar i åldern 12-16 år som får AVONEX 30 mikrogram intramuskulärt (IM) en gång i veckan liknar den som ses hos vuxna.
Rapportering av misstänkta biverkningar
Det är viktigt att rapportera misstänkta biverkningar som inträffar efter godkännande av läkemedlet, eftersom det möjliggör kontinuerlig övervakning av nytta / riskförhållandet för läkemedlet.Hälso- och sjukvårdspersonal uppmanas att rapportera alla misstänkta biverkningar via den italienska läkemedelsmyndigheten. . Webbplats: www.agenziafarmaco.gov.it/it/responsabili.
04.9 Överdosering
Inga fall av överdos har rapporterats. Vid en överdos bör patienten dock läggas in på sjukhus för observation och få lämplig stödjande behandling.
05.0 FARMAKOLOGISKA EGENSKAPER
05.1 Farmakodynamiska egenskaper
Farmakoterapeutisk grupp: interferoner.
ATC -kod: L03 AB07.
Interferoner är en familj av naturliga proteiner som produceras av eukaryota celler som svar på virusinfektion och andra biologiska inducerare. Interferoner är cytokiner som förmedlar antivirala, antiproliferativa och immunmodulerande aktiviteter. Tre huvudformer av interferon har särskiljats: alfa, beta och gamma Interferoner alfa och beta klassificeras som typ I interferoner och interferon gamma som typ II interferon. Dessa interferoner har överlappande men klart urskiljbara biologiska aktiviteter. De kan också skilja sig åt med avseende på det cellulära syntesstället.
Interferon beta produceras av olika celltyper inklusive fibroblaster och makrofager.Naturligt interferon beta och AVONEX (interferon beta-1a) glykosyleras och har en enda komplex kolhydratmolekyl bunden till kväve.För andra proteiner är det känt att glykosylering påverkar blodstabilitet, aktivitet, biologisk fördelning och halveringstid, men effekterna av interferon beta som är beroende av glykosylering är inte helt definierade.
Handlingsmekanism
AVONEX utövar sina biologiska effekter genom att binda till specifika receptorer på ytan av mänskliga celler. Denna länk initierar en komplex kaskad av intracellulära händelser som leder till uttryck av många interferoninducerade genprodukter och markörer. Dessa inkluderar klass I MHC, Mx -protein, 2 "/ 5" - oligoadenylatsyntas, β2 -mikroglobulin och neopterin. Några av dessa produkter har mätts i serum och cellfraktioner av blod som samlats in från patienter som behandlats med AVONEX. Efter en enda intramuskulär dos av AVONEX förblir serumnivåerna av dessa produkter förhöjda i minst fyra dagar och upp till en vecka.
Det är inte känt om verkningsmekanismen för AVONEX vid multipel skleros följer samma sekvens av biologiska händelser som beskrivits ovan, eftersom patofysiologin för multipel skleros inte är väl etablerad.
Klinisk effekt och säkerhet
Effekterna av MS-behandling med frystorkat AVONEX påvisades i en enda placebokontrollerad studie på 301 patienter (AVONEX n = 158, placebo n = 143) med återfallande MS som kännetecknades av minst 2 exacerbationer under de tre senaste åren eller minst en exacerbation vid "året före inträdet i studien, då sjukdomstiden var mindre än 3 år. Patienter med EDSS vid ingång 1 till 3,5 ingick i studien. På grund av studiens utformning följdes patienterna under olika tidsperioder. 150 AVONEX-behandlade patienter avslutade ett studieår och 85 avslutade två års studier. I studien var den kumulativa andelen patienter som utvecklade funktionsnedsättningsprogression (överlevnadsanalys enligt Kaplan-Meier-metoden) vid slutet av de två åren 35% för patienter som behandlats med placebo och 22% för patienter som behandlats med AVONEX. Handikappprogression mättes som en 1,0 -punkts ökning av den utökade skalan för funktionshinder (EDSS), som varade minst sex månader. En tredjedel minskning av den årliga återfallshastigheten har också visats. Denna sista kliniska effekt observerades efter mer än ett års behandling.
En dubbelblind, randomiserad, dosjämförande studie av 802 patienter med återfallande MS (AVONEX 30 mcg n = 402, AVONEX 60 mcg n = 400) visade ingen statistiskt signifikant skillnad eller trend mellan 30 mcg och 60 mcg AVONEX för kliniska och allmänna parametrar för kärnmagnetisk resonans (MR).
Effekterna av AVONEX vid behandling av MS visades också i en randomiserad, dubbelblind studie med 383 patienter (AVONEX n = 193, placebo n = 190) med en enda demyeliniserande händelse associerad med minst två kompatibla hjärnskador som upptäcktes vid RMN . En minskning av risken för att uppleva en andra händelse observerades i AVONEX -behandlingsgruppen. En effekt på MR -parametrar hittades också. Den uppskattade risken för en andra händelse var 50% under tre år och 39% under två år i placebogruppen, och 35% (tre år) och 21% (två år) i den som behandlades med AVONEX. I en post-hoc-analys var risken för en andra händelse inom två år 56% i placebogruppen och 21% i behandlingsgruppen hos patienter som hade minst en gadoliniumförstärkande lesion och nio T2-lesioner vid baslinje-MR. Effekten av tidig AVONEX-behandling är emellertid inte känd även i denna högriskundergrupp, eftersom studien huvudsakligen utformades för att bedöma tidsintervallet mellan första och andra händelser, snarare än evolution. långsiktig sjukdom. Dessutom finns det för närvarande ingen väletablerad definition av högriskpatienter, även om ett mer konservativt tillvägagångssätt är att "acceptera minst nio hyperintensiva T2-lesioner vid den första skanningen och minst en ny T2-lesion eller en ny gadoliniumförstärkande lesion på en efterföljande skanning utförd minst tre månader efter den första Under alla omständigheter ska behandling endast övervägas för patienter som klassas som högrisk.
Pediatrisk population
De få data om effekt / säkerhet av AVONEX som erhållits genom administrering av 15 mikrogram intramuskulärt (IM) en gång i veckan (n = 8) jämfört med en obehandlad grupp (n = 8), med 4-års uppföljning, har resultaten överensstämmande med de som ses hos vuxna, dock ökade poängen Expanded Disability Status Scale (EDSS) i den behandlade gruppen under den 4-åriga uppföljningen, vilket indikerar sjukdomsprogression.Det finns ingen direkt jämförelse med den för närvarande rekommenderade dosen hos vuxna.
05.2 "Farmakokinetiska egenskaper
Den farmakokinetiska profilen för AVONEX bedömdes indirekt med en metod som mäter interferons antivirala aktivitet. Denna analysmetod är begränsad genom att den är känslig för interferon men saknar specificitet för interferon beta. Alternativa analystekniker är inte tillräckligt känsliga.
Efter intramuskulär administrering av AVONEX når serumantivirala aktivitetsnivåer mellan 5 och 15 timmar efter behandlingen och minskar med en halveringstid på cirka 10 timmar. Med en lämplig korrigering för absorptionshastigheten från injektionsstället är den beräknade biotillgängligheten cirka 40%. Den beräknade biotillgängligheten är större utan sådana korrigeringar. Intramuskulär administrering kan inte ersätta subkutan administrering.
05.3 Prekliniska säkerhetsdata
Cancerframkallande: Inga cancerframkallande data finns tillgängliga för interferon beta-1a hos djur och människor.
Kronisk toxicitet: I en 26-veckors upprepad toxicitetsstudie på rhesusapor, administreras intramuskulärt en gång i veckan, i kombination med ett annat immunmodulerande medel, en monoklonal antikropp mot CD40-ligand, inget immunsvar eller några tecken på toxicitet mot interferon beta-1a.
Lokal tolerabilitet: Intramuskulär irritation har inte utvärderats hos djur efter upprepad administrering på samma injektionsställe.
Mutagenicitet: Begränsade men relevanta mutagenicitetsstudier har genomförts. Resultaten var negativa.
Nedsatt fertilitet: Fertilitets- och utvecklingsstudier på rhesusapor har genomförts med en relaterad form av interferon beta-1a. Vid mycket höga doser observerades anovulatoriska och abortiva effekter hos studiedjuren. Liknande dosrelaterade effekter på reproduktiv aktivitet har också observerats med andra former av alfa- och beta-interferoner.Inga teratogena eller fosterutvecklingseffekter har observerats, men tillgänglig information om effekterna av interferon beta-1a under peri- och postnatala perioder är begränsad.
Det finns ingen information om effekterna av interferon beta-1a på manlig fertilitet.
06.0 LÄKEMEDELSINFORMATION
06.1 Hjälpämnen
Natriumacetattrihydrat
Isättika
Argininhydroklorid
Polysorbat 20
Vatten för injektionsvätskor
06.2 Oförenlighet
Inte relevant.
06.3 Giltighetstid
3 år.
06.4 Särskilda förvaringsanvisningar
Förvaras i kylskåp (2 ° C - 8 ° C)
FRYS INTE.
AVONEX kan förvaras i rumstemperatur (mellan 15 ° C och 30 ° C) i upp till en vecka.
Förvara i originalförpackningen (förseglad plastbricka) för att skydda mot ljus (se avsnitt 6.5).
06.5 Förpackningens innehåll och förpackningens innehåll
1 ml förfylld glasspruta (typ I) med en sabotagbar lock och kolvpropp (brombutylgummi) innehållande 0,5 ml lösning.
Förpackningsstorlek: kartong innehållande fyra eller tolv 0,5 ml förfyllda sprutor. Varje spruta är förpackad i en försluten plastbricka som också innehåller en injektionsnål för intramuskulär användning.
Alla förpackningsstorlekar kanske inte marknadsförs.
06.6 Anvisningar för användning och hantering
AVONEX levereras som en färdig att använda injektionsvätska i en förfylld spruta.
När AVONEX har tagits ur kylskåpet ska den i förfylld spruta värmas till rumstemperatur (15 ° C - 30 ° 7C) i cirka 30 minuter.
Använd inte externa värmekällor som varmt vatten för att värma AVONEX 30 mikrogram injektionsvätska, lösning.
Om injektionslösningen innehåller partiklar eller inte är klar och färglös, ska den förfyllda sprutan inte användas. Injektionsnålen tillhandahålls för intramuskulär injektion. Formuleringen innehåller inte konserveringsmedel. Varje AVONEX förfylld spruta innehåller endast en engångsdos. Kassera den oanvända delen av varje förfylld spruta.
Oanvänd medicin och avfall från detta läkemedel måste kasseras i enlighet med lokala föreskrifter.
07.0 INNEHAVARE AV GODKÄNNANDE FÖR FÖRSÄLJNING
BIOGEN IDEC LIMITED Innovation House 70 Norden Road Maidenhead Berkshire SL6 4AY
Storbritannien
08.0 NUMMER FÖR FÖRSÄLJNINGSTILLSTÅND
A.I.C. 033283033
09.0 DATUM FÖR FÖRSTA GODKÄNNANDE ELLER FÖRNYELSE AV GODKÄNNANDET
Datum för det första godkännandet: 13 mars 1997
Datum för senaste förnyelse: 13 mars 2007
10.0 DATUM FÖR ÖVERSYN AV TEXTEN
10/2015