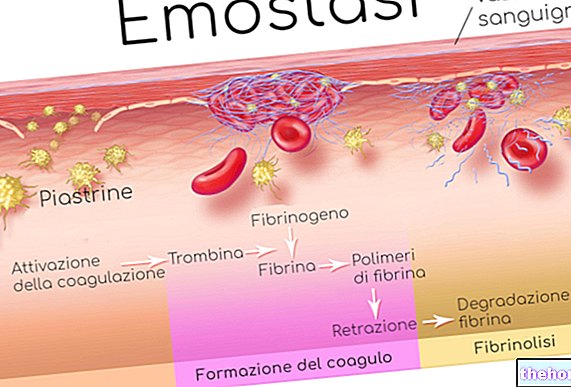
Aktiva ingredienser: Humant papillomvirus 9-valent vaccin (rekombinant, adsorberat)
Gardasil 9 injektionsvätska, suspension i förfylld spruta
Varför används Gardasil 9? Vad är det för?
Gardasil 9 är ett vaccin indikerat för barn och ungdomar från 9 år och för vuxna. Vaccination med Gardasil 9 är indicerat för skydd mot sjukdomar orsakade av humant papillomvirus (HPV) typ 6, 11, 16, 18, 31, 33, 45, 52 och 58.
Dessa tillstånd inkluderar pre-cancerösa och cancerösa lesioner av kvinnliga könsorgan (livmoderhals, vulva och vagina), pre-cancerösa och cancerösa lesioner i anus och könsvårtor hos män och kvinnor.
Gardasil 9 har studerats hos män och kvinnor mellan 9 och 26 år.
Gardasil 9 skyddar mot de typer av HPV som är ansvariga för de flesta fall av dessa sjukdomar.
Gardasil 9 är indicerat för att förebygga dessa sjukdomar. Vaccinet används inte för att behandla HPV-relaterade sjukdomar. Gardasil 9 har ingen effekt hos personer som redan har en ihållande infektion eller sjukdom associerad med en av HPV-typerna i vaccinet. Hos individer som redan har infekterats med en eller flera typer av HPV i vaccinet kan Gardasil 9 dock fortfarande skydda mot sjukdomar som är associerade med de andra HPV -typerna som finns i vaccinet.
Gardasil 9 kan inte orsaka HPV -relaterade sjukdomar.
När en person vaccineras med Gardasil 9 stimulerar immunsystemet (kroppens naturliga försvarssystem) produktion av antikroppar mot de 9 typerna av HPV i vaccinet, som hjälper till att skydda mot sjukdomar som orsakas av dessa virus.
Om du eller ditt barn får en första dos Gardasil 9 måste vaccinationskursen med Gardasil 9 genomföras.
Om du eller ditt barn redan har fått ett HPV -vaccin, fråga din läkare om Gardasil 9 passar dig.
Gardasil 9 måste användas i enlighet med officiella riktlinjer.
Kontraindikationer När Gardasil inte ska användas 9
Du ska inte få Gardasil 9 om du eller barnet:
- om du är allergisk mot en av de aktiva substanserna eller mot någon av de andra ingredienserna i detta vaccin (anges som "andra ingredienser" i avsnitt 6);
- du har utvecklat en allergisk reaktion efter att ha fått en dos Gardasil eller Silgard (HPV typ 6,11,16 och 18) eller Gardasil 9.
Försiktighetsåtgärder vid användning Vad du behöver veta innan du tar Gardasil 9
Tala med din läkare eller sjuksköterska om du eller ditt barn:
- du har en blödningsstörning (en sjukdom som innebär mer än normal blödning), såsom hemofili
- du har ett försvagat immunsystem, till exempel på grund av en genetisk defekt, HIV -infektion eller läkemedel som påverkar immunsystemet;
- du har en sjukdom med hög feber. En mild feber eller en ”övre luftvägsinfektion (till exempel förkylning) utgör dock inte i sig en anledning att skjuta upp vaccinationen.
Svimning, ibland åtföljt av fall, kan förekomma (särskilt hos ungdomar) efter nålinjektion. Tala därför om för din läkare eller sjuksköterska om du svimmat av en tidigare injektion.
Som med alla vacciner skyddar Gardasil 9 kanske inte alla vaccinerade individer fullt ut.
Gardasil 9 skyddar inte mot någon form av humant papillomvirus. Därför bör man vidta lämpliga försiktighetsåtgärder mot sexuellt överförbara sjukdomar.
Vaccination ersätter inte rutinmässig livmoderhalskontroll. Om du är kvinna måste du fortsätta följa din läkares anvisningar angående livmoderhalsprov / Pap -tester och förebyggande och skyddande åtgärder.
Vilken annan viktig information behöver du eller barnet veta om Gardasil 9
Varaktigheten av det skydd som ges är för närvarande inte känt. Långsiktiga studier pågår för att avgöra om en boosterdos behövs.
Interaktioner Vilka läkemedel eller livsmedel kan ändra effekten av Gardasil 9
Tala om för din läkare eller apotekspersonal om du eller barnet tar, nyligen har tagit eller kan tänkas ta andra läkemedel, inklusive receptfria läkemedel.
Gardasil 9 kan ges tillsammans med ett kombinerat boostervaccin som innehåller difteri (d) och stelkramp (T) tillsammans med kikhosta [acellulär komponent] (ap) och / eller [inaktiverad] poliomyelit (IPV) (dTap-vaccin, dT-IPV, dTap -IPV), på separata injektionsställen (i en annan del av kroppen, till exempel den andra armen eller benet) under samma vaccinationspass.
Gardasil 9 kanske inte har en optimal effekt när den används tillsammans med läkemedel som undertrycker immunsystemet.
Hormonella preventivmedel (t.ex. p -piller) minskar inte det skydd som Gardasil 9 ger.
Varningar Det är viktigt att veta att:
Graviditet och amning
Om du är gravid, tror att du kan vara gravid eller planerar att skaffa barn, eller om du ammar, rådfråga din läkare innan du får detta vaccin.
Gardasil 9 kan ges till kvinnor som ammar eller planerar att amma.
Köra och använda maskiner
Gardasil 9 kan lätt och tillfälligt påverka förmågan att framföra fordon eller använda maskiner (se avsnitt 4 "Möjliga biverkningar").
Gardasil 9 innehåller natriumklorid
Detta läkemedel innehåller mindre än 1 mmol natrium (23 mg) per dos, dvs i huvudsak "natriumfritt".
Dos, metod och administreringstid Hur man använder Gardasil 9: Dosering
Gardasil 9 ges genom injektion av din läkare. Du eller barnet får tre doser av vaccinet.
Första injektionen: på fastställt datum.
Andra injektionen: helst 2 månader efter den första injektionen.
Tredje injektionen: helst 6 månader efter den första injektionen.
Om ett annat vaccinationsschema krävs ska den andra dosen ges minst en månad efter den första dosen och den tredje dosen ges minst 3 månader efter den andra dosen. Alla tre doser ska administreras inom 1 år. Be din läkare om mer information om detta.
Försökspersoner som tar emot vaccinet måste genomföra vaccinationskursen i tre doser; annars kan personen som får vaccinet inte vara helt skyddad.
Gardasil 9 ges genom injektion genom huden i muskeln (helst armen eller lårmuskeln).
Överdosering Vad du ska göra om du har tagit för mycket Gardasil 9
Om en dos Gardasil 9 inte ges:
Om du missar en av de schemalagda injektionerna, kommer din läkare att bestämma när du ska ge dig den saknade dosen. Det är viktigt att du följer instruktionerna från din läkare eller sjuksköterska angående efterföljande vaccinationspass för att administrera de återstående doserna. Om du glömmer att gå till läkaren vid angiven tid eller inte kan gå, rådfråga din läkare. 9 som den första dosen, ska de nästa två doserna för att slutföra vaccinationskursen med 3 doser vara Gardasil 9 och inte ett annat HPV-vaccin.
Om du har ytterligare frågor om användningen av detta vaccin, fråga din läkare eller apotekspersonal.
Biverkningar Vilka är biverkningarna av Gardasil 9
Liksom alla vacciner kan detta vaccin orsaka biverkningar, men inte alla får dem.
Följande biverkningar kan observeras efter användning av Gardasil 9:
Mycket vanliga (kan förekomma hos fler än 1 av 10 personer): biverkningar som ses på injektionsstället (smärta, svullnad, rodnad) och huvudvärk.
Vanliga (kan förekomma hos upp till 1 av 10 personer): biverkningar som ses på injektionsstället (blåmärken och klåda), feber, trötthet, yrsel och illamående.
När Gardasil 9 gavs med kombinerad difteri, stelkramp, kikhosta [acellulär komponent] och poliomyelit [inaktiverat] boostervaccin under samma vaccinationspass rapporterades mer svullnad vid injektionsstället.
Följande biverkningar har rapporterats efter att ha fått GARDASIL eller SILGARD och kan också inträffa efter administrering av Gardasil 9:
Svimning, ibland tillsammans med skakningar eller stelningar, har rapporterats. Även om svimningsepisoder inte är vanliga bör vaccinerade individer observeras i 15 minuter efter administrering av HPV -vaccinet.
Allergiska reaktioner har rapporterats. Några av dessa reaktioner har varit allvarliga. Symtomen kan vara andningssvårigheter, andningssvårigheter, väsande andning, nässelutslag och / eller utslag.
Som med andra vacciner har biverkningar rapporterats vid utbredd användning av vaccinet som inkluderar: förstorade lymfkörtlar (nacke, armhålor, ljumske); (muskelsvaghet, onormala känslor, stickningar i armar, ben och övre delen av kroppen, eller förvirring (Guillain-Barrè syndrom, akut disseminerad encefalomyelit); kräkningar, ledvärk, muskelsmärta, ovanlig trötthet och svaghet, frossa, allmän känsla av obehag, blödning eller blåmärken lättare än normalt och infektion i huden på injektionsstället .
Rapportering av biverkningar
Tala med din läkare eller apotekspersonal om du eller barnet får några biverkningar. Detta inkluderar eventuella biverkningar som inte nämns i denna bipacksedel. Du kan också rapportera biverkningar direkt via det nationella rapporteringssystemet som anges i bilaga V. Genom att rapportera biverkningar kan du hjälpa till att ge mer information om säkerheten för detta läkemedel.
Giltighetstid och lagring
Förvara vaccinet utom syn- och räckhåll för barn.
Använd inte detta vaccin efter utgångsdatum som anges på sprutans etikett och ytterkartong efter EXP. Utgångsdatumet avser den sista dagen i den månaden.
Förvaras i kylskåp (2 ° C - 8 ° C). Frys inte. Förvara sprutan i ytterhöljet för att skydda den mot ljus.
Kasta inga läkemedel i avloppsvatten eller hushållsavfall. Fråga din apotekare om hur du ska kasta läkemedel som du inte längre använder. Detta hjälper till att skydda miljön.
Sammansättning och läkemedelsform
Vad Gardasil innehåller 9
De aktiva ingredienserna är: högrenade icke-infektiösa proteiner för varje typ av humant papillomvirus (6, 11, 16, 18, 31, 33, 45, 52 och 58).
1 dos (0,5 ml) innehåller ungefär:
Humant papillomvirus1 typ 6 L1 -protein 30 mikrogram
Humant papillomvirus1 typ 11 L1 -protein 40 mikrogram
Humant papillomvirus1 typ 16 L1 -protein 60 mikrogram
Humant papillomvirus1 typ 18 L1 -protein 40 mikrogram
Humant papillomvirus1 typ 31 L1 -protein 20 mikrogram
Humant papillomvirus1 typ 33 L1 -protein 20 mikrogram
Humant papillomvirus1 typ 45 L1 -protein 20 mikrogram
Humant papillomvirus1 typ 52 L1 -protein 20 mikrogram
Humant papillomvirus1 typ 58 L1 -protein 20 mikrogram
1 Humant papillomvirus = HPV.
2 L1-protein i form av virusliknande partiklar som produceras av jästceller (Saccharomyces cerevisiae CANADE 3C-5 (stam 1895)) med rekombinant DNA-teknik.
3 adsorberades på amorft aluminiumhydroxifosfatsulfatsadjuvans (0,5 milligram Al).
Amorft aluminiumhydroxifosfatsulfat finns i detta vaccin som adjuvans, adjuvanser används för att förbättra vaccins immunsvar.
Övriga innehållsämnen i vaccinsuspensionen är: natriumklorid, L-histidin, polysorbat 80, natriumborat och vatten för injektionsvätskor.
Hur Gardasil 9 ser ut och förpackningens innehåll
1 dos Gardasil 9 injektionsvätska, suspension innehåller 0,5 ml.
Före skakning framstår Gardasil 9 som en klar vätska med en vit fällning. Efter noggrann omrörning framstår den som en opaliserande vit vätska.
Gardasil 9 finns i förpackningar om 1 eller 10 förfyllda sprutor.
Alla förpackningsstorlekar kanske inte marknadsförs.
Bipacksedel: AIFA (Italian Medicines Agency). Innehåll publicerat i januari 2016. Den information som finns finns kanske inte uppdaterad.
För att få tillgång till den senaste versionen är det lämpligt att gå till AIFA (Italian Medicines Agency) webbplats. Ansvarsfriskrivning och användbar information.
01.0 LÄKEMEDLETS NAMN
GARDASIL 9 SUSPENSION FÖR INJEKTION I FÖRFYLLAD SPRUTA
▼ Läkemedlet är föremål för ytterligare övervakning. Detta gör det möjligt att snabbt identifiera ny säkerhetsinformation. Vårdpersonal uppmanas att rapportera alla misstänkta biverkningar. Se avsnitt 4.8 för information om hur du rapporterar biverkningar.
02.0 KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING
1 dos (0,5 ml) innehåller ungefär:
Humant papillomvirus1 typ 6 L1 -protein 30 mcg
Humant papillomvirus1 typ 11 L1 -protein 40 mcg
Humant papillomvirus1 typ 16 L1 -protein 60 mcg
Humant papillomvirus1 typ 18 L1 -protein 40 mcg.
Humant papillomvirus1 typ 31 L1 -protein 20 mcg
Humant papillomvirus1 typ 33 L1 -protein 20 mcg
Humant papillomvirus1 typ 45 L1 -protein 20 mcg
Humant papillomvirus1 typ 52 L1 -protein 20 mcg.
Humant papillomvirus1 typ 58 L1 -protein 20 mcg.
1 Humant papillomvirus = HPV.
2 L1-protein i form av virusliknande partiklar som produceras av jästceller (Saccharomyces cerevisiae CANADE 3C-5 (Strain 1895)) med rekombinant DNA-teknik.
& isup3; Adsorberat på amorft aluminiumhydroxifosfatsulfatsadjuvans (0,5 milligram Al).
För fullständig förteckning över hjälpämnen, se avsnitt 6.1.
03.0 LÄKEMEDELSFORM
Injektionsvätska, suspension i förfylld spruta.
Klar vätska med vit fällning.
04.0 KLINISK INFORMATION
04.1 Terapeutiska indikationer
Gardasil 9 är indicerat för aktiv immunisering av individer från 9 års ålder mot följande HPV -sjukdomar:
• Precancerösa lesioner och tumörer som påverkar livmoderhalsen, vulva, slidan och anus orsakade av HPV -subtyperna i vaccinet.
• Könsvårtor (Condyloma acuminata) orsakas av specifika typer av HPV.
Se avsnitt 4.4 och 5.1 för viktig information om data som stöder dessa terapeutiska indikationer.
Användningen av Gardasil 9 måste fastställas i enlighet med officiella rekommendationer.
04.2 Dosering och administreringssätt
Dosering
Primärvaccinationskursen består av separat administrering av 3 doser om 0,5 ml, enligt följande schema: 0, 2, 6 månader.
Om ett annat vaccinationsschema krävs ska den andra dosen ges minst en månad efter den första dosen och den tredje dosen ges minst 3 månader efter den andra dosen. Alla tre doser ska administreras inom 1 år.
Behovet av en boosterdos har inte fastställts.
Det rekommenderas att försökspersoner som får en första dos Gardasil 9 slutför vaccinationskursen med 3 doser med Gardasil 9 (se avsnitt 4.4).
För Gardasil 9 har inga studier utförts med blandade (utbytbara) regimer av HPV -vacciner.
Försökspersoner som tidigare vaccinerats med en 3-dosers behandling av kvadrivalent HPV-typ 6, 11, 16 och 18 (Gardasil eller Silgard) -vaccin, nedan kallat qHPV-vaccin, kan få 3 doser Gardasil 9 (se avsnitt 5.1).
Pediatrisk population (barn under 9 år)
Säkerhet och effekt för Gardasil 9 hos barn under 9 år har inte fastställts Det finns inga tillgängliga data (se avsnitt 5.1).
Kvinnlig befolkning 27 år eller äldre
Säkerhet och effekt för Gardasil 9 hos kvinnor i åldern 27 år och äldre har inte studerats (se avsnitt 5.1).
Administreringssätt
Vaccinet ska administreras genom intramuskulär injektion. Den föredragna platsen är deltoidregionen i överarmen eller det överlägsna anterolaterala området i låret.
Gardasil 9 får inte injiceras intravaskulärt, subkutant eller intradermalt. Vaccinet ska inte blandas i samma spruta med andra vacciner eller lösning.
För instruktioner om hur du hanterar vaccinet före användning, se avsnitt 6.6.
04.3 Kontraindikationer
Överkänslighet mot de aktiva substanserna eller mot något hjälpämne som anges i avsnitt 6.1.
Patienter med överkänslighet efter en tidigare administrering av Gardasil 9 eller Gardasil / Silgard ska inte få ytterligare doser Gardasil 9.
04.4 Särskilda varningar och lämpliga försiktighetsåtgärder vid användning
Beslutet att vaccinera en patient måste ta hänsyn till risken för tidigare HPV -exponering och den potentiella fördelen med vaccination.
Som med alla injicerbara vacciner bör adekvat medicinsk behandling och övervakning alltid vara lättillgänglig vid sällsynta anafylaktiska reaktioner efter administrering av vaccinet.
Synkope (svimning) kan förekomma, ibland i samband med fallande, efter eller till och med före vaccination, särskilt hos ungdomar, som ett psykogent svar på nålinjektion.Detta fenomen kan åtföljas av olika neurologiska störningar såsom övergående synstörningar, parestesi och tonisk-kloniska rörelser i lemmarna under återhämtningsfasen Därför bör vaccinerade försökspersoner hållas under observation i cirka 15 minuter efter vaccinationen. Det är viktigt att procedurer finns för att undvika skador orsakade av svimning.
Vaccination bör skjutas upp hos personer som lider av akut allvarlig febersjukdom. Men förekomsten av en mindre infektion, såsom en mild övre luftvägsinfektion eller låg feber, är inte en kontraindikation mot immunisering.
Som med alla andra vacciner garanterar vaccination med Gardasil 9 inte alla vaccinerade individer.
Vaccinet skyddar endast mot sjukdomar som orsakas av de HPV -typer som vaccinet omfattar (se avsnitt 5.1). Därför måste lämpliga försiktighetsåtgärder mot sexuellt överförbara sjukdomar fortsätta att följas.
Vaccinet är endast indicerat för profylaktisk användning och har ingen effekt på aktiva HPV -infektioner eller etablerade kliniska patologier. Vaccinet har inte visat sig ha en terapeutisk effekt. Vaccinet är därför inte indicerat för behandling av livmoderhalscancer, högkvalitativa dysplastiska lesioner i livmoderhalsen, vulva och vagina eller könsvårtor. Vaccinet är inte heller indicerat för att förhindra progression av andra befintliga skador relaterade till humant papillomvirus (HPV).
Gardasil 9 förhindrar inte skada på grund av en av HPV -typerna i vaccinet hos individer som är infekterade med samma HPV -typ vid vaccinationstillfället (se avsnitt 5.1).
Vaccination ersätter inte traditionell cervikal screening. Eftersom inget vaccin är 100% effektivt och Gardasil 9 inte skyddar mot någon typ av HPV, eller mot HPV -infektioner som förekommer vid vaccinationstillfället, behåller traditionell hals screening "livmodern kritisk betydelse och bör utföras i enlighet med lokala rekommendationer.
Det finns inga data om användning av Gardasil 9. För personer med nedsatt immunsvar. Säkerheten och immunogeniciteten för qHPV -vaccinet har utvärderats hos personer i åldern 7 till 12 år med känd HIV -infektion (Human Immunodeficiency Virus (HIV).) (Se avsnitt 5.1).
Personer med nedsatt immunsvar på grund av användning av stark immunsuppressiv terapi, en genetisk defekt, HIV -infektion (Human Immunodeficiency Virus) eller andra orsaker kanske inte svarar på vaccinet.
Detta vaccin ska administreras med försiktighet till personer med trombocytopeni eller någon annan koagulationsstörning eftersom blödning kan uppstå hos dessa individer efter intramuskulär administrering.
Långsiktiga uppföljningsstudier pågår för närvarande för att fastställa skyddets varaktighet (se avsnitt 5.1).
Det finns inga säkerhets-, immunogenicitets- eller effektdata som stöder utbytbarheten av Gardasil 9 med tvåvärda eller fyrvärda HPV -vacciner.
04.5 Interaktioner med andra läkemedel och andra former av interaktion
Säkerheten och immunogeniciteten hos patienter som fick immunglobulin eller blodhärledda produkter under de tre månaderna före vaccinationen har inte studerats i kliniska studier.
Använd med andra vacciner
Gardasil 9 kan administreras samtidigt med ett kombinerat boostervaccin innehållande difteri (d) och stelkramp (T) tillsammans med kikhosta [acellulär komponent] (ap) och / eller [inaktiverad] lapoliomyelit (IPV) (dTap-vaccin, dT-IPV, dTap -IPV) utan någon signifikant interferens med antikroppssvaret för något av vaccinerna. Dessa data är baserade på resultat som observerats i en klinisk studie där kombinationsvaccinet dTap-IPV administrerades samtidigt med den första dosen Gardasil 9 (se avsnitt 4.8).
Använd med hormonella preventivmedel
I kliniska prövningar använde 60,2% av kvinnorna i åldern 16 till 26 år som fick Gardasil 9 hormonella preventivmedel under vaccinationsperioden. Användningen av hormonella preventivmedel tycktes inte påverka specifika immunsvar mot Gardasil 9.
04.6 Graviditet och amning
Graviditet
Ett stort antal studier av Gardasil 9 hos gravida kvinnor (mer än 1 000 drabbade fall) tyder inte på någon missbildning eller foster- / neonatal toxicitet (se avsnitt 5.1).
Djurstudier tyder inte på reproduktionstoxicitet (se avsnitt 5.3).
Dessa uppgifter anses dock vara otillräckliga för att rekommendera användning av Gardasil 9. Vaccination bör därför skjutas upp till graviditetens slut (se avsnitt 5.1).
Matdags
Gardasil 9 kan användas under amning.
Totalt 92 kvinnor ammade under vaccinationsperioden för de kliniska studierna med Gradasil 9. I studierna var vaccinimmunogenicitet liknande mellan ammande och icke ammande kvinnor. Biverkningsprofilen för kvinnor som ammade var liknande den för kvinnor i den allmänna kliniska prövningspopulationen. Inga allvarliga biverkningar rapporterades hos spädbarn som ammades under vaccinationsperioden.
Fertilitet
Det finns inga data om effekterna av Gardasil 9 på fertilitet hos människor. Djurstudier visar inte skadliga effekter på fertiliteten (se avsnitt 5.3).
04.7 Effekter på förmågan att framföra fordon och använda maskiner
Gardasil 9 har ingen eller försumbar påverkan på förmågan att framföra fordon eller använda maskiner. Några av effekterna som nämns i avsnitt 4.8 "Biverkningar" kan emellertid tillfälligt påverka förmågan att framföra fordon eller använda maskiner.
04.8 Biverkningar
A. Sammanfattning av säkerhetsprofilen
Under sju kliniska prövningar fick försökspersonerna Gardasil 9 på dagen för inskrivningen och cirka 2 och 6 månader därefter. Säkerheten bedömdes genom övervakning med vaccinationskortstöd (VRC - vaccinationskort), under de 14 dagarna efter varje Gardasil -injektion 9. Totalt 15776 försökspersoner (varav 10 495 försökspersoner i åldern 16 till 26 och 5 281 ungdomar i åldern 9 till 15 år, vid tidpunkten för inskrivningen) hade fått Gardasil 9. Få försökspersoner (0,1 %) avbruten dosering på grund av biverkningar.
De vanligaste biverkningarna som observerades med Gardasil 9 var relaterade till injektionsstället (84,8% av vaccinerade inom 5 dagar efter varje vaccinationspass) och huvudvärk (13,2% av vaccinerade inom 15 dagar efter varje vaccinationspass).). Dessa biverkningar var generellt milda eller måttliga i intensitet.
B. Sammanfattningstabell över biverkningar
Kliniska studier
Biverkningar, som ansågs kunna ha samband med vaccination, delades med frekvens.
Frekvenser rapporteras som:
• Mycket vanligt (≥1 / 10)
• Vanliga (≥1 / 100 år
Tabell 1: Biverkningar observerade efter administrering av Gardasil 9, med en frekvens av minst 1,0% i kliniska studier
I en klinisk studie med 1 053 friska ungdomar i åldern 11 till 15 år visade administrering av den första dosen Gardasil 9 samtidigt med boosterdosen av en kombinerad difteri, stelkramp, kikhosta [acellulär komponent] och poliomyelitvaccin [inaktiverat] en ökning av injektionen reaktioner på platsen (svullnad, erytem), huvudvärk och feber. De observerade skillnaderna var
Erfarenhet efter marknadsföring
Följande biverkningar rapporterades spontant under användning av qHPV-vaccinet efter dess godkännande och kan också observeras under erfarenhet efter marknadsföring med Gardasil 9. Säkerhetserfarenhet efter marknadsföring med qHPV-vaccin är korrelerad. Till Gardasil 9, eftersom vacciner innehåller L1 HPV -proteiner av fyra av samma HPV -typer.
Eftersom dessa biverkningar rapporterades frivilligt från en population av odefinierad storlek, är det inte möjligt att på ett tillförlitligt sätt uppskatta deras frekvens eller fastställa ett orsakssamband till vaccinexponering för alla händelser.
Infektioner och angrepp: Cellulit vid injektionsstället
Blod- och lymfsystemet: Idiopatisk trombocytopen purpura, lymfadenopati.
Immunsystemet: Överkänslighetsreaktioner inklusive anafylaktiska / anafylaktoida reaktioner.
Nervsystemet: Akut disseminerad encefalopati, Guillan-Barré syndrom, synkope ibland åtföljt av toniska / kloniska rörelser.
Magtarmkanalen: Kräkningar.
Muskuloskeletala systemet och bindväv: Artralgi, myalgi.
Allmänna symtom och / eller symtom vid administreringsstället: Asteni, frossa, illamående.
Rapportering av misstänkta biverkningar
Rapportering av misstänkta biverkningar som inträffar efter godkännande av läkemedlet är viktigt eftersom det möjliggör kontinuerlig övervakning av nytta / riskbalansen för läkemedlet.Hälso- och sjukvårdspersonal uppmanas att rapportera alla misstänkta biverkningar via det nationella rapporteringssystemet.
04.9 Överdosering
Inga fall av överdos har rapporterats.
05.0 FARMAKOLOGISKA EGENSKAPER
05.1 Farmakodynamiska egenskaper
Farmakoterapeutisk grupp: Vacciner, papillomavirusvacciner, ATC -kod: J07BM03
Handlingsmekanism
Gardasil 9 är ett icke-infektiöst adjuvanserat rekombinant 9-valent vaccin. Den framställs av högrenade virusliknande partiklar (VLP) av det stora kapsidproteinet L1 från de 4 typerna av humant papillomvirus (HPV) (6, 11, 16 och 18), som finns i Gardasil- eller Silgard-qHPV-vaccinet, och från de ytterligare 5 typerna av HPV. Använder samma amorfa aluminiumhydroxifosfatsulfatadjuvans som används för qHPV -vaccinet. VLP kan inte infektera celler, reproducera eller orsaka sjukdom. Effekten av L1 VLP-vacciner antas förmedlas av utvecklingen av ett humoralt liknande immunsvar.
Epidemiologiska studier tyder på att Gardasil 9 skyddar mot olika typer av HPV som är ansvariga för ungefär: 90% av livmoderhalscancer, mer än 95% av adenokarcinom in situ (AIS), 75-85% av hög livmoderhalscancer (CIN 2/3), 85 -90% av HPV-relaterade vulvarcancer, 90-95% av HPV-relaterade högkvalitativa vulva intraepiteliala neoplasmer (VIN 2/3), 80-85% av HPV-relaterade vaginala cancer, 75-85% av HPV-relaterade högkvalitativa vaginala intraepiteliala neoplasmer (VaIN 2/3), 90-95% av HPV-relaterade analcancer, 85-90% av HPV-relaterade högkvalitativa anal-intraepiteliala neoplasmer (AIN 2/3) och 90% av könsvårtor.
Indikationen för Gardasil 9 är baserad på:
• den icke-underlägsna immunogeniciteten mellan Gardasil 9 och qHPV-vaccinet för HPV-typ 6, 11, 16 och 18 hos flickor och kvinnor i åldern 9 till 26 år; följaktligen kan man dra slutsatsen att effekten av Gardasil 9 mot ihållande infektion och sjukdomar relaterad till HPV -typ 6, 11, 16 eller 18, är den jämförbar med qHPV -vaccinet.
• demonstration av effekt mot ihållande infektion och sjukdomar relaterade till HPV typ 31, 33, 45, 52 och 58 hos flickor och kvinnor i åldern 16 till 26 år, och
• demonstration av inte mindre immunogenicitet mot de nio typerna av HPV som finns i Gardasil 9, hos pojkar och flickor mellan 9 och 15 år och män mellan 16 och 26 år, jämfört med flickor och kvinnor mellan 16 och 26 år år.
Kliniska studier för qHPV -vaccinet
Effekt hos kvinnor och män i åldern 16 till 26 år
Effekten utvärderades i 6 randomiserade, dubbelblinda, placebokontrollerade fas II och III kliniska prövningar med 28 413 försökspersoner (20 541 flickor och kvinnor i åldern 16 till 26 år, 4 055 pojkar och män i åldern 16 till 26 år) qHPV-vaccinet har visat sig vara effektivt för att minska förekomsten av CIN (alla grader, inklusive CIN 2/3); AIS, könsvårtor; VIN 2/3; och VaIN 2/3 för vaccin mot HPV typ 6,11,16 eller 18 hos de tjejer och kvinnor som testade negativt på PCR och seronegativ vid baslinjen (tabell 2). QHPV -vaccinet var effektivt för att minska förekomsten av könsvårtor relaterade till HPV typ 6 och 11 hos pojkar och män som var PCR -negativa och seronegativa vid baslinjen. Effekt mot penis / perineal intraepitelial neoplasi (PIN) grad 1/2/3 / perianal eller penis / perineal / perianal cancer har inte påvisats på grund av för få fall för att nå statistisk signifikans (tabell 2). QHPV-vaccinet var effektivt för att minska förekomsten av anala intraepiteliala neoplasmer (AIN) grad 2 och 3 relaterade till HPV-vaccin typ 6, 11, 16 och 18 hos PCR-negativa och seronegativa pojkar och män vid baslinjen (tabell 2).
Tabell 2: Analys av qHPV -vaccineffektivitet i PPE -befolkningen * för vaccin mot olika typer av HPV
* PPE -befolkningen bestod av individer som hade fått alla 3 vaccinationer inom 1 år efter inskrivningen, som inte hade haft signifikanta avvikelser från studieprotokollet och var naiva (PCR -negativa och seronegativa) för de aktuella HPV -typerna (typ 6, 11 , 16 och 18) före dos 1 och upp till 1 månad efter dos 3 (månad 7).
† Analyserna av de sammanslagna studierna planerades prospektivt och inkluderade användning av liknande inkluderingskriterier.
N = antal personer med minst 1 uppföljningsbesök efter månad 7.
CI = konfidensintervall.
Effekt hos kvinnor i åldern 24 till 45 år
Effekten av qHPV-vaccin hos kvinnor 24 till 45 år utvärderades i en randomiserad, dubbelblind, placebokontrollerad fas III-studie (protokoll 019, FUTURE III), som omfattade totalt 3 817 kvinnor.
I PPE -befolkningen var effekten av qHPV -vaccin mot den kombinerade förekomsten av ihållande infektion, könsvårtor, vulva och vaginala lesioner, alla grader CIN, AIS och livmoderhalscancer relaterad till HPV typ 6, 11, 16 eller 18 88,7% (95% KI: 78,1, 94,8). Effekten av qHPV -vaccinet mot den kombinerade förekomsten av ihållande infektion, könsvårtor, vulvaskador och vaginala, CIN av alla kvaliteter, AIS och livmoderhalscancer relaterade till HPV typ 16 eller 18 var 84,7% (95% CI: 67,5, 93,7).
Långsiktiga effektstudier
En undergrupp av patienter följs för närvarande upp 10 till 14 år efter qHPV -vaccination för säkerhet, immunogenicitet och skydd mot klinisk sjukdom relaterad till HPV -typerna 6/11/16/18.
Antikroppssvarets beständighet observerades i 8 år hos ungdomar i åldern 9 till 15 år vid vaccinationstillfället; i 9 år hos kvinnor i åldern 16-23 vid vaccinationstillfället; i 6 år hos män i åldern 16 till 23 vid vaccinationstillfället och hos kvinnor i åldern 24 till 45 vid vaccinationstillfället.
Kliniskt skydd observerades hos alla ämnen (inklusive de som visade sig vara seronegativa för anti-HPV 6, anti-HPV 11, anti-HPV 16 och anti-HPV 18): inga fall av HPV-sjukdom observerades efter en uppföljning. cirka 6,9 år hos flickor mellan 9 och 15 år vid vaccinationen; 6,5 år hos män mellan 9 och 15 år vid vaccinationen; 8 år hos kvinnor i åldern 16 till 23 år vid vaccinationen; 6 år hos män i åldern 16 till 26 år vid vaccinationen och hos kvinnor i åldern 24 till 45 år vid vaccinationen.
Effekt hos HIV -infekterade patienter
En studie som dokumenterar säkerheten och immunogeniciteten för qHPV-vaccinet utfördes på 126 HIV-infekterade personer i åldern 7 till 12 år med en baslinje-CD4-frekvens ≥ 15 och minst 3 månaders högaktiv antiretroviral terapi (HAART) för personer med andel CD4 antigener förekom hos mer än 96% av försökspersonerna. Geometriska medel för titrar (GMT) var något lägre än de som rapporterats i andra studier av icke-HIV-infekterade försökspersoner i samma ålder. Klinisk relevans för det lägre svaret är okänd. Säkerhetsprofilen var liknande den hos icke-HIV-infekterade försökspersoner som rapporterats i andra studier. Andelen CD4- eller plasma-HIV-RNA påverkades inte av vaccination.
Kliniska studier av Gardasil 9
Effekten och / eller immunogeniciteten av Gardasil 9 utvärderades i sju kliniska studier. Kliniska prövningar som utvärderade effekten av Gardasil 9 jämfört med placebo var inte acceptabla eftersom HPV -vaccination rekommenderas och genomförs i många länder för skydd mot HPV -infektion och sjukdom. Därför utvärderade den avgörande kliniska prövningen (protokoll 001) effekten av Gardasil 9, med användning av qHPV -vaccinet som jämförelse.
Effekten mot HPV -typerna 6, 11, 16 och 18 bedömdes först med en överbryggande strategi som demonstrerade liknande immunogenicitet (mätt med Geometric Mean Titers (GMT)) av Gardasil 9 mot qHPV -vaccin (protokoll 001 och GDS01C / protokoll 009).
I den avgörande protokoll 001 -studien utvärderades effekten av Gardasil 9 mot HPV -typerna 31, 33, 45, 52 och 58 mot qHPV -vaccinet hos kvinnor i åldern 16 till 26 år (N = 14 204: 7 099 Gardasil 9 -mottagare; 7 105 qHPV vaccinmottagare).
I protokoll 002 utvärderades Gardasil 9: s immunogenicitet hos flickor och pojkar i åldrarna 9 till 15 och kvinnor i åldern 16 till 26 (N = 3.066: 1.932 flickor; 666 pojkar och 468 kvinnor som fick Garsadil 9).
Protokoll 003 utvärderade immunogeniciteten för Gardasil 9 hos män i åldrarna 16 till 26 och hos kvinnor i åldrarna 16 till 26 (1 103 heterosexuella män [HM]; 313 män som hade sex med män [MSM] och kvinnor som fick Gardasil 9).
Protokoll 005 och 007 utvärderade administrering av Gardasil 9 samtidigt med rutinmässigt rekommenderade vacciner till flickor och pojkar 11 till 15 år (N = 2 295).
I protokoll 006 utvärderade de administreringen av Gardasil 9 till flickor och kvinnor i åldern 12 till 26 år som tidigare vaccinerats med qHPV -vaccinet (N = 921; 615 som fick Gardasil 9 och 306 som fick placebo).
GDS01C / protokoll 009 utvärderade immunogeniciteten hos Gardasil 9 hos flickor 9 till 15 år (N = 600; 300 som fick Gardasil 9 och 300 som fick qHPV -vaccin).
Studier som stöder effekten av Gardasil 9 mot HPV typ 6, 11, 16, 18
Jämförande effektstudier mellan Gardasil 9 och qHPV -vaccinet mot de olika typerna av HPV 6, 11, 16 och 18 utfördes i en population av kvinnor i åldrarna 16 till 26 från protokoll 001 och flickor mellan 9 och 15 år från GDS01C / Protocol 009.
En "statistisk analys av non-inferioritet utfördes vid månad 7 och jämförde antikroppstitrarna cLIA GMT anti-HPV 6, anti-HPV 11, anti-HPV 16 och anti-HPV 18 mellan försökspersoner som vaccinerats med Gardasil 9 och försökspersoner som vaccinerats med Gardasil Immunsvar, mätt med GMT, för Gardasil 9 var inte sämre än immunsvar för Gardasil (tabell 3.) I kliniska prövningar blev 99,6-100% av försökspersoner som fick Gardasil 9 seropositiva för antikroppar mot alla 9 vaccintyper efter månad 7 i alla testade grupper.
Tabell 3: Jämförelse av immunsvar (mätt med cLIA) mellan Gardasil 9 och qHPV -vaccin för HPV -typ 6, 11, 16 och 18 i PPI * -populationen inklusive flickor och kvinnor i åldern 9 till 26 år.
* PPI -populationen bestod av försökspersoner som fick alla tre vaccinationer inom de angivna dagintervallen, visade inga större avvikelser från studieprotokollet, visade fördefinierade kriterier för intervallerna mellan sessionerna vid månad 6 och månad 7, var naiva (PCR -negativa och seronegativa) för de berörda HPV -typerna (typ 6, 11, 16 och 18) före dos 1 och flickor och kvinnor i åldrarna 16 till 26 år, PCR -negativa för HPV -typen i fråga upp till 1 månad efter dos 3 (månad 7).
§MMU = milli-Merck-enheter.
¶Värde-sid
CI = konfidensintervall.
GMT = Geometriskt medelvärde för aktier.
cLIA = Competitive Luminex Immunoassay.
N = Antal randomiserade patienter från respektive vaccinationsgrupp som fick minst en injektion.
n = antal försökspersoner som bidragit till analysen.
Studier som stöder effekten av Gardasil 9 mot HPV -typerna 31, 33, 45, 52 och 58 Effekten av Gardasil 9 utvärderades hos kvinnor i åldern 16 till 26 år, i en klinisk studie som jämfördes med - aktiv, dubbelblind, randomiserad kontroll (Protokoll 001), som omfattade totalt 14 204 kvinnor (Gardasil 9 = 7 099; qHPV -vaccin = 7 105). Ämnen följdes upp till månad 54 med en genomsnittlig uppföljningstid på 40 månader. Gardasil 9 var effektivt för att förebygga ihållande infektion och HPV-relaterade sjukdomar 31-, 33-, 45-, 52- och 58 (tabell 4). Gardasil 9 minskade också incidensen av Pap -utstötningsavvikelser, livmoderhals- och yttre genitalprocedurer (t.ex. biopsier) och slutgiltiga cervikalterapeutiska ingrepp relaterade till HPV 31, 33, 45, 52 och 58 (tabell 4).
Tabell 4: Analys av effekten av Gardasil 9 mot HPV -typerna 31, 33, 45, 52 och 58 i PPE -befolkningen ‡ inklusive kvinnor i åldern 16 till 26 år.
‡ PPE -befolkningen bestod av försökspersoner som hade fått alla 3 vaccinationer inom 1 år efter inskrivningen, inte hade några större avvikelser från studieprotokollet och var naiva (PCR -negativa och seronegativa) för de aktuella HPV -typerna (typ 31, 33, 45 , 52 och 58) före dos 1, och som förblev PCR -negativ för HPV -typerna i fråga 1 månad efter dos 3 (månad 7).
N = Antal försökspersoner randomiserade till respektive vaccinationsgrupp som fick minst en injektion.
n = antal individer som bidragit till analysen § Ihållande infektion upptäckt i prover efter två eller flera på varandra följande besök med 6 månaders mellanrum (besök fönster ± 1).
¶ Ihållande infektion upptäcktes i prover efter två eller flera på varandra följande besök med 6 månaders mellanrum (besök fönster ± 1).
#Papanicolaou -test.
CI = konfidensintervall.
ASC-US = Atypiska skivepitelceller av osäker betydelse.
HR = Hög risk.
* Antal personer med minst ett uppföljningsbesök efter månad 7.
** Ämnen följde upp till 54 månader efter dos 1 (median 4 år).
α Inga fall av livmoderhalscancer, VIN2 / 3, vulvar och vaginal cancer diagnostiserades i PPE -populationen.
† Elektrokirurgisk loop -excisionsprocedur (LEEP) eller konisering.
Utvärdering av den ytterligare effekten av Gardasil 9 mot HPV -typ 6, 11, 16, 18, 31, 33, 45, 52 och 58
Eftersom effekten av Gardasil 9 inte kunde utvärderas mot placebo, genomfördes följande undersökande analyser.Utvärdering av effekten av Gardasil 9 mot högkvalitativa livmoderhalssjukdomar orsakade av HPV typ 6, 11, 16, 18, 31, 33, 45, 52 och 58 i PPE Effekten av Gardasil 9 mot CIN 2 och högre, relaterad HPV typ 6, 11, 16, 18, 31, 33, 45, 52 och 58 jämfört med qHPV -vaccin var 94,4% (95% KI 78,8, 99,0) med 2 /5 952 fall mot 36 / 5,947 fall. Effekten av Gardasil 9 mot CIN 3 relaterad till HPV -typerna 6, 11, 16, 18, 31, 33, 45, 52 och 58 jämfört med qHPV -vaccinet var 100% (95% CI 46,3; 100, 0) med 0 / 5.952 fall mot 8 / 5.947.
Gardasil 9: s inverkan på livmoderhalsbiopsi och avgörande behandling relaterad till HPV typ 6, 11, 16, 18, 31, 33, 45, 52 och 58 vid PPE Effekten av Gardasil 9 mot HPV-relaterad livmoderhalsbiopsi av typ 6, 11 , 16, 18, 31, 33, 45, 52 och 58 jämfört med qHPV -vaccinet var 95,9% (95% CI 92,7, 97,9), med 11/6016 fall mot 262/6018. Effekten av Gardasil 9 mot avgörande livmoderhals terapi (inklusive elektrokirurgisk loop -excisionsprocedur (LEEP) eller konisering) relaterad till HPV typ 6, 11, 16, 18, 31, 33, 45, 52 och 58 jämfört med qHPV -vaccinet var 90,7% (95% CI 76,3; 97,0 ) med 4/6016 fall mot 43/6018.
Immunogenicitet Minsta anti-HPV-titer, som ger skyddande effekt, har inte fastställts. Typspecifika immunanalyser med typspecifika standarder användes för att bedöma immunogenicitet för varje HPV-typ som ingår i vaccinet. Dessa test mäter antikroppar mot neutraliserande epitoper för varje HPV-typ. Vågen för dessa tester är unika för varje typ. Varje HPV-typ; därför är typjämförelser och andra tester inte lämpliga Immunsvar mot Gardasil 9 vid månad 7 i alla kliniska prövningar Immunogenicitet mättes med andelen individer som är seropositiva för vaccinantikroppar av relevant typ HPV och det geometriska medelvärdet för titrarna (GMT ). Gardasil 9 inducerade robusta anti-HPV 6, anti-HPV 11, anti-HPV 16, anti-HPV 18, anti-HPV 31, anti-HPV 33, anti-HPV 45, anti-HPV 52 och anti-HPV immunsvar 58 mätt vid månad 7 (tabell 5). I kliniska studier blev 99,6-100% av individerna som fick Gardasil 9, efter månad 7 HIV-positiva för antikroppar mot alla 9 vaccintyper i alla testade grupper. GMT var högre hos flickor och pojkar än hos kvinnor i åldern 16 till 26 år och högre hos pojkar än hos flickor och kvinnor.
Tabell 5: Sammanfattning av månad 7, av det geometriska medelvärdet för titrarna mätt med cLIA Anti-HPV i PPI-populationen *
* PPI -populationen bestod av försökspersoner som fick alla tre vaccinationer inom ett bestämt dagintervall, visade inga större avvikelser från studieprotokollet, visade fördefinierade kriterier för intervallerna mellan sessionerna vid månad 6 och månad 7, var naiva (PCR -negativa och seronegativa) för de berörda HPV -typerna (typ 6, 11, 16 och 18) före dos 1 och hos flickor och kvinnor i åldern 16 till 26 år och som var PCR -negativa för de aktuella HPV -typerna (typ 6, 11, 16 och 18 ) 1 månad efter dos 3 (månad 7).
§MMU = milli-Merck-enheter.
cLIA = Competitive Luminex Immunoassay.
CI = konfidensintervall.
GMT = Geometriskt medelvärde för aktier.
N = Antal randomiserade patienter från respektive vaccinationsgrupp som fick minst en injektion.
n = antal försökspersoner som bidragit till analysen.
Anti-HPV-svar vid månad 7 hos flickor / pojkar 9 till 15 år var jämförbara med anti-HPV-svar hos kvinnor 16 till 26 år i den kombinerade Gardasil 9. immunogenicitetsstudiedatabasen. Sådan immunogenicitet överbryggar, effekten av Gardasil 9 hos pojkar och flickor i åldern 9 till 15 år dras slutsatsen.
Anti-HPV GMT-antikroppar vid månad 7 hos heterosexuella (HM) pojkar och män i åldern 16 till 26 år var jämförbara med anti-HPV GMT-antikroppar hos flickor och kvinnor i åldern 16 till 26 år. Hög immunogenicitet observerades hos män som har haft sexuellt umgänge med män (MSM) mellan 16 och 26 år, fastän mindre än hos HM, liknande qHPV -vaccinet. Dessa resultat stöder effekten av Gardasil 9 i den manliga befolkningen.
Inga studier har utförts på kvinnor över 26 år. Effekten av Gardasil 9 för de fyra ursprungliga typerna hos kvinnor i åldrarna 27 till 45 år förväntas baseras på den höga effekten av qHPV -vaccinet hos kvinnor i åldern 16 till 45 år och den jämförbara immunogeniciteten för Gardasil 9 och qHPV -vaccinet hos flickor och kvinnor i åldern 9 till 26 år.
Immunsvarets beständighet mot Gardasil 9 Antikroppssvarets beständighet efter ett komplett vaccinationsprogram med Gardasil 9 studeras i en undergrupp av patienter som kommer att följas i minst 10 år efter vaccination för att utvärdera säkerhet, "immunogenicitet och effekt. " Hos ungdomar i åldern 9 till 15 år har antikroppssvarets beständighet visats i minst 3 år; beroende på typ av HPV var 93-99% av försökspersonerna HIV-positiva. Hos kvinnor i åldern 16 till 26 år har antikroppssvarets beständighet visats i minst 3,5 år; beroende på typ av HPV var 78-98% av försökspersonerna HIV-positiva. Effekten bibehölls i alla ämnen fram till slutet av studien, oavsett seropositiv status, för alla typer av HPV -vaccin.
Administrering av Gardasil 9 till individer som tidigare vaccinerats med qHPV -vaccinet
Protokoll 006 utvärderade immunogeniciteten för Gardasil 9 hos 921 flickor och kvinnor (i åldern 12 till 26 år) som tidigare hade vaccinerats med qHPV-vaccinet. administrerades med ett intervall på minst 12 månader mellan slutförandet av vaccination med qHPV -vaccinet och initiering av vaccination med Gardasil 9, (tidsintervallet 12 till 36 månader). per protokoll, seropositivitet för HPV -typer 6, 11, 16, 18, 31, 33, 45, 52 och 58 vid månad 7, varierade från 98,3 till 100%, hos försökspersoner som fick Gardasil 9. GMT för HPV -typ 6, 11, 16, 18 var högre än befolkningen som inte tidigare fått qHPV -vaccinet i andra studier, medan GMT för HPV -typerna 31, 33, 45, 52 och 58 var lägre. Den kliniska betydelsen av denna observationsstudie är okänd.
Graviditet
Inga specifika studier har utförts på Gardasil 9 hos gravida kvinnor. QHPV -vaccin användes som en aktiv kontroll under det kliniska utvecklingsprogrammet för Gardasil 9.
Under det kliniska utvecklingsprogrammet Gardasil 9 upplevde 2 586 kvinnor (inklusive 1 347 i gruppen Gardasil 9 mottagare mot 1 239 i mottagargruppen för qHPV -vaccin) minst en graviditet. Typen av abnormiteter eller andelen negativa graviditeter hos försökspersoner som fick Gardasil 9 eller qHPV -vaccinet var jämförbara och överensstämde med dem som rapporterats av den allmänna befolkningen.
05.2 "Farmakokinetiska egenskaper
Inte tillämpbar.
05.3 Prekliniska säkerhetsdata
Studier av enstaka och upprepade doser av toxicitet hos råttor och lokala toleransstudier avslöjade ingen särskild risk för människor.
Administrering av Gardasil 9 till honråttor hade ingen effekt på reproduktionskapacitet, fertilitet eller embryonal / fosterutveckling.
Administrering av Gardasil 9 till honråttor hade ingen effekt på avkommans utveckling, beteende, reproduktionskapacitet eller fertilitet. Antikroppar mot alla 9 HPV -typer överfördes till avkommor under dräktighet och amning.
06.0 LÄKEMEDELSINFORMATION
06.1 Hjälpämnen
Natriumklorid
L-histidin
Polysorbat 80
Natriumborat
Vatten för injektionsvätskor
För adjuvans, se avsnitt 2.
06.2 Oförenlighet
I avsaknad av kompatibilitetsstudier får detta läkemedel inte blandas med andra produkter.
06.3 Giltighetstid
3 år.
06.4 Särskilda förvaringsanvisningar
Förvaras i kylskåp (2 ° C - 8 ° C).
Frys inte. Förvara den förfyllda sprutan i ytterkartongen för att skydda den mot ljus.
Gardasil 9 ska administreras så snart som möjligt efter att ha tagits ur kylskåpet.
Stabilitetsdata indikerar att vaccinkomponenterna förblir stabila under en period av 72 timmar om vaccinet förvaras vid temperaturer mellan 8 ° C och 25 ° C eller mellan 0 ° C och 2 ° C. Vid slutet av denna tid måste Gardasil 9 användas eller kasseras. Dessa data är en guide för vårdpersonal endast vid tillfällig temperaturutflykt.
06.5 Förpackningens innehåll och förpackningens innehåll
0,5 ml suspension i förfylld spruta (glas) med kolvpropp (silikoniserad FluroTec-belagd bromobutylelastomer) och lock (syntetisk blandning av isopren och brombutyl), med 2 nålar i förpackningar om 1 till 10.
Alla förpackningsstorlekar kanske inte marknadsförs.
06.6 Anvisningar för användning och hantering
• Innan skakning kan Gardasil 9 se ut som en klar vätska med en vit fällning.
• Skaka väl före användning tills en suspension bildas. Efter noggrann omrörning erhålls en vit opaliserande vätska.
• Före administrering ska suspensionen inspekteras visuellt med avseende på förekomst av partiklar och missfärgning Kassera vaccinet i närvaro av partiklar och / eller om färgen verkar missfärgad.
• 2 nålar med olika längd finns i förpackningen, välj lämplig nål för att säkerställa intramuskulär (IM) administrering baserat på patientens storlek och vikt.
• Sätt in nålen genom att vrida den medurs tills den sitter ordentligt på sprutan. Administrera hela dosen enligt protokollet.
• Injicera omedelbart intramuskulärt (IM), helst i deltoidregionen av överarmen eller det övre anterolaterala området på låret.
• Vaccinet ska användas enligt anvisningarna. Den fullständiga rekommenderade vaccindosen ska användas.
• Grundlig skakning omedelbart före användning krävs för att hålla vaccinet i suspension.
Allt oanvänt material och avfall från detta läkemedel måste kasseras i enlighet med lokala föreskrifter.
07.0 INNEHAVARE AV GODKÄNNANDE FÖR FÖRSÄLJNING
Sanofi Pasteur MSD SNC
162 avenue Jean Jaurès
69007 Lyon
Frankrike
08.0 NUMMER FÖR FÖRSÄLJNINGSTILLSTÅND
EU/1/15/1007/002
700017940
EU/1/15/1007/003
700017953
09.0 DATUM FÖR FÖRSTA GODKÄNNANDE ELLER FÖRNYELSE AV GODKÄNNANDET
Datum för första godkännandet: DD månad ÅÅÅÅ