Vad är Luveris?
Luveris är ett läkemedel som innehåller den aktiva substansen lutropin alfa. Det finns som pulver och lösningsmedel för att framställa en lösning för injektion och som en lösning för injektion i en patron.
Vad används Luveris till?
Luveris används vid behandling av infertilitet. Tillsammans med follikelstimulerande hormon (FSH) stimulerar det mognad av ägg i äggstockarna hos kvinnor med svår brist (mycket låga nivåer) av luteiniserande hormon (LH) och FSH.
Läkemedlet kan endast fås på recept.
Hur används Luveris?
Luveris -behandling bör utföras av läkare med erfarenhet av infertilitetsbehandling.
Luveris ges tillsammans med FSH en gång om dagen. Svar på behandlingen bör övervakas för att övervaka utvecklingen av äggutvecklingen i äggstocken. FSH -dosen bör justeras enligt patientens svar och behandlingen kan pågå. Upp till fem veckor. Luveris ges genom injektion under huden (under huden). Injektionen kan övas av patienten själv på lämpligt sätt instruerat av läkaren och under förutsättning att hon har möjlighet att rådgöra med en expert.
Om pulver och lösningsmedel används måste de blandas omedelbart före användning.Den resulterande lösningen kan blandas med FSH i samma spruta. En injektionsflaska med pulver och lösningsmedel är endast avsedd för engångsbruk, men varje patron med lösning innehåller sex doser Luveris.
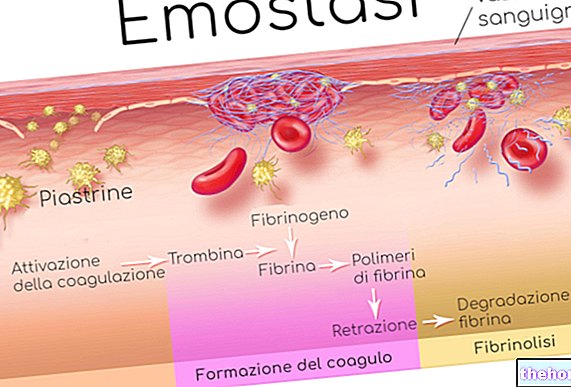
Hur fungerar Luveris?
Den aktiva substansen i Luveris är lutropin alfa, en kopia av det naturligt producerade hormonet LH. När det släpps ut i kroppen orsakar hormonet LH att äggen frigörs (ägglossning) under menstruationscykeln.Luveris används i kombination med FSH, vilket också stimulerar ägglossning.
Lutropin alfa produceras med en metod som kallas 'rekombinant DNA -teknik': den tillverkas av en cell som har mottagit en gen (DNA), vilket gör den kapabel att producera humant LH.
Hur har Luveris studerats?
Luveris, givet med FSH, var föremål för en huvudstudie med 38 kvinnor med svår LH- och FSH -brist. På grund av det lilla antalet patienter med denna dysfunktion jämfördes Luveris inte med andra läkemedel. Det främsta måttet på effektivitet var antalet kvinnor som producerade funktionella folliklar (ägg inne i äggstockarna redo att släppas).
Vilken nytta har Luveris visat under studierna?
I huvudstudien producerade 67% av kvinnorna som tog den godkända dosen Luveris (75 internationella enheter) i kombination med FSH funktionella folliklar (6 av 9). Högre doser visade inte större effekt än vid denna dos.
Vilken risk är förknippad med Luveris?
De vanligaste biverkningarna som ses med Luveris (ses hos 1 till 10 patienter av 100) är reaktioner på injektionsstället, huvudvärk, dåsighet, illamående, buksmärtor, smärta i bäckenregionen (nedre delen av buken), ovarial hyperstimuleringssyndrom (såsom illamående, viktökning och diarré), cystor på äggstockarna (utveckling av vätskefylld hålighet i äggstockarna) och bröstsmärta. Ovarial hyperstimuleringssyndrom uppstår när äggstockarna överreagerar på behandling, särskilt om de har använts för att stimulera ägglossning. En fullständig förteckning över biverkningar som rapporterats för Luveris finns i bipacksedeln.
Luveris får inte användas till personer som kan vara överkänsliga (allergiska) mot "LH", FSH eller andra ingredienser i läkemedlet. Det får inte användas till kvinnor med cancer i hypofysen, hypothalamus, bröst, livmoder eller äggstockar. Det ska inte heller användas i närvaro av äggstocksförstoring eller närvaro av cystor som inte beror på polycystisk äggstockssjukdom eller oförklarlig vaginal blödning. För fullständig lista över användningsrestriktioner, se bipacksedeln.
Varför har Luveris godkänts?
Kommittén för humanläkemedel (CHMP) beslutade att Luveris fördelar är större än riskerna i kombination med ett FSH -preparat för att stimulera follikelutveckling hos kvinnor med svår LH- och FSH -brist. Kommittén rekommenderade att Luveris skulle godkännas för försäljning.
Annan information om Luveris:
Den 29 november 2000 beviljade Europeiska kommissionen Serono Europe Limited ett "marknadsföringstillstånd" för Luveris, giltigt i hela Europeiska unionen. "Marknadstillstånd" förnyades den 29 november 2005.
För den fullständiga versionen av Luveris EPAR klicka här.
Senaste uppdateringen av denna sammanfattning: 04-2009.
Informationen om Luveris - Lutropin alfa som publiceras på denna sida kan vara inaktuell eller ofullständig. För korrekt användning av denna information, se sidan Ansvarsfriskrivning och användbar information.