Trypsin och kymotrypsin är två viktiga enzymer i matsmältningen av matproteiner. Båda produceras och utsöndras som zymogener, dvs i inaktiv form, av bukspottkörteln; zymogenprekursorn för trypsin kallas trypsinogen, medan chymotrypsin kallas chymotrypsinogen.
Trypsin och kymotrypsin tillhör den stora familjen proteolytiska enzymer (involverade i proteinsmältning) och till undergruppen av endopeptidaser. Dessa ämnen - inklusive magepepsin och bukspottkörtelelastas - angriper peptidbindningarna i aminosyrakedjan, vilket ger upphov till mindre molekylfragment. Enzymerna som tillhör den andra gruppen, exopeptidasernas, slutför trypsin och kymotrypsins arbete och lossar enstaka aminosyror från ändarna av peptidkedjan; bukspottkörteln karboxypeptidaser (A1, A2 och B, som angriper karboxyländen), men även aminopeptidaserna (som angriper den aminoterminala änden) och dipeptidaser, både producerade och utsöndrade av tunntarmens slemhinna, tillhör denna familj. karboxypeptidas, liknande det som har sett för trypsin (trypsinogen) och chymotrypsin (chymotrypsinogen), utsöndras av bukspottkörteln i inaktiv form.I alla tre fallen är enzymet som är involverat i den enzymatiska aktiveringsprocessen enteropeptidas, ett protein som produceras och utsöndras av cellerna av duodenalslemhinnan; mer specifikt är enteropeptidas specifikt för trypsinogen, som en gång omvandlades till trypsin också aktiverar de andra proteolytiska enzymerna, inklusive samma trypsinogen.
Låt oss kort komma ihåg att tolvfingertarmen är den första delen av tunntarmen och att inte bara bukspottskörteljuicer strömmar in i den, utan också leverjuicer (galla), avgörande för pH -korrigering och lipidsmältning.

De funktionella skillnaderna mellan trypsin och kymotrypsin gäller helt enkelt deras specificitet, det vill säga förmågan att känna igen och dela endast de bindningar som bildas av specifika aminosyror. Trypsin verkar framför allt på peptidbindningar som engagerar basiska aminosyror (såsom arginin och lysin), medan kymotrypsin huvudsakligen hydrolyserar bindningar som involverar tyrosin, fenylalanin, tryptofan, leucin och metionin.
Tack vare de olika proteolytiska enzymerna, med bidrag från magsyra, bryts proteinerna i kosten - ursprungligen bildade av flera dussin aminosyror - till dipeptider, tripeptider och fria aminosyror, alla lätt absorberbara ämnen som kommer från kapillärerna i tarmslemhinnan transporteras till levern.
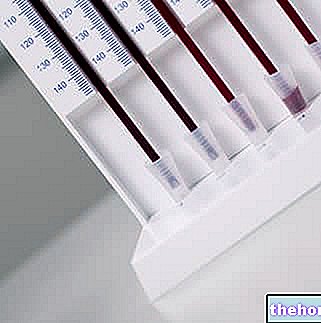
Trypsin och kymotrypsin i avföringen
Bestämningen av kymotrypsin och trypsin i avföring används, och var särskilt så tidigare, som ett indirekt test av den exokrina bukspottkörtelns funktionella kapacitet. Om något på denna körtelns nivå inte fungerar som det ska, är det logiskt att förvänta sig en minskad syntes av trypsin och kymotrypsin, vilket också kommer att vara bristfälligt i avföringen. Testet har god känslighet, men belastas med den verkliga risken för falska positiva och falska negativ. Användningen av laxermedel minskar till exempel koncentrationen av enzymer i fekalt material, medan intaget av bukspottkörtel (t.ex. pankreatin) eller grönsaker (t.ex.ananasstam, papaya, papain och bromelain) orsakar falskt negativa resultat. Tarmfloran påverkar också något av trypsin och kymotrypsin som kommer oförändrat i avföringen; av denna anledning kan användning av antibiotika ge falska negativ; tvärtom, i närvaro av divertikulos och andra tillstånd som gynnar bakteriell spridning, kan falska positiva resultat registreras.
En klassisk tillämpning av trypsin- och kymotrypsinanalys i avföring är upptäckt av bukspottkörtelinsufficiens hos patienter med cystisk fibros.En av konsekvenserna av denna sjukdom är försämringen av normal transport av trypsin och andra matsmältningsenzymer från bukspottkörteln till tolvfingertarmen. av denna anledning, vid födseln, är avföringen hos barnet med cystisk fibros särskilt kompakt för att orsaka tarmobstruktion. Följaktligen finns det särskilt små mängder kymotrypsin och trypsin i mekonium.























.jpg)

