Aktiva ingredienser: Nadroparin (Calcium Nadroparin)
FRAXIPARINA 2.850 I.U. antiXa / 0,3 ml injektionsvätska, lösning
FRAXIPARINA 3800 I.U. antiXa / 0,4 ml injektionsvätska, lösning
FRAXIPARINA 5700 I.E. antiXa / 0,6 ml injektionsvätska, lösning
FRAXIPARINA 7600 I.U. antiXa / 0,8 ml injektionsvätska, lösning
FRAXIPARINA 9.500 I.U. antiXa / 1 ml injektionsvätska, lösning
Varför används Fraxiparin? Vad är det för?
Fraxiparin innehåller den aktiva substansen nadroparinkalcium, ett antitrombotiskt preparat från heparin som används för att förhindra blodproppar.
Fraxiparin används:
- Vid förebyggande av djup ventrombos (DVT) vid allmän kirurgi och vid ortopedisk kirurgi. Det tjänar därför till att förhindra bildning av blodproppar i venerna i benen vid omöjlighet eller minskad risk för rörelse efter större operation.
- Vid behandling av djup ventrombos.
- För att förebygga koagelbildning under hemodialys, som tjänar till att rena blodet hos patienter som lider av njurinsufficiens
- Vid behandling av särskilda former av hjärtinfarkt (instabil angina och icke-Q-hjärtinfarkt).
Tala med din läkare om du inte mår bättre eller om du mår sämre.
Kontraindikationer När Fraxiparin inte ska användas
Använd inte FRAXIPARINE
- om du är allergisk mot kalcium nadroparin eller något annat innehållsämne i detta läkemedel
- om du tidigare har haft trombocytopeni (lågt antal trombocyter, cellerna som är ansvariga för blodproppar)
- om du löper en ökad risk för blödning relaterad till blödningsstörningar, med undantag för spridd intravaskulär koagulation (ett allvarligt syndrom som leder till blodpropp i många blodkärl) som inte induceras av heparin.
- om du har skador med risk för blödning (t.ex. aktivt magsår - magsår)
- om du lider (eller har lidit) av retinopatier (näthinnesjukdomar, membranet som täcker ögats inre yta)
- om du lider av (eller har haft) blödningssyndrom.
- om du har (eller har lidit) av hjärnblödningar (hjärnblödningar)
- om du har (eller har lidit) av en "infektion i hjärtats innerfoder (akut infektiös endokardit)
- om du har svår njurinsufficiens och behandlas för djup venetrombos, instabil angina och icke-Q-hjärtinfarkt.
- om du har allvarlig njure- eller bukspottskörtel
- om du har mycket högt blodtryck (svår arteriell hypertoni)
- om du nyligen har opererats för en huvudskada (kirurgiskt behandlad huvudskada)
- vid lokalregional anestesi för kirurgiska ingrepp.
Försiktighetsåtgärder vid användning Vad du behöver veta innan du tar Fraxiparin
Tala med din läkare eller apotekspersonal innan du använder Fraxiparin.
Du kan utveckla heparininducerad trombocytopeni (lågt antal blodplättar), därför bör ditt trombocytantal övervakas under hela behandlingen med nadroparin.
Det har förekommit sällsynta rapporter om trombocytopeni, ibland allvarliga, som kan vara associerade med arteriell eller venös trombos. Denna diagnos bör övervägas i följande situationer:
- trombocytopeni
- någon signifikant minskning av blodplättarnas nivå
- försämring av initial trombos under behandlingen
- trombos som uppstår under behandlingen
- sprids intravaskulär koagulation
I sådana fall bör behandlingen med nadroparin avbrytas.
Om du har trombocytopeni på grund av behandling med heparin (både standard och låg molekylvikt) kan din läkare överväga:
- vid behov behandling med nadroparin.
- ersättare med en antitrombot av en annan klass
- om detta inte är möjligt, men administrering av heparin är nödvändig, ersätts med ett annat "lågmolekylärt heparin
I sådana fall kommer din läkare att behöva övervaka trombocyttalet minst dagligen och om trombocytopeni inträffar ska behandlingen avbrytas omedelbart (se "Använd inte FRAXIPARINE").
Nadroparin ska användas med försiktighet i följande situationer, vilket kan vara förknippat med en ökad risk för blödning:
- leversvikt (leversvikt)
- mycket högt blodtryck (svår arteriell hypertoni)
- historia av magsår (magsår) eller andra organiska skador med risk för blödning
- kärlsjukdom av chorioretin (en del av ögat med många blodkärl)
- under den postoperativa perioden efter hjärnkirurgi, ryggrads- eller ögonoperation och vid huvudskador.
Var särskilt uppmärksam på:
- Om du har nedsatt njurfunktion: du har en ökad risk för blödning och bör behandlas med försiktighet
- Om du är äldre: din läkare måste kontrollera din njurfunktion innan behandlingen påbörjas (se "Använd inte Fraxiparin").
- Om du har höga kaliumnivåer i blodet eller om du löper risk för ökade kaliumnivåer, till exempel om du har diabetes mellitus, kroniskt njursvikt, redan existerande metabolisk acidos (störningar i koncentrationen av gaser och salter i blodet ) eller om du tar läkemedel som kan öka kaliumnivåerna i ditt blod (till exempel ACE-hämmare, icke-steroida antiinflammatoriska läkemedel (NSAID)), kan heparin undertrycka produktionen av aldosteron (ett hormon som reglerar koncentrationen av salter i blodet) med resulterande i ökade kaliumnivåer i blodet Denna risk tycks öka i förhållande till behandlingstiden, men är i allmänhet reversibel.
- Om du genomgår spinal- eller epiduralanestesi kan användning av lågmolekylär heparin sällan förknippas med hematom, vilket kan leda till långvarig eller permanent förlamning av underbenen. Du kommer därför att behöva övervakas ofta för tecken och symtom på neurologiska förändringar. såsom ryggsmärta, sensoriska och motoriska underskott (domningar och svaghet i nedre extremiteterna), tarm- och / eller urinblåsdysfunktion. Du bör omedelbart informera läkare eller vårdpersonal om något av ovanstående symtom uppstår. hematom / epidural förstärks med katetrar placerade i ryggmärgen (epidural kateter) eller genom samtidig användning av andra läkemedel som kan påverka koagulation, såsom icke-steroida antiinflammatoriska läkemedel (NSAID), trombocytaggregationshämmare eller andra antikoagulantia. ökar också av trauma eller upprepade ländryggen.
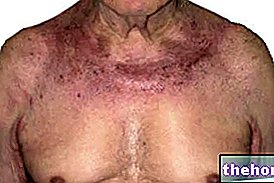
- om du märker tecken som mörkröd färg (kutan purpura) eller infiltrerade eller smärtsamma erytematösa plack, med eller utan allmänna symtom, eftersom dessa kan vara associerade med hudanekros (dvs död av hudvävnader) som har rapporterats mycket sällan. I sådana fall kommer läkaren att avbryta behandlingen omedelbart.
Latexallergi
Skyddet på nålen på den förfyllda sprutan kan innehålla latexgummi, vilket kan orsaka allvarliga allergiska reaktioner hos de som är känsliga för latex.
Barn och ungdomar
Nadroparin rekommenderas inte för barn och ungdomar under 18 år.
Interaktioner Vilka läkemedel eller livsmedel kan ändra effekten av Fraxiparin
Tala om för din läkare eller apotekspersonal om du tar, nyligen har tagit eller kan tänkas ta andra läkemedel. Nadroparin ska administreras med försiktighet om du tar:
- orala antikoagulantia, eftersom samtidig administrering kan öka den antikoagulerande effekten
- (gluko-) systemiska kortikosteroider (kortison och liknande), eftersom samtidig administrering kan öka risken för blödning
- dextrans (ämnen som används för att öka blodvolymen) eftersom samtidig administrering kan öka risken för blödning
- Vid samtidig administrering av askorbinsyra (vitamin C), antihistaminer, digitalis, penicilliner IV, tetracykliner eller fenotiaziner, eftersom det är möjligt att administrera samtidigt, kan läkemedlets aktivitet minskas.
Fraxiparin rekommenderas inte om du tar följande läkemedel eftersom risken för blödning ökar i dessa fall:
- Acetylsalicylsyra och andra salicylater, icke-steroida antiinflammatoriska läkemedel-NSAID (generellt). Använd andra ämnen för smärtstillande eller febernedsättande effekt.
- Tiklopidin (oral antikoagulant) - Andra trombocythämmande medel (klopidogrel, dipyridamol, sulfinpyrazon, etc.)
Varningar Det är viktigt att veta att:
Graviditet, amning och fertilitet
Om du är gravid eller ammar, tror att du kan vara gravid eller planerar att skaffa barn, rådfråga din läkare eller apotekspersonal innan du använder detta läkemedel.
Graviditet
Användning av nadroparin under graviditet rekommenderas inte om inte de terapeutiska fördelarna överväger de möjliga riskerna.
Matdags
Information om utsöndring av nadroparin i bröstmjölk är begränsad. Som en försiktighetsåtgärd bör ammande mödrar som får nadroparin avrådas från att amma.
Fertilitet
Det finns inga studier om effekten av nadroparin på fertiliteten.
Köra och använda maskiner
Inga studier har gjorts om förmågan att framföra fordon och använda maskiner.
Dosering och användningssätt Hur man använder Fraxiparin: Dosering
Använd alltid detta läkemedel enligt läkarens eller apotekspersonalens anvisningar. Kontakta din läkare eller apotekspersonal om du är osäker.
Blanda inte kalcium nadroparin med andra preparat.
Var särskilt uppmärksam på doseringsanvisningarna, specifika för olika märken av lågmolekylär heparin, eftersom olika mätsystem används för varje heparin med låg molekylvikt för att uttrycka doserna (enheter eller mg).
Därför ska nadroparin inte användas omväxlande med andra lågmolekylära hepariner under behandlingen.
Nadroparin ska inte ges intramuskulärt.
Administrering av nadroparin under den tid som ligger nära en spinal / epidural anestesi eller en ländryggen punktering bör följa specifika rekommendationer (se "Varningar och försiktighetsåtgärder").
Du bör övervaka ditt trombocytantal under behandlingen med nadroparin (se "Varningar och försiktighetsåtgärder").
Subkutan injektionsteknik
När adroparin administreras subkutant ska injektion ges på den anterolaterala eller posterolaterala sidan av bukväggen, alternerande mellan höger och vänster sida. Låret kan vara ett alternativt ställe.
För att undvika läckage av lösning när du använder förfyllda sprutor, ska du inte slänga ut luftbubblan från sprutan innan du injicerar.
Nålen måste införas helt, vinkelrätt (dvs. bilda en vinkel på 90 grader med buken) och inte tangentiellt, i tjockleken på en hudveck mellan tummen och pekfingret på operatören.
Vikningen måste bibehållas under injektionens varaktighet. Efter injektionen ska du inte gnugga huden utan utöva lätt tryck på platsen.
I fallet med en dos anpassad till dess vikt, justeras volymen som ska administreras genom att föra kolven till önskat skår medan sprutan hålls i vertikalt läge.
Sprutor är endast för engångsbruk och allt oanvänt innehåll i varje spruta ska kasseras. Lösningar ska inte blandas med andra preparat eller administreras på nytt.
Förebyggande av djup ventrombos
Subkutan administrering
Vid allmän kirurgi: den rekommenderade dosen är en subkutan injektion 2-4 timmar före operationen. Därefter var 24: e timme i minst 7 dagar; i alla fall måste profylax fortsätta under hela riskperioden och åtminstone tills promenader börjar igen.
Vid ortopedisk kirurgi: den rekommenderade dosen är en injektion före operationen 12 timmar före operationen, en postoperativ 12 timmar efter operationens slut, sedan en daglig injektion. Behandlingstiden är minst 10 dagar; i alla fall bör profylax fortsättas under riskperioden och åtminstone tills promenader börjar igen.
Behandling av djup ventrombos
Subkutan administrering: den rekommenderade dosen är en injektion var 12: e timme
Om det inte finns några kontraindikationer, starta oral antikoagulantbehandling så snart som möjligt.
Du bör övervaka ditt trombocytantal under behandlingen med nadroparin (se "Varningar och försiktighetsåtgärder").
Förebyggande av koagulation under hemodialys
Intravaskulär administrering: om det inte finns någon risk för blödning och för en session som varar mindre än eller lika med 4 timmar måste en injektion av en engångsdos ges i början av sessionen, i arteriell åtkomst, utvärderas efter dess vikt.
Om du har ökad risk för blödning kan dialyspass utföras med en dos reducerad till hälften.
Vid sessioner som är längre än 4 timmar kan en ytterligare reducerad dos administreras.För efterföljande dialyspass kan dosen om nödvändigt justeras utifrån den effekt som observerades initialt.
Han måste noggrant övervakas under dialyspasset för tecken på blödning eller koagulering i dialyskretsen.
Behandling av instabil angina och icke-Q-hjärtinfarkt
Subkutan administrering
Den rekommenderade dosen nadroparin, administrerad subkutant, är två gånger dagligen (var 12: e timme). Behandlingstiden är i allmänhet 6 dagar.
Användning till barn och ungdomar
Nadroparin rekommenderas inte till barn och ungdomar eftersom det inte finns tillräckliga säkerhets- och effektdata för att fastställa dosen till patienter under 18 år.
Pensionärer
Ingen dosjustering är nödvändig om du är äldre om inte njurfunktionen är nedsatt. Din läkare kommer att kontrollera din njurfunktion innan behandlingen påbörjas (se "Njursvikt" nedan).
Njursvikt
Förebyggande av djup ventrombos
Ingen dosreduktion krävs om du har lätt njurinsufficiens.Om du har måttlig eller svår njurinsufficiens har du en ökad risk för tromboembolism och blödning. Om läkaren bedömer att en dosreduktion är lämplig, med hänsyn tagen till enskilda hemoragiska och tromboemboliska riskfaktorer, bör dosen minskas variabelt (se "Varningar och försiktighetsåtgärder") om du har måttlig eller svår njurinsufficiens.
Fraxiparin är kontraindicerat om du har svår njurinsufficiens.
Behandling av djup ventrombos, instabil angina och icke-Q-hjärtinfarkt.
Om du har lätt njurinsufficiens och tar nadroparin för att behandla dessa tillstånd är det inte nödvändigt att minska dosen.
Om du har måttlig eller svår njurinsufficiens har du en ökad risk för tromboembolism och blödning.
Om läkaren bedömer att en dosreduktion är lämplig, med hänsyn tagen till enskilda hemoragiska och tromboemboliska riskfaktorer, om du har måttlig eller svår njurinsufficiens, bör dosen minskas variabelt (se "Varningar och försiktighetsåtgärder").
Nadroparin är kontraindicerat hos patienter med svår njurinsufficiens
Nedsatt leverfunktion Inga studier har utförts på patienter med nedsatt leverfunktion.
Överdosering Vad du ska göra om du har tagit för mycket Fraxiparin
Om du av misstag tar en överdos av Fraxiparin, meddela din läkare omedelbart eller gå till närmaste sjukhus.
Den mest uppenbara manifestationen av överdosering, både subkutant och intravenöst, är blödning.I detta fall måste läkaren utföra en trombocyttal för att mäta de andra koagulationsparametrarna.
Mindre blödningar kräver sällan specifik behandling och det är vanligtvis tillräckligt för att minska eller fördröja efterföljande doser av nadroparin.
Fråga din läkare eller apotekspersonal om du har ytterligare frågor om användningen av detta läkemedel.
Om du slutar att ta Fraxiparin
Fråga din läkare eller apotekspersonal om du har ytterligare frågor om användningen av detta läkemedel.
Biverkningar Vilka är biverkningarna av Fraxiparin
Liksom alla läkemedel kan detta läkemedel orsaka biverkningar men alla användare behöver inte få dem.
Biverkningar listas nedan i frekvensfrekvens:
Mycket vanliga (kan förekomma hos fler än 1 av 10 personer)
- Blödning på olika platser (inklusive fall av spinal hematom), mer frekvent hos patienter med andra riskfaktorer (se "Använd inte Fraxiparin" och "Varningar och försiktighetsåtgärder").
- Injektionshematom: I vissa fall kan utseende av fasta knölar noteras. Dessa knölar försvinner i allmänhet efter några dagar.
Vanliga (kan förekomma hos upp till 1 av 10 personer)
- Ökning av transaminaser (enzymer som produceras av levern), vanligtvis övergående
- Reaktion på injektionsstället
Sällsynta (kan förekomma hos upp till 1 av 1000 användare)
- Trombocytopeni, dvs. minskning av antalet trombocyter i blodet (inklusive den som induceras av heparin), trombocytos (ökning av antalet trombocyter i blodet).
- Utslag, nässelfeber, erytem, klåda.
- Calcinosis (avsättning av kalciumsalter) på injektionsstället. Calcinosis är vanligare hos patienter med onormal kalciumfosfatproduktion, liksom i vissa fall av kroniskt njursvikt.
Mycket sällsynta (kan förekomma hos upp till 1 av 10 000 personer)
- Eosinofili, d.v.s. en ökning av antalet av en typ av vita blodkroppar i blodet som är reversibel när behandlingen avbryts.
- Överkänslighetsreaktioner (inklusive angioödem och hudreaktioner), anafylaktoid reaktion.
- reversibel ökning av blodkaliumkoncentrationen, särskilt hos patienter i riskzonen
- Priapism (onormal, långvarig och smärtsam erektion).
- Hudnekros (död av hudvävnader), vanligtvis vid injektionsstället
Rapportering av biverkningar
Om du får några biverkningar, tala med din läkare, apotekspersonal eller sjuksköterska. Detta inkluderar eventuella biverkningar som inte nämns i denna bipacksedel. Du kan också rapportera biverkningar direkt via det nationella rapporteringssystemet. / Ansvarig.
Genom att rapportera biverkningar kan du hjälpa till att ge mer information om läkemedlets säkerhet.
Giltighetstid och lagring
Förvara detta läkemedel utom syn- och räckhåll för barn.
Använd inte detta läkemedel efter utgångsdatum som anges på förpackningen efter EXP. Utgångsdatumet avser den sista dagen i den månaden. Utgångsdatumet avser den oöppnade, korrekt lagrade produkten.
Använd inte detta läkemedel om du märker några partiklar (t.ex. fast material i en flytande lösning) eller en förändring i färgen på nadroparin injektionsvätska. Om du märker någon förändring visuellt bör lösningen kasseras.
Detta läkemedel kräver inga särskilda förvaringsförhållanden.
Frys inte. Förvara inte i kylskåp eftersom kalla injektioner kan vara smärtsamma.
Kasta inga läkemedel i avloppsvatten eller hushållsavfall. Fråga din apotekare om hur du ska kasta läkemedel som du inte använder längre. Detta skyddar miljön.
Annan information
Vad FRAXIPARINE innehåller
Den aktiva ingrediensen är kalcium nadroparin (I.U.antiXa). 1 förfylld spruta innehåller:
- 0,3 ml FRAXIPARINA 2.850 I.U. antiXa;
- 0,4 ml FRAXIPARINA 3.800 I.U. antiXa;
- 0,6 ml FRAXIPARINA 5.700U.I. antiXa;
- 0,8 ml FRAXIPARINA 7.600U.I. antiXa;
- 1 ml FRAXIPARINA 9.500U.I. antiXa.
Övriga innehållsämnen är: kalciumhydroxidlösning eller utspädd saltsyra - vatten för injektionsvätskor.
Beskrivning av hur Fraxiparin ser ut och förpackningens innehåll
Injektionsvätska, lösning för subkutan användning och för hemodialys
- 6 förfyllda graderade sprutor redo för användning av 0,3 ml (2850 I.U.antiXa)
- 6 förfyllda graderade sprutor redo för användning av 0,4 ml (3800 I.U. antiXa)
- 10 förfyllda graderade sprutor redo att använda 0,6 ml (5700 I.U.antiXa)
- 10 förfyllda graderade sprutor färdiga för användning på 0,8 ml (7.600 I.U.antiXa)
- 10 förfyllda graderade sprutor redo att använda 1 ml (9 500 I.U.antiXa)
Bipacksedel: AIFA (Italian Medicines Agency). Innehåll publicerat i januari 2016. Den information som finns finns kanske inte uppdaterad.
För att få tillgång till den senaste versionen är det lämpligt att gå till AIFA (Italian Medicines Agency) webbplats. Ansvarsfriskrivning och användbar information.
01.0 LÄKEMEDLETS NAMN
FRAXIPARINA
02.0 KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING
För fullständig förteckning över hjälpämnen, se avsnitt 6.1.
03.0 LÄKEMEDELSFORM
Injektionsvätska, lösning för subkutan användning och för hemodialys.
04.0 KLINISK INFORMATION
04.1 Terapeutiska indikationer
- Profylax av djup ventrombos (DVT) vid allmän kirurgi och ortopedisk kirurgi.
- Behandling av djup ventrombos.
- Förebyggande av koagulation under hemodialys.
- Behandling av instabil angina och icke-Q-hjärtinfarkt.
04.2 Dosering och administreringssätt
Dosering
Särskild uppmärksamhet bör ägnas doseringsinstruktionerna, specifika för olika märken av lågmolekylär heparin, eftersom olika mätsystem används för varje heparin med låg molekylvikt för att uttrycka doserna (enheter eller mg).
Därför ska nadroparin inte användas omväxlande med andra lågmolekylära hepariner under behandlingen.
Profylax av djup ventrombos
Subkutan administrering
I allmän kirurgi:
En subkutan injektion av 0,3 ml (2850 IE antiXa) 2-4 timmar före operationen. Därefter var 24: e timme i minst 7 dagar; i alla fall måste profylax fortsättas under riskperioden och åtminstone tills patienten återupptar ambulationen.
Vid ortopedisk kirurgi:
Doseringen, som består av en "subkutan injektion en gång per dag, måste justeras enligt patientens vikt enligt tabellen nedan.
En "preoperativ injektion av 38 IE antiXa / kg 12 timmar före" operationen, en postoperativ 12 timmar efter slutet av "operationen, sedan en" daglig injektion fram till den tredje postoperativa dagen ingår; 57 I.U. antiXa / kg / dag från och med den fjärde postoperativa dagen.
Behandlingstiden är minst 10 dagar; i alla fall måste profylax fortsättas under hela riskperioden och åtminstone tills patienten fortsätter att gå.
Som exempel och beroende på patientens vikt är doseringarna som ska administreras enligt följande:
0,1 ml nadroparin innehåller 950 I.E. antiXa
Behandling av djup ventrombos
Subkutan administrering
En injektion var 12: e timme i 10 dagar i en dos av cirka 92,7 IE antiXa / kg.
Som exempel och beroende på patientens vikt är doseringarna som ska administreras enligt följande:
Om det inte finns några kontraindikationer, starta oral antikoagulantbehandling så snart som möjligt.
Nadroparinbehandling ska inte avbrytas förrän det nödvändiga internationella normaliserade förhållandet (INR) har uppnåtts.
Trombocytantalet bör övervakas under hela behandlingen med nadroparin (se avsnitt 4.4 Varningar och försiktighet vid användning).
Förebyggande av koagulation under hemodialys
Intravaskulär administrering
För att förhindra koagulering under extrakorporeal cirkulation under hemodialys.
Hos de patienter som inte har en blödningsrisk och för en session som varar mindre än eller lika med 4 timmar, övar i början av sessionen en injektion, i arteriell åtkomst, av en enda dos, utvärderad enligt patientens vikt i storleksordningen 64,6 IE antiXa / kg.
Som exempel och beroende på patientens vikt:
Vid behov kommer dosen att justeras från fall till fall enligt patienten och de tekniska villkoren för dialys.
För patienter med ökad risk för blödning kan dialyspass utföras med en dos reducerad till hälften.
För sessioner som varar mer än 4 timmar är det möjligt att administrera ytterligare en reducerad dos.
Vid efterföljande dialyspass kan dosen om nödvändigt justeras baserat på effekten som observerades initialt.
Patienterna bör övervakas noggrant under dialyspasset för tecken på blödning eller koagulation i dialyskretsen.
Behandling av instabil angina och icke-Q-hjärtinfarkt
Subkutan administrering
Nadroparin ska administreras subkutant två gånger dagligen (var 12: e timme). Behandlingstiden är i allmänhet 6 dagar. I kliniska studier på patienter med instabil angina och icke-Q-hjärtinfarkt administrerades nadroparin i kombination med acetylsalicylsyra i en maximal dos av 325 mg per dag.
Initialdosen ska administreras som en intravenös bolus på 86 I.E. antiXa / kg, följt av subkutana injektioner av 86 I.U. antiXa / kg.
Dosen bör baseras på patientens vikt.
Som exempel och beroende på patientens vikt är doserna som ska administreras enligt följande:
Pediatrisk population
Nadroparin rekommenderas inte till barn och ungdomar eftersom det inte finns tillräckliga säkerhets- och effektdata för att fastställa dosen hos patienter under 18 år.
Pensionärer
Ingen dosjustering är nödvändig hos äldre om inte njurfunktionen är nedsatt.Det rekommenderas att njurfunktionen kontrolleras innan behandling påbörjas (se Nedsatt njurfunktion och avsnitt 5.2 Farmakokinetiska egenskaper nedan).
Njursvikt
Profylax av djup ventrombos
Ingen dosreduktion krävs hos patienter med lätt nedsatt njurfunktion (kreatininclearance större än eller lika med 50 ml / min). "Både måttlig och svår njurinsufficiens är associerad med" ökad nadroparinexponering. Dessa patienter har en ökad risk för tromboembolism och blödning. Hos patienter med måttlig njurinsufficiens (kreatininclearance större än eller lika med 30 ml / min och mindre än 50 ml / min) ska dosen anses lämplig av läkaren, med hänsyn tagen till individuella blödnings- och tromboemboliska riskfaktorer. grader från 25% till 33% (se avsnitt 4.4 Varningar och försiktighet vid användning och 5.2 Farmakokinetiska egenskaper).
Dosen bör minskas från 25% till 33% hos patienter med svårt nedsatt njurfunktion (kreatininclearance mindre än 30 ml / min) (se avsnitt 4.4 Varningar och försiktighetsåtgärder vid användning och 5.2 Farmakokinetiska egenskaper).
Behandling av djup ventrombos, instabil angina och icke-Q-hjärtinfarkt
Hos patienter med lätt nedsatt njurfunktion (kreatininclearance ≥50 ml / min) som får nadroparin för behandling av dessa tillstånd krävs ingen dosreduktion.
"Både måttlig och svår njurinsufficiens är associerad med" ökad nadroparinexponering. Dessa patienter har en ökad risk för tromboembolism och blödning.
Hos patienter med måttlig njurinsufficiens (kreatininclearance större än eller lika med 30 ml / min och mindre än 50 ml / min) ska dosen anses lämplig av läkaren, med hänsyn tagen till individuella blödnings- och tromboemboliska riskfaktorer. grader från 25% till 33% (se avsnitt 4.4 Varningar och försiktighet vid användning och 5.2 Farmakokinetiska egenskaper).
Nadroparin är kontraindicerat hos patienter med allvarligt nedsatt njurfunktion (se avsnitt 4.4 Varningar och försiktighetsåtgärder vid användning och 5.2 Farmakokinetiska egenskaper).
Leverinsufficiens
Inga studier har utförts på patienter med leverinsufficiens.
Administreringssätt
Nadroparin ska inte ges intramuskulärt.
Administrering av nadroparin nära spinal / epidural anestesi eller ländryggsinjektion bör följa specifika rekommendationer (se avsnitt 4.4 Varningar och försiktighetsåtgärder vid användning).
Subkutan injektionsteknik
När nadroparin administreras subkutant ska injektion ges i det anterolaterala eller posterolaterala bukbältet, alternerande vänster och höger. Låret kan vara ett alternativt ställe.
För att undvika läckage av lösning när du använder förfyllda sprutor, ska du inte slänga ut luftbubblan från sprutan innan du injicerar.
Nålen måste införas helt, vinkelrätt och inte tangentiellt, i tjockleken på en hudveck mellan tummen och operatörens pekfinger.
Vikningen måste bibehållas under injektionens varaktighet.I slutet av injektionen ska du inte gnugga huden utan utöva ett måttligt tryck på platsen.
I fallet med en dos anpassad till patientens vikt, justeras volymen som ska administreras genom att föra kolven till önskat skår medan sprutan hålls i vertikalt läge.
04.3 Kontraindikationer
Nadroparin är kontraindicerat vid:
- överkänslighet mot den aktiva substansen eller mot något hjälpämne som anges i avsnitt 6.1
- historia av trombocytopeni med nadroparin (se även avsnitt 4.4 Varningar och försiktighet vid användning)
- aktiv blödning eller ökad blödningsrisk relaterad till hemostasstörningar, med undantag för spridd intravaskulär koagulation som inte induceras av heparin
- organiska skador med risk för blödning (magsår i aktiv fas, retinopatier, hemorragiskt syndrom)
- hemorragiska cerebrovaskulära olyckor
- akut infektiös endokardit
- svår njurinsufficiens (undanröjning av kreatinin djup ventrombos, instabil angina och icke-Q-hjärtinfarkt
- allvarliga nefropatier och pankreopatier, svår arteriell hypertoni, allvarligt kranioencefaliskt trauma under den postoperativa perioden
- Flerdosflaskan innehåller bensylalkohol och bör därför inte användas till barn under tre år
- loko-regional anestesi för elektiva kirurgiska ingrepp är kontraindicerad hos patienter som får heparin med låg molekylvikt för terapeutiskt bruk.
04.4 Särskilda varningar och lämpliga försiktighetsåtgärder vid användning
Trombocytopeni induceras av heparin
På grund av risken för heparininducerad trombocytopeni bör antalet trombocyter övervakas under hela behandlingen med nadroparin.
Det har förekommit sällsynta rapporter om trombocytopeni, ibland allvarliga, som kan vara associerade med arteriell eller venös trombos. Denna diagnos bör övervägas i följande situationer:
- trombocytopeni
- någon signifikant minskning av trombocytnivån (30-50% jämfört med baslinjen)
- förvärrad initial trombos under behandlingen
- trombos som uppstår under behandlingen
- spridd intravaskulär koagulation.
I sådana fall bör behandlingen med nadroparin avbrytas.
Dessa effekter är förmodligen av immunallergisk natur och har vid en första behandling rapporterats huvudsakligen mellan den 5: e och 21: e behandlingsdagen, men kan också uppträda mycket tidigare vid trombocytopeni som orsakats av heparin .
Om en historia av trombocytopeni inträffar vid behandling med heparin (både standard och låg molekylvikt), kan behandling med nadroparin övervägas om det behövs. I sådana fall bör noggrann klinisk övervakning och kontroll av trombocytantalet göras minst en gång om dagen. Om trombocytopeni inträffar ska behandlingen omedelbart avbrytas.
När trombocytopeni inträffar med användning av heparin (standard eller låg molekylvikt), bör ersättning med ett antitrombotiskt läkemedel av annan klass övervägas.
Om detta inte är möjligt, men heparinadministrering fortfarande krävs, kan substitution med ett annat lågmolekylärt heparin övervägas.I sådana fall bör övervakning av trombocytantal utföras minst dagligen och behandling ska utföras. Avbrytas så snart som möjligt, som fall av initial trombocytopeni som fortsatte efter utbyte har rapporterats (se avsnitt 4.3 Kontraindikationer).
Trombocytaggregationstest in vitro de är av begränsat värde vid diagnos av heparininducerad trombocytopeni.
Nadroparin ska administreras med försiktighet i följande situationer, vilket kan vara förknippat med en ökad risk för blödning:
- leverinsufficiens
- svår arteriell hypertoni
- klinisk historia av magsår eller andra organiska skador med risk för blödning
- kärlsjukdomar i chorioretina
- under den postoperativa perioden efter hjärn-, ryggmärgs- eller ögonoperation och vid huvudskador
Njursvikt
Det är känt att Nadroparin huvudsakligen utsöndras via njurarna, vilket resulterar i ökad nadroparinexponering för patienter med nedsatt njurfunktion (se avsnitt 5.2 Farmakokinetiska egenskaper - Njurinsufficiens). Patienter med nedsatt njurfunktion har ökad risk för blödning och bör behandlas med försiktighet.
Varje dosreduktion hos patienter med kreatininclearance mellan 30 ml / min och 50 ml / min bör baseras på klinikerens kliniska bedömning av den individuella blödningsrisken mot tromboembolismrisk (se avsnitt 4.2 Dosering och administreringssätt).
Pensionärer
Det rekommenderas att kontrollera njurfunktionen innan behandling påbörjas (se avsnitt 4.3 Kontraindikationer).
Hyperkalemi
Heparin kan undertrycka binjurssekretionen av aldosteron vilket leder till hyperkalemi, särskilt hos patienter med förhöjda plasmakaliumnivåer eller med risk för ökade plasmakaliumnivåer, såsom patienter med diabetes mellitus, kroniskt njursvikt, pre -metabolisk acidos. -Existerande eller tar läkemedel som kan orsaka hyperkalemi (t.ex. angiotensinkonverterande enzymhämmare (ACE-hämmare), icke-steroida antiinflammatoriska läkemedel (NSAID)).
Risken för hyperkalemi tycks öka i förhållande till behandlingstiden, men är i allmänhet reversibel.
Hos patienter med risk bör plasmakalium övervakas.
Spinal / epidural bedövning, ländryggen punktering och samtidig medicinering
Hos patienter som genomgår spinal- eller epiduralanestesi kan användning av lågmolekylär heparin sällan associeras med hematom, vilket kan leda till långvarig eller permanent förlamning av underbenen.
Risken för spinal / epidural hematom ökar genom användning av inhemska epiduralkateter eller vid samtidig användning av andra läkemedel som kan påverka hemostas, såsom icke-steroida antiinflammatoriska läkemedel (NSAID), trombocytaggregationshämmare eller andra. Antikoagulantia. Risken ökar också av trauma eller av upprepade epidurala eller lumbala punkteringar.
Därför måste samtidig användning av ett neuraxialt block och antikoaguleringsterapi avgöras efter att den individuella nytta / riskbalansen noggrant har fastställts i följande situationer:
- hos patienter som redan behandlats med antikoagulantia måste fördelarna med ett neuraxialt block noggrant vägas mot riskerna.
- hos patienter där elektiv kirurgi med neuraxialt block är planerat måste fördelarna med antikoagulantia -behandling noggrant vägas mot riskerna.
För patienter som genomgår lumbal spinal punktering, spinalanestesi eller epiduralbedövning måste det gå 12 timmar mellan injektionen av nadroparin i profylaktiska doser och införandet eller avlägsnandet av katetern eller ryggmärgen / epiduralnålen och minst 24 timmar vid nadroparin injektion vid behandlingsdoser med hänsyn tagen till produktegenskaper och patientprofil.
Längre tidsintervall bör övervägas för patienter med nedsatt njurfunktion. Nästa dos ska inte ges förrän minst 4 timmar har gått.
Återadministrering av nadroparin bör fördröjas tills det kirurgiska ingreppet har slutförts.
Patienter bör övervakas ofta för tecken och symtom på neurologiska förändringar, såsom smärta i nedre delen av ryggen, sensoriska och motoriska underskott i nedre extremiteterna (domningar och svaghet), tarm- och / eller urinblåsdysfunktion. Om neurologisk försämring noteras krävs akut behandling. Vårdpersonal bör vara beredd att upptäcka sådana tecken och symtom. Patienter bör rådas att omedelbart meddela en läkare eller sjukvårdspersonal om något av ovanstående symtom uppstår.
Om man misstänker tecken eller symtom på epidural eller spinal hematom bör en diagnos och behandling som inkluderar dekompression av ryggmärgen göras snarast.
Om signifikant eller uppenbar blödning har inträffat under placeringen av den epidurala katetern, bör en noggrann nytta / riskbedömning göras innan behandling med heparin påbörjas / återupptas.
Hudnekros
Hudnekros har rapporterats mycket sällan. Det föregås av infiltrerad eller smärtsam purpura eller erytematösa plack, med eller utan allmänna symptom. I sådana fall måste behandlingen avbrytas omedelbart.
Latexallergi
Nålkåpan på den förfyllda sprutan kan innehålla naturligt latexgummi som kan orsaka allergiska reaktioner hos latexkänsliga individer.
04.5 Interaktioner med andra läkemedel och andra former av interaktion
Nadroparin ska administreras med försiktighet till patienter som får orala antikoagulantia, systemiska (gluko-) kortikosteroider och dextrans. När man påbörjar oral antikoagulantia -behandling hos patienter som får nadroparin, ska behandlingen med nadroparin fortsätta tills International Normalized Ratio (INR) har stabiliserats till önskat värde.
Salicylater, icke-steroida antiinflammatoriska läkemedel och blodplättsaggregat
Vid profylax eller behandling av venösa tromboemboliska störningar och vid förebyggande av koagulation under hemodialys, rekommenderas inte samtidig användning av aspirin, andra salicylater, NSAID och trombocytantagande medel, eftersom dessa läkemedel kan öka risken för blödning. När sådana kombinationer inte kan undvikas rekommenderas noggrann övervakning av kliniska och biologiska parametrar.
I kliniska prövningar för behandling av instabil angina och icke-Q-hjärtinfarkt administrerades nadroparin i kombination med aspirin upp till en maximal dos av 325 mg per dag acetylsalicylsyra (se avsnitt 4.2 Dosering och administreringssätt och 4.4 Varningar och försiktighetsåtgärder vid användning).
Föreningar rekommenderas inte
- Acetylsalicylsyra och andra salicylater (i allmänhet)
Ökad risk för blödning (hämning av trombocytfunktionen och aggression av gastroduodenal slemhinna av salicylater).
Använd andra ämnen för smärtstillande eller febernedsättande effekt.
Vid behandling av instabil angina och icke-Q-hjärtinfarkt ska nadroparin administreras i kombination med acetylsalicylsyra i en maximal dos av 325 mg / dag (se avsnitt 4.2 Dosering och administreringssätt och 4.4 Varningar och försiktighet vid användning ).
- NSAID (i allmänhet)
Ökad risk för blödning (hämning av trombocytfunktionen och aggression av gastroduodenal slemhinna av icke-steroida antiinflammatoriska läkemedel).
Om föreningen inte kan undvikas, inled noggrann klinisk och biologisk övervakning.
- Tiklopidin: ökad risk för blödning (hämning av trombocytfunktionen av tiklopidin).
Sambandet med höga doser heparin rekommenderas inte: sambandet med låga doser heparin (förebyggande heparinbehandling) kräver noggrann klinisk och biologisk övervakning.
- Andra blodplättshämmande medel (klopidogrel, dipyridamol, sulfinpyrazon, etc.): ökad risk för blödning (hämning av trombocytfunktionen).
Föreningar som kräver försiktighetsåtgärder vid användning:
- Orala antikoagulantia
Förstärkning av antikoagulantia. Heparin snedvrider protrombinhastigheten.
Vid ersättning av heparin med orala antikoagulantia:
- förstärka klinisk och biologisk övervakning (snabb tid uttryckt i INR).
- för att kontrollera effekten av orala antikoagulantia, ta provet före administrering av heparin, om detta är diskontinuerligt eller använd helst ett reagens som inte är känsligt för heparin. På grund av den latens som krävs för att det orala antikoagulanten ska vara fullt effektiv bör heparinbehandlingen fortsätta tills INR har stabiliserats inom det terapeutiska intervallet (mellan 2 och 3).
- Glukokortikoider (allmän väg)
Förvärring av den hemorragiska risk som är typisk för glukokortikoidbehandling (magslemhinna, vaskulär bräcklighet), vid höga doser eller vid långvarig behandling i mer än tio dagar.
Föreningen måste vara motiverad; förbättra klinisk övervakning.
- Dextran (injicering)
Ökad risk för blödning (hämning av trombocytfunktionen).
Justera dosen av heparin för att inte överstiga en hypokoagulering som är större än 1,5 gånger referensvärdet, under kombinationen och efter suspension av dextran.
- Vid samtidig administrering av askorbinsyra, antihistaminer, digitalis, IV -penicilliner, tetracykliner eller fenotiaziner kan en hämning av läkemedlets aktivitet inträffa.
04.6 Graviditet och amning
Graviditet
Djurstudier har inte visat någon teratogen eller fetotoxisk aktivitet, men det finns endast begränsade kliniska data avseende passering av nadroparin genom moderkakan hos gravida kvinnor. Därför rekommenderas inte användning av nadroparin under dräktighet, såvida inte de terapeutiska fördelarna överväger de möjliga risker.
Matdags
Information om utsöndring av nadroparin i bröstmjölk är begränsad. Nuvarande kunskap tyder på att på grund av molekylstorleken hos hepariner med låg molekylvikt och gastrointestinal inaktivering är passage till bröstmjölk och oral absorption genom amning försumbar. mödrar som får nadroparin bör avrådas från att amma.
Fertilitet
Det finns inga kliniska studier av effekten av nadroparin på fertiliteten.
04.7 Effekter på förmågan att framföra fordon och använda maskiner
Inga studier har gjorts om förmågan att framföra fordon och använda maskiner.
04.8 Biverkningar
Biverkningar listas nedan efter system, organ, klass och frekvens.
Biverkningar klassificeras enligt systemorganklass och enligt frekvenskonventionen: mycket vanligt ≥1 / 10, vanligt ≥1 / 100 till
* I vissa fall kan du märka uppkomsten av fasta knölar som inte är ett tecken på en heparin -encykst. Dessa knölar försvinner i allmänhet efter några dagar.
1 Kalsinos är vanligare hos patienter med onormal kalciumfosfatproduktion, liksom i vissa fall av kroniskt njursvikt.
Rapportering av misstänkta biverkningar
Rapportering av misstänkta biverkningar som uppstår efter godkännande av läkemedlet är viktigt eftersom det möjliggör kontinuerlig övervakning av nytta / riskbalansen för läkemedlet.Hälso- och sjukvårdspersonal uppmanas att rapportera alla misstänkta biverkningar via www.agenziafarmaco.gov. It / det / ansvarig
04.9 Överdosering
Symtom och tecken
Den mest uppenbara kliniska manifestationen av överdosering, både subkutan och intravenös, är blödning, i detta fall bör antalet blodplättar tas och andra koagulationsparametrar mätas.
Mindre blödningar kräver sällan specifik behandling och det är vanligtvis tillräckligt för att minska eller fördröja efterföljande doser av nadroparin.
Behandling
Endast i allvarliga fall bör man överväga att använda protaminsulfat, vilket i hög grad neutraliserar den antikoagulerande effekten av nadroparin, även om en del av antiXa -aktiviteten kvarstår.
0,6 ml protaminsulfat neutraliserar cirka 950 I.U. antiXa av nadroparin. För att mängden protamin ska injiceras måste den tid som förflutit sedan heparininjektionen beaktas och vid behov måste en minskning av protamindosen göras.
05.0 FARMAKOLOGISKA EGENSKAPER
05.1 Farmakodynamiska egenskaper
Farmakoterapeutisk grupp: Antitrombotika - heparinderivat
ATC -kod: B01AB06
Handlingsmekanism
Nadroparin är ett heparin med låg molekylvikt som erhålls genom depolymerisering av standardheparin, det är en glykosaminoglykan med en genomsnittlig molekylvikt på cirka 4300 dalton.
Nadroparin uppvisar en hög bindningsaffinitet till plasma anti-trombin III (ATIII) protein. Denna bindning leder till en acceleration av hämningen av faktor Xa, vilket bidrar till den höga antitrombotiska potentialen för nadroparin.
Andra mekanismer som bidrar till den antitrombotiska aktiviteten hos nadroparin inkluderar stimulering av vävnadsfaktor TFP1-hämmare, aktivering av fibrinolys genom direkt frisättning av vävnadsplasminogenaktivator från endotelceller och modifiering av blödningsparametrar (minskning av blodviskositet och ökad fluiditet av trombocyter och granulocyt membran).
Farmakodynamiska effekter
Nadroparin har ett högt antiXa / anti-IIa aktivitetsförhållande. Detta resulterar i en snabb och långvarig "antitrombotisk aktivitet över tid.
05.2 Farmakokinetiska egenskaper
De farmakokinetiska egenskaperna för nadroparin bestämdes på grundval av dess biologiska aktivitet, dvs genom att utvärdera anti-faktor Xa-aktiviteten.
Absorption
Topp anti-Xa-aktivitet (Cmax) uppnås cirka 3-5 timmar (tmax) efter subkutan administrering.
Biotillgängligheten är nästan fullständig (cirka 88%).
Efter intravenös injektion uppnås den maximala plasmanivån mot Xa inom mindre än 10 minuter och halveringstiden är cirka 2 timmar.
Eliminering
Eliminationshalveringstiden efter subkutan injektion är cirka 3,5 timmar.
AntiXa -aktivitet kan dock påvisas i minst 18 timmar efter en injektion av 1900 IE antiXa.
Särskilda populationer
Pensionärer
Njurfunktionen minskar i allmänhet med åldern så att elimineringen går långsammare hos äldre (se avsnitt 5.2 Farmakokinetiska egenskaper: njurinsufficiens nedan). Möjligheten till njurinsufficiens i denna åldersgrupp och dosen bör justeras i enlighet med detta (se avsnitt 4.4 Varningar och försiktighet) för användning).
Njursvikt
I en klinisk studie om farmakokinetiken för nadroparin administrerat intravenöst hos patienter med varierande grad av njurinsufficiens, hittades en korrelation mellan nadroparinclearance och kreatininclearance. I jämförelse med friska frivilliga ökade den genomsnittliga AUC- och eliminationshalveringstiden för patienter med måttligt nedsatt njurfunktion (kreatininclearance 36-43 ml / min) med 52 respektive 39%.
Hos dessa patienter minskade den genomsnittliga plasmaclearance för nadroparin med 63% från normalt. En stor interindividuell variation observerades i studien. Hos personer med allvarligt nedsatt njurfunktion (kreatininclearance 10-20 ml / min) ökade både genomsnittlig AUC och halveringstid med 95% respektive 112% i jämförelse med friska frivilliga Plasmaclearance hos patienter med svårt nedsatt njurfunktion minskade med 50% av det som observerades hos patienter med normal njurfunktion.
Data från tidigare genomförda studier indikerar att en liten ackumulering av nadroparin kan uppstå hos patienter med lätt till måttligt nedsatt njurfunktion (kreatininclearance lika med eller större än 30 ml / min och mindre än 60 ml / min), hos patienter som får nadroparin för behandling av tromboemboliska störningar, instabil angina och icke-Q-hjärtinfarkt för vilka dosreduktion kan övervägas (se avsnitt 4.2 Dosering och administreringssätt och 4.4 Varningar och försiktighet vid användning).
Hos patienter med allvarligt nedsatt njurfunktion (kreatininclearance 3 till 6 ml / min) som genomgick hemodialys ökade både genomsnittlig AUC och halveringstid med 62 respektive 65%, jämfört med friska frivilliga. Plasmaclearance hos hemodialyspatienter med svår njurinsufficiens minskade med 67% jämfört med det som observerades hos patienter med normal njurfunktion (se avsnitt 4.2 Dosering och administreringssätt och 4.4 Varningar och försiktighet vid användning).
05.3 Prekliniska säkerhetsdata
Icke-kliniska data avslöjar ingen särskild fara för människor baserat på konventionella studier av säkerhetsfarmakologi, toxicitet vid upprepade doser, gentoxicitet, cancerframkallande potential och reproduktionstoxicitet och utvecklingstoxicitet.
06.0 LÄKEMEDELSINFORMATION
06.1 Hjälpämnen
Kalciumhydroxidlösning eller utspädd saltsyra, vatten för injektionsvätskor.
06.2 Oförenlighet
Blanda inte med andra preparat.
06.3 Giltighetstid
3 år
06.4 Särskilda förvaringsanvisningar
Förvaras vid högst 25 ° C.
06.5 Förpackningens innehåll och förpackningens innehåll
FRAXIPARINA 2.850 I.U. antiXa / 0,3 ml injektionsvätska, lösning: 6 förfyllda sprutor av typ I färglöst glas
FRAXIPARINA 3800 I.U. antiXa / 0,4 ml injektionsvätska, lösning: 6 förfyllda graderade typ I färglösa glassprutor
FRAXIPARINA 5700 I.E. antiXa / 0,6 ml injektionsvätska, lösning: 10 förfyllda graderade färglösa glassprutor typ I
FRAXIPARINA 7600 I.U. antiXa / 0,8 ml injektionsvätska, lösning: 10 förfyllda graderade färglösa glassprutor typ I
FRAXIPARINA 9.500 I.U. antiXa / 1 ml injektionsvätska, lösning: 10 förfyllda graderade färglösa färgsprutor av typ I
06.6 Anvisningar för användning och hantering
Hantering: se avsnitt 4.2 Dosering och administreringssätt.
Nadroparin injektionsvätska, lösning bör inspekteras visuellt före användning för att se om det finns partiklar eller färgförändringar.
Sprutor är endast för engångsbruk och allt oanvänt innehåll i varje spruta ska kasseras. Lösningar ska inte blandas med andra preparat eller administreras på nytt.
ANVÄNDNING AV SÄKERHETSENHETEN
Efter injektionen, förbered säkerhetsanordningen för FRAXIPARINA -sprutan.
Håll spruthylsan med ena handen, dra fast i sprutringen med den andra handen för att låsa upp hylsan och tryck tills den klickar på plats. Nålen som används är nu helt skyddad.
Frys inte. Förvara inte i kylskåp eftersom kalla injektioner kan vara smärtsamma.
Oanvänd medicin och avfall från detta läkemedel måste kasseras i enlighet med lokala föreskrifter.
07.0 INNEHAVARE AV GODKÄNNANDE FÖR FÖRSÄLJNING
Aspen Pharma Trading Limited 3016 Lake Drive
Citywest Business Campus
Dublin 24
Irland
08.0 NUMMER FÖR FÖRSÄLJNINGSTILLSTÅND
6 förfyllda sprutor 2850 I.U. antiXa / 0,3 ml - AIC 026736064
6 förfyllda sprutor 3800 IE antiXa / 0,4 ml - AIC 026736076
10 förfyllda sprutor 5 700 IU antiXa / 0,6 ml - AIC 026736088
10 förfyllda sprutor 7600 IE antiXa / 0,8 ml - AIC 026736090
10 förfyllda sprutor 9 500 IU antiXa / 1 ml - AIC 026736102
09.0 DATUM FÖR FÖRSTA GODKÄNNANDE ELLER FÖRNYELSE AV GODKÄNNANDET
Första tillstånd: 1 februari 1993 / Förnyelse: februari 2008
10.0 DATUM FÖR REVISION AV TEXTEN
Juni 2017























-e-ruscogenina.jpg)



