Aktiva ingredienser: Metotrexat
Reumaflex 50 mg / ml injektionsvätska, lösning, förfylld spruta
Varför används Reumaflex? Vad är det för?
Reumaflex innehåller metotrexat som aktiv ingrediens. Metotrexat är ett ämne med följande egenskaper:
- det stör tillväxten av vissa celler i kroppen som fortplantar sig snabbt
- minskar immunsystemets aktivitet (kroppens försvarsmekanism)
- det har antiinflammatoriska effekter
Reumaflex är indicerat för behandling av:
- aktiv reumatoid artrit hos vuxna patienter;
- polyartritiska former av svår juvenil idiopatisk artrit i den aktiva fasen, med otillräckligt svar på icke-steroida antiinflammatoriska läkemedel (NSAID);
- svår, återfallande och handikappande psoriasis som inte svarar tillräckligt på andra former av terapi som fototerapi, PUVA och retinoider och svår psoriasisartrit hos vuxna patienter.
- mild till måttlig Crohns sjukdom hos vuxna patienter, i de fall adekvat behandling med andra läkemedel inte är möjlig.
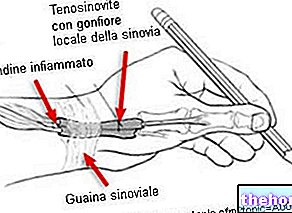
Reumatoid artrit (RA) är en kronisk bindvävssjukdom som kännetecknas av inflammation i synovialmembranen (membran i lederna). Dessa membran producerar en vätska som fungerar som ett smörjmedel för många leder. Inflammation orsakar förtjockning av dessa membran och svullnad i lederna.
Juvenil idiopatisk artrit påverkar barn och ungdomar under 16 år. Polyartritformer är de som påverkar 5 eller fler leder inom de första sex månaderna av sjukdomsuppkomsten.
Psoriasisartrit är en typ av artrit med psoriasisskador på hud och naglar, särskilt i lederna i fingrar och tår
Psoriasis är en vanlig kronisk hudsjukdom som kännetecknas av röda fläckar kantade med torra, tjocka, silverfärgade fjäll som är svåra att skala av.
Reumaflex har visat sig kunna modifiera och bromsa utvecklingen av dessa sjukdomar.
Crohns sjukdom är en typ av inflammatorisk tarmsjukdom som kan påverka någon del av mag -tarmkanalen som orsakar symtom som buksmärtor, diarré, kräkningar eller viktminskning.
Kontraindikationer När Reumaflex inte ska användas
Ta inte Reumaflex
- om du är allergisk mot metotrexat eller något annat innehållsämne i detta läkemedel
- om du har svår lever- eller njursjukdom eller blodsjukdom.
- om du regelbundet dricker stora mängder alkoholhaltiga drycker.
- om du har en allvarlig infektion, t.ex. tuberkulos, HIV eller andra immunsviktssyndrom.
- om du lider av munsår eller magsår eller tarmsår.
- om du är gravid eller ammar.
- om du vaccineras samtidigt med levande vacciner.
Försiktighetsåtgärder vid användning Vad du behöver veta innan du tar Reumaflex
Tala med din läkare eller apotekspersonal innan du tar Reumaflex om:
- är äldre eller i allmänhet känner sig sjuk och svag.
- har leverfunktionsproblem.
- lider av uttorkning (förlust av vatten).
Efterföljande undersökningar och rekommenderade säkerhetsåtgärder
Även om Reumaflex ges i en låg dos kan allvarliga biverkningar uppstå. För att identifiera dem omedelbart måste läkaren utföra kontroller och laboratorietester.
Före terapin
Innan behandlingen påbörjas bör ett blodprov tas för att kontrollera att det finns tillräckligt med blodceller och tester för att kontrollera leverns och njurs funktion och mängden serumalbumin (ett blodprotein). Din läkare kommer också att se till att du inte lider av tuberkulos (en infektionssjukdom som är förknippad med små klumpar i den drabbade vävnaden) genom att ta en röntgen på bröstet.
Under terapin
Minst en gång i månaden de första sex månaderna och minst var tredje månad därefter måste följande test utföras:
- Undersökning av mun och svalg för att verifiera att det inte finns några förändringar i slemhinnan
- Blodprov
- Kontroll av leverfunktionen
- Kontroll av njurfunktionen
- Kontroll av andningsorganen och vid behov lungfunktionstester
Metotrexat kan påverka immunsystemet och vaccinationsresultaten. Det kan också påverka resultatet av immunanalyser. Inaktiva kroniska infektioner som herpes zoster [Saint Anthony's fire], tuberkulos, hepatit B eller C. kan blossa upp. Du bör inte vaccineras med levande vacciner när du tar Reumaflex.
Strålningsdermatit och solbränna kan återkomma under metotrexatbehandling (återkallningsreaktion). Psoriasisskador kan förvärras efter samtidig användning av ultraviolett strålning och metotrexat.
Förstorade lymfkörtlar (lymfom) kan uppträda och behandlingen måste därför avbrytas.
Diarré kan vara en toxisk effekt av Reumaflex och kräver att behandlingen avbryts. Om du lider av diarré, tala med din läkare.
Encefalopati (hjärnsjukdom) och leukoencefalopati (särskild hjärtsjukdom i hjärnan) har inträffat hos patienter med tumörer som får metotrexat, och det kan inte uteslutas att de kan uppstå under metotrexatbehandling vid andra sjukdomar.
Interaktioner Vilka läkemedel eller livsmedel kan ändra effekten av Reumaflex
Tala om för din läkare eller apotekspersonal om du tar, nyligen har tagit eller kan tänkas ta andra läkemedel.
Behandlingseffekten kan ändras om Reumaflex administreras samtidigt med andra läkemedel såsom:
- Läkemedel som är skadliga för levern eller blodkropparna, t.ex. leflunomid
- Antibiotika (läkemedel för att förebygga / bekämpa vissa infektioner) såsom: tetracykliner, kloramfenikol och icke-absorberbara bredspektrumantibiotika, penicilliner, glykopeptider, sulfonamider (svavelmedicin som förebygger / bekämpar vissa infektioner), ciprofloxacin och cefalotin
- Icke-steroida eller salicylerade antiinflammatoriska läkemedel (smärtstillande och / eller antiinflammatoriska)
- Probenecid (giktmedicin)
- Svaga organiska syror som loop -diuretika eller vissa läkemedel som används för behandling av smärta och inflammatoriska sjukdomar (t.ex. acetylsalicylsyra, dikoflenak och ibuprofen) och pyrazolonderivat (t.ex. metamizol för smärtbehandling)
- Läkemedel som kan ha oönskade effekter på benmärgen, t.ex. trimetoprimsulfametoxazol (ett antibiotikum) och pyrimetamin
- Sulfasalazin (en antireumatisk)
- Azatioprin (ett immunsuppressivt medel som ibland används vid svåra former av reumatoid artrit)
- Merkaptopurin (en cytostatika)
- Retinoider (medicin mot psoriasis och andra dermatologiska sjukdomar)
- Teofyllin (medicin mot bronkial astma och andra lungsjukdomar)
- Protonpumpshämmare (läkemedel mot magbesvär)
- Hypoglykemi (läkemedel som används för att sänka blodsockret)
Vitaminkomplex som innehåller folsyra kan försämra effekten av behandlingen och bör endast tas under medicinsk övervakning.
Vaccinationer med levande vacciner bör undvikas.
Användning av Reumaflex tillsammans med mat, dryck och alkohol
Under behandlingen med Reumaflex bör följande undvikas: alkoholhaltiga drycker, stora mängder kaffe, läsk som innehåller koffein och svart te.
Varningar Det är viktigt att veta att:
Graviditet, amning och fertilitet
Om du är gravid eller ammar, tror att du kan vara gravid eller planerar att skaffa barn, rådfråga din läkare eller apotekspersonal innan du använder detta läkemedel.
Reumaflex ska inte användas under graviditet, eftersom det finns risk för fosterskador och missfall. Män och kvinnor bör använda en effektiv preventivmetod under behandlingen och i sex månader efter avslutad behandling med Reumaflex.
Hos kvinnor i fertil ålder bör en pågående graviditet säkert uteslutas genom att genomföra ett graviditetstest innan behandlingen påbörjas.
Eftersom metotrexat kan vara genotoxiskt rekommenderas alla kvinnor som vill bli gravida att konsultera ett genetiskt rådgivningscenter eventuellt före behandlingen, och män rekommenderas att fråga om möjligheter till spermier innan de börjar behandlingen.
Amning ska avbrytas före och under behandling med Reumaflex.
Köra och använda maskiner
Behandling med Reumaflex kan orsaka biverkningar som påverkar centrala nervsystemet, såsom trötthet och yrsel. Därför kan förmågan att köra fordon och / eller använda maskiner i vissa fall försämras. Om du känner dig trött eller sömnig ska du inte köra bil eller använda maskiner.
Viktig information om några av ingredienserna i Reumaflex
Detta läkemedel innehåller mindre än 1 mmol natrium (23 mg) per dos, dvs det är i huvudsak "natriumfritt".
Dos, metod och administreringstid Hur man använder Reumaflex: Dosering
Läkaren bestämmer dosen som ska anpassas till den enskilda patienten. I allmänhet märks effekterna av behandlingen efter 4-8 veckor.
Reumaflex ges av eller under överinseende av en läkare eller vårdpersonal som en injektion endast en gång i veckan. Tillsammans med din läkare, bestäm vilken dag i veckan du vill ha den veckovisa injektionen.
Reumaflex kan injiceras intramuskulärt (i en muskel), intravenöst (i en ven) eller subkutant (under huden).
På grund av den begränsade tillgängligheten av data om intravenös administrering hos barn och ungdomar ska produkten endast injiceras subkutant eller intramuskulärt hos dessa patienter.
Läkaren bestämmer lämplig dosering för barn och ungdomar med polyartrit av juvenil idiopatisk artrit.
Reumaflex rekommenderas inte för barn under 3 år på grund av liten erfarenhet av denna åldersgrupp.
Administreringssätt och behandlingstid
Reumaflex administreras en gång i veckan!
Behandlingslängden bestäms av den behandlande läkaren. Reumatoid artrit, juvenil idiopatisk artrit, psoriasis vulgaris och psoriasisartritbehandlingar med Reumaflex är långtidsbehandlingar.
I början av behandlingen kan Reumaflex administreras av medicinsk personal. I vissa fall kan din läkare besluta att förklara hur du ska injicera Reumaflex själv subkutant. Om så är fallet får du lämpliga instruktioner.
Under inga omständigheter ska du försöka ge dig själv en injektion av Reumaflex utan att tidigare ha fått dessa instruktioner.
Se bruksanvisningen i slutet av bipacksedeln.
Hantering och bortskaffande bör göras som för andra cytostatiska preparat i enlighet med lokala föreskrifter. Gravida vårdpersonal bör avstå från att hantera och / eller administrera Reumaflex.
Metotrexat får inte komma i kontakt med hudytan eller slemhinnorna. Vid förorening ska det drabbade området omedelbart sköljas med mycket vatten.
Tala om för din läkare eller apotekspersonal om du känner att effekten av Reumaflex är för stark eller för svag.
Biverkningar Vilka är biverkningarna av Reumaflex
Liksom alla läkemedel kan Reumaflex orsaka biverkningar men alla användare behöver inte få dem.
Frekvensen liksom svårighetsgraden av de oönskade effekterna beror på dosering och administreringsfrekvens. Eftersom vissa allvarliga biverkningar kan uppstå även vid en låg dos, är det viktigt för din läkare att övervaka dem regelbundet.
Din läkare måste då beställa tester för att upptäcka avvikelser i ditt blod (t.ex. minskat antal vita blodkroppar, minskat antal trombocyter, lymfom) och förändringar i njurarnas och leverns funktion.
Tala omedelbart för din läkare om du märker något av följande symtom som kan indikera allvarliga, potentiellt livshotande biverkningar som kräver akut specifik behandling:
- ihållande torr hosta utan slem, andfåddhet och feber: dessa kan vara tecken på en "lunginfektion (lunginflammation) [vanligt - kan drabba upp till 1 av 10 personer];
- symtom på leverskada såsom gulning av hud och ögonvitor: metotrexat kan orsaka kronisk leverskada (levercirros), bildning av ärrvävnad i levern (leverfibros), fett degeneration av levern [allt ovanligt - kan påverka upp till 1 av 100 personer], inflammation i levern (akut hepatit) [sällsynt - kan drabba upp till 1 av 1000 personer] och leversvikt [mycket sällsynt - kan drabba upp till 1 av 10 000 personer]
- allergiska symtom som utslag inklusive röd kliande hud, svullnad i händer, fötter, anklar, ansikte, läppar, mun eller svalg (som kan orsaka svårigheter att svälja eller andas) och att känna sig svag - detta kan vara tecken på allvarliga allergiska reaktioner eller anafylaktisk chock [sällsynt - kan drabba upp till 1 av 1000 personer]
- symtom på njurskador som svullnad i händer, anklar, fötter eller förändringar i urineringsfrekvensen eller minskad eller ingen urin: dessa kan vara tecken på njursvikt [sällsynt - kan drabba upp till 1 av 1000 personer]
- symptom på infektion, t.ex. feber, frossa, värk, halsont: metotrexat kan göra dig mer mottaglig för infektioner. I sällsynta fall kan allvarliga infektioner [kan drabba upp till 1 av 1000 personer] såsom en specifik typ av lunginflammation (Pneumocystis carinii pneumoni) eller blodförgiftning (sepsis) uppstå
- svår diarré, kräkningar med blod och svarta eller mörka avföring: dessa symtom kan indikera en allvarlig och sällsynt [kan drabba upp till 1 av 1000 personer] mag -tarmsystemet orsakat av metotrexat, t.ex. gastrointestinala sår
- symptom i samband med blockering (ocklusion) av ett blodkärl genom en fristående blodpropp (tromboembolisk händelse) såsom svaghet på ena sidan av kroppen (stroke) eller ovanlig smärta, svullnad, rodnad och värme i ett ben (djup venetrombos): metotrexat kan orsaka tromboemboliska händelser [sällsynta - kan drabba upp till 1 av 1000 personer]
- feber och allvarlig försämring av allmäntillståndet eller plötslig feber åtföljt av ont i halsen eller ont i munnen eller urinproblem: metotrexat kan mycket sällan [kan drabba upp till 1 av 10 000 personer] en kraftig minskning av antalet vita blodkroppar (agranulocytos) och svår benmärgsdepression
- plötslig blödning, t.ex. blödning från tandköttet, blod i urinen, kräkningar med blod eller blåmärken: dessa kan vara tecken på en kraftig minskning av antalet trombocyter orsakade av allvarliga benmärgsförstöringar [mycket sällsynta - kan drabba upp till 1 av 10 000 personer]
- allvarliga utslag eller blåsor (kan också förekomma i munnen, ögonen och könsorganen): dessa kan vara tecken på ett mycket sällsynt tillstånd [kan drabba upp till 1 10 000 personer] som kallas Stevens Johnsons syndrom eller bränt hudsyndrom (toxisk epidermal nekrolys).
Andra biverkningar kan också förekomma, listade nedan:
Mycket vanliga: kan förekomma hos fler än 1 av 10 personer
- Inflammation i munnen, matsmältningsbesvär, illamående (illamående), aptitlöshet
- Ökade leverenzymer
Vanliga: kan förekomma hos upp till 1 av 10 personer
- Munsår, diarré
- Utslag, rodnad i huden, klåda
- Huvudvärk, trötthet, sömnighet
- Minskad bildning av blodkroppar med minskade vita och / eller röda blodkroppar och / eller trombocyter (leukopeni, anemi, trombocytopeni)
Mindre vanliga: kan förekomma hos upp till 1 av 100 personer
- Inflammation i halsen, tarminflammation, kräkningar
- Ökad ljuskänslighet, håravfall, ökat antal reumatiska knölar, Sankt Antonius brand, inflammation i blodkärl, herpesliknande utslag, nässelfeber
- Uppkomst av diabetes mellitus
- Yrsel, förvirring, depression
- Minskning av serumalbumin
- Minskning av antalet blodkroppar och trombocyter
- Inflammation och sår i urinblåsan eller slidan, nedsatt njurfunktion, problem med urinering (urinering)
- Ledsmärta, muskelsmärta, osteoporos (minskad benmassa)
Sällsynta: kan förekomma hos upp till 1 av 1000 personer
- Ökad hudpigmentering, akne, blåmärken på grund av blödning från blodkärl
- Allergisk inflammation i blodkärl, feber, röda ögon, infektion, svårigheter att läka sår, minskat antal antikroppar i blodet
- Synstörningar
- Inflammation i membranet som omger hjärtat, vätskeansamling i membranet som omger hjärtat
- Lågt blodtryck
- Lungfibros, andfåddhet och bronkial astma, ansamling av vätska i membranet som leder lungorna
- Elektrolytstörningar.
Mycket sällsynta: kan förekomma hos upp till 1 av 10 000 personer
- Kraftig blödning, giftigt megakolon (akut toxisk utvidgning av tarmen)
- Ökad nagelpigmentering, inflammation i områdena runt naglarna (nagelband), furunkulos (djup infektion i hårsäckarna), synlig förstoring av kapillärerna
- Lokal skada (steril abscessbildning, fettvävnadsförändringar) vid injektionsstället efter intramuskulär eller subkutan administrering.
- Störande syn, smärta, förlust av styrka eller känsla av domningar eller stickningar i armar och ben, smakförändringar (metallisk smak), anfall, förlamning, svår huvudvärk åtföljt av feber
- Retinopati (ögonsjukdomar av icke-inflammatoriskt ursprung) Förlust av libido, impotens, utvidgning av manliga bröstkörtlar (gynekomasti), onormal spermier, menstruation, vaginal urladdning
- Förstorade lymfkörtlar (lymfom)
Frekvens ej känd: kan inte uppskattas utifrån tillgängliga data:
- Leukoencefalopati (hjärtsjukdom)
När metotrexat administreras intramuskulärt är lokala biverkningar (brännande känsla) eller skada (steril abscessbildning, förstörelse av fettvävnad) på injektionsstället vanliga manifestationer. Subkutan administrering av metotrexat tolereras lokalt väl. Endast milda lokala hudreaktioner observerades och minskade under behandlingen.
Rapportering av biverkningar
Tala med din läkare eller apotekspersonal om du får några biverkningar. Detta inkluderar eventuella biverkningar som inte nämns i denna bipacksedel.Du kan också rapportera biverkningar direkt eller via Italian Medicines Agency-webbplats: https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse. Genom att rapportera biverkningar kan du hjälpa till att tillhandahålla mer information om säkerheten för detta läkemedel.
Giltighetstid och lagring
Förvara detta läkemedel utom syn- och räckhåll för barn.
Förvaras vid en temperatur som inte överstiger 25 ° C.
Förvara de förfyllda sprutor i ytterkartongen för att skydda dem mot ljus.
Använd inte detta läkemedel efter utgångsdatum som anges på kartongen. Utgångsdatumet avser den sista dagen i den månaden.
Läkemedel ska inte kastas i avloppsvatten eller hushållsavfall. Fråga din apotekare hur du ska kasta läkemedel som du inte använder längre. Detta hjälper till att skydda miljön.
Innehåller Reumaflex
- Den aktiva ingrediensen är metotrexat. 1 ml lösning innehåller dinatriummetotrexat motsvarande 50 mg metotrexat.
- Övriga innehållsämnen är natriumklorid, natriumhydroxid, vatten för injektionsvätskor.
Hur Reumaflex ser ut och förpackningens innehåll
Reumaflex förfyllda sprutor innehåller en klar gulbrun lösning.
Följande förpackningar finns tillgängliga:
- Förfyllda sprutor med fast subkutan nål, graderade märken och spritpinne innehållande 0,15 ml, 0,20 ml, 0,30 ml, 0,40 ml och 0,50 ml injektionsvätska, lösning i förpackningar med 1, 4, 6, 12 och 24 förfyllda sprutor.
- Förfyllda sprutor med separat subkutan nål, graderade märken och spritsudd, innehållande 0,15 ml, 0,20 ml, 0,30 ml, 0,40 ml och 0,50 ml injektionsvätska, lösning i förpackningar med 1, 4, 6, 12 och 24 förfyllda sprutor. För intramuskulär och intravenös användning bör en nål lämplig för dessa administreringsvägar användas Den separata nålen som ingår i förpackningen är endast lämplig för subkutan användning.
Alla förpackningsstorlekar kanske inte marknadsförs.
Användningsinstruktioner
Läs dessa instruktioner noggrant innan du börjar injektionen och använd alltid den injektionsteknik som rekommenderas av din läkare, apotekspersonal eller sjuksköterska. Kontakta din läkare, apotekspersonal eller sjuksköterska om du har några problem eller frågor
Förberedelse
Välj en platt, ren och väl upplyst arbetsyta.
Innan du börjar, samla allt du behöver:
- 1 förfylld spruta med Reumaflex
- 1 spritsudd (medföljer i förpackningen)
Tvätta händerna noggrant. Före användning, kontrollera Reumaflex -sprutan för eventuella synfel (eller sprickor).
Injektionsplats
De bästa injektionsställena är:
- lår,
- buken, exklusive området kring naveln.
- Om du har hjälp av en person för injektionen kan injektionen också ges på baksidan av armen, strax under axeln.
- Byt injektionsstället för varje injektion. Om du gör det kan du minska risken för irritation på injektionsstället.
- Injicera aldrig i områden med ömtålig, blåmärken, röd, hård, ärr eller hud med streckmärken. Om du lider av psoriasis, försök att inte injicera direkt i skador eller områden med upphöjd, tjock, röd eller upphöjd hud. hud eller skador.
Injektion av lösningen
1. Ta ut den förfyllda metotrexat sprutan ur förpackningen och läs bipacksedeln noggrant. Ta ut den förfyllda sprutan ur förpackningen vid rumstemperatur.
2. Desinfektion
Välj en injektionsplats och desinficera den med en pinne doppad i desinfektionsmedel.
Låt desinfektionsmedlet torka i minst 60 sekunder.
3. Ta bort det skyddande plastlocket
Ta försiktigt bort det grå skyddande plastlocket genom att dra det rakt ut ur sprutan. Om locket är mycket robust, vrid det försiktigt genom att dra utåt
Viktigt: Rör inte nålen på den förfyllda sprutan!
4. För in nålen
Ta tag i en hudveck med två fingrar och sätt snabbt in nålen i huden i 90 graders vinkel.
5. Injektion
För in nålen hela vägen in i hudvecket. Skjut kolven långsamt och injicera vätskan under huden. Håll ett stadigt grepp om hudvecket tills injektionen är klar.
Dra försiktigt ut nålen vertikalt
Metotrexat får inte komma i kontakt med hudytan eller slemhinnan. Vid förorening ska det drabbade området omedelbart sköljas med mycket vatten.
Om du eller någon i din närhet skadas av nålen, kontakta din läkare omedelbart och använd inte den förfyllda sprutan.
Avfallshantering och andra manipulationer
Hantering och bortskaffande av detta läkemedel och den förfyllda sprutan ska ske i enlighet med lokala krav. Gravida vårdpersonal bör avstå från att hantera och / eller administrera Reumaflex
Bipacksedel: AIFA (Italian Medicines Agency). Innehåll publicerat i januari 2016. Den information som finns finns kanske inte uppdaterad.
För att få tillgång till den senaste versionen är det lämpligt att gå till AIFA (Italian Medicines Agency) webbplats. Ansvarsfriskrivning och användbar information.
01.0 LÄKEMEDLETS NAMN
REUMAFLEX 50 mg / ml injektionsvätska, förfylld spruta
02.0 KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING
1 ml lösning innehåller 50 mg metotrexat (som dinatriummetotrexat).
1 förfylld spruta med 0,15 ml innehåller 7,5 mg metotrexat.
1 förfylld spruta med 0,20 ml innehåller 10 mg metotrexat.
1 förfylld spruta med 0,30 ml innehåller 15 mg metotrexat.
1 förfylld spruta med 0,40 ml innehåller 20 mg metotrexat.
1 förfylld spruta med 0,50 ml innehåller 25 mg metotrexat.
För fullständig förteckning över hjälpämnen, se avsnitt 6.1.
03.0 LÄKEMEDELSFORM
Injektionsvätska, lösning, förfylld spruta.
Klar gulbrun lösning.
04.0 KLINISK INFORMATION
04.1 Terapeutiska indikationer
Reumaflex är indicerat för behandling av:
- aktiv reumatoid artrit hos vuxna patienter,
-polyartritiska former av svår juvenil idiopatisk artrit i den aktiva fasen, med otillräckligt svar på icke-steroida antiinflammatoriska läkemedel (NSAID),
- svår, återfallande och handikappande psoriasis som inte svarar tillräckligt på andra former av terapi som fototerapi, PUVA och retinoider och svår psoriasisartrit hos vuxna patienter.
- mild till måttlig Crohns sjukdom, ensam eller i kombination med kortikosteroider hos vuxna patienter som är eldfasta eller intoleranta mot tiopuriner.
04.2 Dosering och administreringssätt
Reumaflex ska endast ordineras av läkare som är fullt bekanta med de olika egenskaperna hos läkemedlet och dess verkningsmekanism.Det ska administreras rutinmässigt av vårdpersonal.I vissa fall, om den kliniska situationen tillåter det, kan den behandlande läkaren delegera subkutan administrering till patienten själv.I dessa fall måste läkaren tillhandahålla detaljerade instruktioner för administration. Reumaflex administreras en gång i veckan.
Patienten måste uttryckligen informeras om doseringsfrekvensen en gång i veckan. Det är lämpligt att ställa in en fast veckodag som injektionsdag.
Elimineringen av metotrexat reduceras hos patienter med ett "tredje utrymme" i distributionen (ascites, pleural effusioner). Dessa patienter kräver noggrann övervakning av toxicitet och kräver dosreduktion eller i vissa fall avbrytande av dosering av metotrexat (se avsnitt 5.2 och 4.4).
Dosering hos vuxna patienter med reumatoid artrit
Den rekommenderade startdosen är 7,5 mg metotrexat en gång i veckan, administrerat subkutant, intramuskulärt eller intravenöst. Beroende på sjukdomens svårighetsgrad och patientens visade tolerabilitet för läkemedlet kan startdosen gradvis ökas med 2,5 mg per vecka. I allmänhet bör veckodosen på 25 mg inte överskridas även om redan högre doser än 20 mg / vecka är förknippade med en signifikant ökning av toxiciteten; särskilt undertryckande av benmärgsaktivitet. Svar på behandling kan ske efter 4 - 8 veckor. När önskat terapeutiskt resultat har uppnåtts bör dosen gradvis reduceras till den minsta effektiva underhållsdosen.
Dosering till barn och ungdomar under 16 år med polyartritiska former av juvenil idiopatisk artrit
Den rekommenderade dosen är 10 - 15 mg / m2 kroppsyta / en gång i veckan. Vid refraktär behandling kan veckodosen ökas upp till 20 mg / m2 kroppsyta / en gång i veckan. Vid dosökning, rekommenderas att öka övervakningsfrekvensen.
På grund av den begränsade tillgängligheten av data om intravenös administrering till barn och ungdomar, bör parenteral administrering begränsas till subkutana och intramuskulära injektioner.
Juvenil idiopatisk artritpatienter bör alltid hänvisas till specialiserade reumatologer för behandling av barn / ungdomar.
Användning till barn under 3 år rekommenderas inte på grund av den begränsade tillgängligheten av säkerhets- och effektdata för denna patientpopulation (se avsnitt 4.4).
Dosering till patienter med psoriasis vulgaris och psoriasisartrit
Det rekommenderas att en testdos på 5-10 mg parenteralt administreras en vecka före behandlingen för att upptäcka eventuella särdrag. Den rekommenderade startdosen av metotrexat är 7,5 mg en gång i veckan, administrerad subkutant, intramuskulärt eller intravenöst. Dosen kan ökas gradvis, men i allmänhet bör den aldrig överstiga en veckodos på 25 mg metotrexat. Doser över 20 mg per vecka kan redan vara associerade med en signifikant ökning av toxiciteten, särskilt med undertryckande av benmärgsaktivitet. Svar på behandlingen kan ske efter 2 - 6 veckor. När önskat terapeutiskt resultat har uppnåtts ska dosen gradvis reduceras till den lägsta effektiva underhållsdosen.
Dosen bör ökas efter behov men i allmänhet inte överstiga den högsta rekommenderade veckodosen på 25 mg. Endast i undantagsfall kan en högre dos vara kliniskt motiverad, men bör inte överstiga den maximala veckodosen på 30 mg metotrexat, eftersom toxiciteten ökar avsevärt.
Dosering till patienter med Crohns sjukdom:
• Induktionsterapi:
25 mg / vecka administreras subkutant, intravenöst eller intramuskulärt.
Svar på behandlingen kan förväntas efter cirka 8 till 12 veckor.
• Underhållsterapi:
15 mg / vecka administreras subkutant, intravenöst eller intramuskulärt.
Det finns otillräcklig erfarenhet hos den pediatriska populationen för att rekommendera Reumaflex 50 mg / ml vid behandling av Crohns sjukdom i denna population.
Patienter med nedsatt njurfunktion
Reumaflex ska användas med försiktighet till patienter med nedsatt njurfunktion. Dosen bör justeras enligt följande:
Patienter med nedsatt leverfunktion
Metotrexat ska administreras med stor försiktighet, särskilt hos patienter som lider av allvarlig leversjukdom, antingen nuvarande eller tidigare, särskilt om det beror på alkohol.Metotrexat är kontraindicerat i de fall bilirubin är högre än 5 mg / dl (85,5 mcmol / l).
För en fullständig lista över kontraindikationer, se avsnitt 4.3.
Användning hos äldre patienter
Hos äldre patienter kan dosen minskas på grund av nedsatt lever- och njurfunktion och minskade folatreserver i samband med ålder.
Användning till patienter med ett "tredje utrymme" för distribution (pleural effusion, ascites)
Hos patienter med ett "tredje utrymme" för distribution kan halveringstiden för metotrexat öka upp till fyra gånger, därför kan en dosreduktion eller, i vissa fall, avbrytande av metotrexat administrering krävas (se avsnitt 5.2 och 4.4).
Varaktighet och administreringssätt
Läkemedlet är endast för engångsbruk.
Reumaflex injektionsvätska, lösning kan administreras intramuskulärt, intravenöst eller subkutant (endast hos barn och ungdomar, subkutant eller intramuskulärt).
Den totala behandlingstiden bestäms av läkaren.
Notera:
Att byta från oral behandling till parenteral administrering kan kräva en dosreduktion på grund av variationen i biotillgängligheten för metotrexat efter oral administrering.
Folsyratillskott kan övervägas i enlighet med gällande riktlinjer.
04.3 Kontraindikationer
Reumaflex är kontraindicerat vid
- överkänslighet mot metotrexat eller mot något hjälpämne som anges i avsnitt 6.1,
- Allvarligt nedsatt leverfunktion (se avsnitt 4.2),
- alkoholmissbruk,
- allvarligt nedsatt njurfunktion (kreatininclearance mindre än 20 ml / min, se avsnitt 4.2 och 4.4),
- redan existerande bloddyskrasi såsom benmärgshypoplasi, leukopeni, trombocytopeni eller signifikant anemi,
- allvarliga, akuta eller kroniska infektioner som tuberkulos, HIV eller andra immunsviktssyndrom
- munsår och historia av aktivt mag -tarmsår,
- graviditet, amning (se avsnitt 4.6),
- samtidig vaccination med levande vacciner.
04.4 Särskilda varningar och lämpliga försiktighetsåtgärder vid användning
Patienterna bör tydligt informeras om att terapi bör utföras en gång i veckan och inte varje dag.
Patienter som genomgår behandling bör underkastas lämpliga kontroller för att snabbt identifiera och bedöma utseendet på möjliga toxiska effekter eller biverkningar. Metotrexat ska därför endast administreras av eller under överinseende av läkare som har kunskap och erfarenhet av användning av antimetabolitbehandling.På grund av möjliga allvarliga, till och med dödliga toxiska reaktioner, måste patienten informeras tillräckligt av läkaren om eventuella risker och om de säkerhetsåtgärder som ska vidtas.
Användning till barn under 3 år rekommenderas inte på grund av den begränsade tillgängligheten av säkerhets- och effektdata för denna patientpopulation (se avsnitt 4.2).
Rekommenderade undersökningar och säkerhetsåtgärder
Innan behandling med metotrexat påbörjas eller återinförs efter avbrott:
Kompletta och differentiella blodtal, trombocytantal, leverenzymer, bilirubin, serumalbumin, röntgen på bröstet och njurfunktionstester. Uteslut tuberkulos och hepatit om det är kliniskt indikerat.
Under behandlingen (minst en gång i månaden under de första sex månaderna och därefter var tredje månad):
Öka övervakningsfrekvensen om dosen ökas.
1. Undersökning av mun och hals för eventuella slemhinneförändringar.
2. Kompletta och differentiella blodtal och trombocytantal. Undertryckandet av hematopoes orsakad av metotrexat kan plötsligt och med uppenbarligen säkra doser inträffa. En drastisk minskning av antalet vita blodkroppar eller trombocyter leder till omedelbar avbrytande av läkemedlet och initiering av adekvat stödjande behandling. Patienter bör uppmanas att rapportera alla tecken. och symptom som tyder på en infektion. Blod- och trombocytantal bör övervakas noggrant hos patienter som samtidigt tar andra myelotoxiska läkemedel (t.ex. leflunomid).
3. Leverfunktionstester: särskild uppmärksamhet bör ägnas åt förekomsten av levertoxicitet. Behandling ska inte ges eller ska avbrytas om onormala leverfunktionstester eller leverbiopsi hittas eller utvecklas under behandlingen. Dessa avvikelser ska återgå till det normala inom två veckor, varefter behandlingen kan återupptas efter läkarens gottfinnande. Det finns inga belägg för användning av leverbiopsi för övervakning av levertoxicitet vid reumatologiska indikationer.
För patienter med psoriasis är behovet av leverbiopsi före och under behandlingen kontroversiellt. Ytterligare forskning behövs för att fastställa om seriell lever eller typ III-kollagenpropeptidkemiska tester snabbt och effektivt kan rapportera hepatotoxicitet. Bedömning bör göras från fall till fall och bör skilja mellan patienter utan riskfaktorer och patienter med risk faktorer som tidigare alkoholmissbruk, ihållande förhöjning av leverenzymer, leversjukdom, anamnes på ärftlig leversjukdom, diabetes mellitus, fetma, historia av betydande exponering för hepatotoxiska läkemedel eller kemikalier, långvarig behandling med metotrexat eller kumulativa doser på 1,5 g eller mer.
Kontroll av leverenzymer i serum: Tillfälliga ökningar av transaminaser med upp till två eller tre gånger normalgränsen har rapporterats av patienter med en frekvens på 13 - 20%. Vid en stadig ökning av leverenzymer bör en dosreduktion eller avbrott av behandlingen övervägas.
På grund av den potentiellt toxiska effekten på levern ska inga andra hepatotoxiska läkemedel tas under behandling med metotrexat.om de inte helt klart behövs och alkoholkonsumtion bör undvikas eller minskas avsevärt (se avsnitt 4.5). Noggrann övervakning av leverenzymer bör utföras hos patienter som samtidigt tar andra hepatotoxiska läkemedel (t.ex. leflunomid). Detsamma gäller för samtidig administrering av hematotoxiska läkemedel (t.ex. leflunomid).
4. Njurfunktionen bör övervakas genom njurfunktionstester och urinanalys (se avsnitt 4.2 och 4.3).
Eftersom metotrexat elimineras främst via njurarna kan ökade serumkoncentrationer uppstå vid nedsatt njurfunktion, vilket kan leda till allvarliga biverkningar.
Om njurfunktionen kan vara nedsatt (t.ex. hos äldre) bör övervakning ske oftare. Frekvent övervakning bör tillämpas särskilt när läkemedel som kan påverka eliminering av metotrexat och orsaka njurskada (t.ex. icke-steroida antiinflammatoriska läkemedel), eller som potentiellt kan leda till nedsatt hematopoies, administreras samtidigt. Dehydrering kan också öka toxiciteten för metotrexat.
5. Utvärdering av andningsorganen: vaksamhet för symtom på nedsatt lungfunktion och vid behov lungfunktionstester Lunginvolvering kräver snabb diagnos och avbrytande av metotrexat. Lungesymtom (särskilt torr hosta och oproduktiv) eller ospecifik lunginflammation som uppstår under metotrexat behandling, kan vara en indikation på en potentiellt farlig skada och kräva "avbrytande av behandlingen och" noggrann undersökning. Akut eller kronisk interstitiell lunginflammation kan uppstå, ofta förknippad med eosinofili i blodet, och vissa dödsfall har registrerats. När lunginfektioner har uteslutits, den typiska metotrexatinducerade lungsjukdomen hos patienten, även om den är kliniskt varierande, uppvisar feber, hosta, dyspné, hypoxemi och infiltrat på röntgenbilder på bröstet. Lungnedsättning kräver tidig diagnos och avbrott och metotrexatbehandling. Denna försämring kan uppstå oavsett vilka doser som används.
6. På grund av dess effekt på immunsystemet kan metotrexat försämra svaret på vaccinationsresultat och påverka resultatet av immunologiska tester. Särskild försiktighet bör också iakttas i närvaro av kroniska inaktiva infektioner (t.ex. herpes zoster, tuberkulos, hepatit B eller C) på grund av eventuell aktivering. Vaccination med levande vaccin bör inte utföras under metotrexatbehandling.
Maligna lymfom kan förekomma hos patienter som får låg dos metotrexat, och i detta fall bör behandlingen avbrytas. Om lymfom inte visar några tecken på spontan regression, bör cytotoxisk behandling påbörjas.
I sällsynta fall har samtidig administrering av folatantagonister som trimetoprim-sulfametoxazol inducerat akut megaloblastisk pancytopeni.
Strålningsdermatit och solbränna kan återkomma under metotrexatbehandling (återkallningsreaktion). Psoriatiska skador kan förvärras efter samtidig användning av ultraviolett strålning och metotrexat.
Elimination av metotrexat reduceras hos patienter med ett "tredje utrymme" i distributionen (ascites, pleural effusioner) Dessa patienter kräver noggrann övervakning av toxicitet och kräver dosreduktion eller, i vissa fall, avbrytande av dosering av metotrexat. Pleural effusioner och ascites måste dräneras innan behandling med metotrexat påbörjas (se avsnitt 5.2).
Diarré och ulcerös stomatit kan vara toxiska effekter och kräva att behandlingen avbryts, annars kan hemorragisk enterit och död från tarmperforering uppstå.
Vitaminpreparat eller andra läkemedel som innehåller folsyra, folinsyra eller derivat kan minska metotrexats effektivitet.
För behandling av psoriasis bör metotrexat begränsas till svår, återfallande och handikappande psoriasis som inte svarar adekvat på andra behandlingsformer, men endast när diagnosen bekräftas av en biopsi och / eller dermatologisk konsultation.
Encefalopati / leukoencefalopati har rapporterats hos cancerpatienter som får metotrexat och kan inte uteslutas för metotrexatbehandling vid icke-cancerindikationer.
Detta läkemedel innehåller mindre än 1 mmol natrium (23 mg) per dos och anses i huvudsak vara "natriumfritt".
Frånvaro av graviditet måste fastställas innan Reumaflex ges. Metotrexat kan orsaka embryotoxicitet, abort och fosterskador hos kvinnor. Metotrexat påverkar spermatogenes och oogenes under administreringsperioden och kan orsaka minskad fertilitet. Dessa effekter tycks vara reversibla när behandlingen avbryts.Effektivt preventivmedel för män och kvinnor bör utövas under behandlingen och åtminstone under sex månader efter avslutad behandling. Patienter i fertil ålder och deras partner bör informeras på lämpligt sätt om de möjliga riskerna och reproduktionseffekterna (se avsnitt 4.6).
04.5 Interaktioner med andra läkemedel och andra former av interaktion
Alkohol, hepatotoxiska läkemedel, hematotoxiska läkemedel
Sannolikheten för att metotrexat inducerar hepatotoxiska effekter ökar genom regelbunden alkoholkonsumtion och samtidig användning av andra hepatotoxiska läkemedel (se avsnitt 4.4) Patienter som samtidigt tar andra hepatotoxiska läkemedel (t.ex. leflunomid) bör övervakas noggrant. samtidig administrering av hematotoxiska läkemedel (t.ex. leflunomid, azatioprin, retinoider, sulfasalazin). Samtidig administrering av metotrexat och leflunomid kan öka förekomsten av pancytopeni och hepatotoxicitet.
Kombinerad behandling med metotrexat och retinoider som acitretin eller etretinat ökar risken för hepatotoxicitet.
Orala antibiotika
Orala antibiotika som tetracykliner, kloramfenikol och icke-absorberbara bredspektrumantibiotika, genom att hämma tarmfloran eller undertrycka bakteriell metabolism, kan störa den enterohepatiska cirkulationen av metotrexat.
Antibiotika
Antibiotika som penicilliner, glykopeptider, sulfonamider, ciprofloxacin och cefalotin kan i enskilda fall reducera renal clearance av metotrexat, vilket leder till ökade koncentrationer av metotrexat i serum med följd hematologisk och gastrointestinal toxicitet.
Läkemedel med hög plasmaproteinbindning
Cirkulerande metotrexat binder till plasmaproteiner och kan ersättas av andra proteinbindande läkemedel som salicylater, hypoglykemiska medel, diuretika, sulfonamider, difenylhydantoin, tetracykliner, kloramfenikol, p-aminobensoesyra och antiinflammatoriska syror, vilket resulterar i potentiellt ökad toxicitet vid samtidig användning .
Probenecid, svaga organiska syror, pyrazoler och icke-steroida antiinflammatoriska medel
Probenecid, svaga organiska syror, såsom loop -diuretika och pyrazolonderivat (fenylbutazon), kan minska eliminering av metotrexat med möjliga högre serumkoncentrationer och risk för ökad hematologisk toxicitet. Toxicitet kan också öka när lågdosmetotrexat och icke-steroida antiinflammatoriska läkemedel eller salicylater kombineras tillsammans.
Läkemedel med biverkningar på benmärgen
Vid behandling med läkemedel som kan vara ansvariga för biverkningar på benmärgen (t.ex. sulfonamider, trimetoprim-sulfametoxazol, kloramfenikol, pyrimetamin) bör man uppmärksamma risken för allvarlig försämring av hematopoes.
Läkemedel som orsakar folatbrist
Samtidig administrering av läkemedel som orsakar folatbrist (t.ex. sulfonamider, trimetoprim-sulfametoxazol) kan leda till ökad metotrexattoxicitet. Särskild uppmärksamhet rekommenderas därför för redan existerande folsyrabrister.
Produkter som innehåller folsyra eller folinsyra
Vitaminpreparat eller andra produkter som innehåller folsyra, folsyra eller deras derivat kan minska metotrexats effektivitet.
Andra antireumatiska läkemedel
I allmänhet förväntas ingen ökning av de toxiska effekterna av metotrexat när Reumaflex administreras samtidigt med andra antireumatiska läkemedel (t.ex. guldsalter, penicillamin, hydroxiklorokin, sulfasalazin, azatioprin, cyklosporin).
Sulfasalazin
Endast i sällsynta enskilda fall som observerats i kliniska prövningar resulterade inhiberingen av folsyrasyntesen inducerad av sulfasalazin samtidigt administrerad med metotrexat i en ökning av metotrexats effekt och följaktligen ett större antal biverkningar.
Merkaptopurin
Metotrexat ökar plasmamerkaptopurinhalten. Kombinationen av metotrexat och merkaptopurin kan därför kräva dosjustering.
Protonpumpshämmare
Samtidig administrering av protonpumpshämmare såsom omeprazol eller pantoprazol kan leda till interaktioner. Samtidig administrering av metotrexat och omeprazol resulterade i försenad renal eliminering av metotrexat. Kombinationen med pantoprazol resulterade i inhibering av renal eliminering av metaboliten 7-hydroximetotrexat med myalgi och tremor.
Teofyllin
Metotrexat kan minska teofyllinclearance; teofyllinnivåerna bör övervakas vid samtidig användning med metotrexat.
Drycker som innehåller koffein eller teofyllin
Överdriven konsumtion av koffeinhaltiga eller teofyllinhaltiga drycker (kaffe, koffeinhaltiga läskedrycker, svart te) bör undvikas under metotrexatbehandling.
04.6 Graviditet och amning
Graviditet
Reumaflex är kontraindicerat under graviditet (se avsnitt 4.3). I djurstudier har metotrexat visat toxiska effekter på reproduktionen (se avsnitt 5.3). Metotrexat har visat sig vara teratogent hos människor; Fall av fosterdöd och / eller medfödda avvikelser har rapporterats. Exponering av ett begränsat antal gravida kvinnor har visat en ökad förekomst (1:14) av missbildningar (kranial, kardiovaskulär och lem). När metotrexat avbröts före befruktningen registrerades normala graviditeter. Kvinnor får inte bli gravida under behandling med metotrexat. Om graviditet inträffar under behandlingen bör läkaren rådfrågas om risken för biverkningar av barnet i samband med metotrexatbehandling. Följaktligen måste patienter i könsmogen ålder (män och kvinnor) utöva effektivt preventivmedel under behandling med Reumaflex som förlängs till minst sex månader efter avslutad behandling (se avsnitt 4.4).
Innan behandling påbörjas hos kvinnor i fertil ålder bör en befintlig graviditet säkert uteslutas med ett graviditetstest.
Matdags
metotrexat utsöndras i bröstmjölk i koncentrationer som utgör en risk för den nyfödda och följaktligen måste amning avbrytas före och under administrering
Fertilitet
Eftersom metotrexat kan vara genotoxiskt rekommenderas alla kvinnor som vill bli gravida att konsultera ett genetiskt rådgivningscenter om möjligt innan behandling påbörjas, och för män att fråga om möjligheterna att lagra spermier innan terapin påbörjas.
04.7 Effekter på förmågan att framföra fordon och använda maskiner
Centrala nervsystemet symptom som trötthet och yrsel kan uppstå under behandlingen; Reumaflex har "mild eller måttlig påverkan på förmågan att framföra fordon och använda maskiner."
04.8 Biverkningar
De mest relevanta biverkningarna är undertryckande av hematopoes och gastrointestinala störningar.
Följande titlar används för att klassificera oönskade effekter efter frekvens:
Mycket vanliga (≥ 1/10), vanliga (≥ 1/100,
Neoplasmer är godartade, maligna och ospecificerade (inklusive cystor och polyper).
Mycket sällsynta: Enstaka fall av lymfomregression har rapporterats efter avbrytande av metotrexatbehandling.I en ny studie var det inte möjligt att fastställa om metotrexatbehandling ökar förekomsten av lymfom.
Störningar i blodet och lymfsystemet
Vanliga: leukopeni, anemi, trombocytopeni.
Mindre vanliga: pancytopeni.
Mycket sällsynta: agranulocytos, svår benmärgsdepression.
Metabolism och näringsstörningar
Mindre vanliga: dekompenserad diabetes mellitus.
Nervsystemet
Vanliga: huvudvärk, trötthet, sömnighet.
Mindre vanliga: yrsel, förvirring, depression.
Mycket sällsynta: synskada, smärta, muskelsvaghet eller parestesi i lemmarna, smakförändringar (metallisk smak), kramper, meningism, förlamning.
Ingen känd frekvens: leukoencefalopati
Ögonbesvär
Sällsynta: synstörningar.
Mycket sällsynta: retinopati.
Hjärtpatologier
Sällsynta: perikardit, perikardial effusion, perikardial tamponad.
Vaskulära patologier
Sällsynta: hypotoni, tromboemboliska händelser.
Andningsvägar, bröstkorg och mediastinum
Vanliga: lunginflammation, alveolit / interstitiell lunginflammation som ofta förknippas med eosinofili. Symtom som indikerar en potentiellt allvarlig lungskada (interstitiell lunginflammation) är: torr, icke-produktiv hosta, andfåddhet och feber.
Sällsynt: lungfibros, lunginflammation från Pneumocystis cariniiandfåddhet och bronkial astma, pleural effusion.
Gastrointestinala störningar
Mycket vanliga: stomatit, dyspepsi, illamående, aptitlöshet.
Vanliga: munsår, diarré.
Mindre vanliga: faryngit, enterit, kräkningar.
Sällsynta: gastrointestinala sår.
Mycket sällsynta: hematemes, blödning, giftigt megakolon.
Lever- och gallvägar (se avsnitt 4.4)
Mycket vanligt: förhöjda transaminaser.
Mindre vanliga: cirros, fibros och fet leversjukdom, minskat serumalbumin.
Sällsynta: akut hepatit.
Mycket sällsynta: leversvikt.
Hud och subkutan vävnad
Vanliga: utslag, erytem, klåda.
Mindre vanliga: fotosensibilisering, håravfall, ökade reumatiska knölar, herpes zoster, vaskulit, herpetiform hudutbrott, urtikaria.
Rarei: ökad pigmentering, akne, blåmärken.
Mycket sällsynta: Stevens-Johnsons syndrom, toxisk epidermal nekrolys (Lyells syndrom), nagelpigmenteringsförändringar, akut paronychia, furunkulos, telangiektasi.
Muskuloskeletala systemet och bindvävssjukdomar
Mindre vanliga: artralgi, myalgi, osteoporos.
Njurar och urinvägar
Mindre vanliga: inflammation och sår i urinblåsan, nedsatt njurfunktion, urinering.
Sällsynta: njursvikt, oliguri, anuri, elektrolytstörningar.
Sjukdomar i reproduktionssystemet och bröstet
Mindre vanliga: inflammation och sår i slidan.
Mycket sällsynta: förlust av libido, impotens, gynekomasti, oligospermi, menstruationsstörningar, vaginal urladdning.
Allmänna störningar och tillstånd på administreringsstället
Sällsynta: allergiska reaktioner, anafylaktisk chock, allergisk vaskulit, feber, konjunktivit, infektion, sepsis, fördröjd sårläkning, hypogammaglobulinemi.
Mycket sällsynta: Lokal skada (steril abscessbildning, lipodystrofi) på injektionsstället efter intramuskulär eller subkutan administrering.
Förekomsten och svårighetsgraden av oönskade effekter beror på dosering och administreringsfrekvens. Men eftersom allvarliga biverkningar kan uppstå även vid låga doser, är det absolut nödvändigt att patienter övervakas av sin läkare med korta och regelbundna intervall.
När metotrexat administreras intramuskulärt är lokala biverkningar (brännande känsla) eller skador (steril abscessbildning, förstörelse av fettvävnad) på injektionsstället vanliga manifestationer. Subkutan administrering av metotrexat tolereras lokalt väl. Endast milda lokala hudreaktioner återgick under behandlingens gång.
Rapportering av misstänkta biverkningar
Det är viktigt att rapportera misstänkta biverkningar som inträffar efter godkännande av läkemedlet, eftersom det möjliggör kontinuerlig övervakning av nytta / riskförhållandet för läkemedlet.Hälso- och sjukvårdspersonal uppmanas att rapportera alla misstänkta biverkningar via den italienska läkemedelsmyndigheten. - webbplats: www.agenziafarmaco.gov.it/it/responsabili.
04.9 Överdosering
a) Symtom på överdosering
Metotrexats toxicitet påverkar främst det hematopoetiska systemet.
b) Insatsåtgärder vid överdosering
Kalciumfolinat är den specifika motgiften för att neutralisera de oönskade toxiska effekterna av metotrexat.
Vid oavsiktlig överdos ska en dos kalciumfolinat som är lika med eller större än den toxiska dosen metotrexat administreras intravenöst eller intramuskulärt inom en "timme, följt av ytterligare doser tills serummetotrexathalter under 10-7 mol erhålls. /L.
Vid massiv överdosering kan hydrering och urinalkalinisering krävas för att förhindra utfällning av metotrexat och / eller dess metaboliter i njurtubuli. Varken hemodialys eller peritonealdialys har visat en förbättring av eliminering av metotrexat. "Effektiv eliminering av metotrexat med" akut intermittent hemodialys med hjälp av en högflödessdialysator har rapporterats.
05.0 FARMAKOLOGISKA EGENSKAPER
05.1 Farmakodynamiska egenskaper
Farmakoterapeutisk grupp: folsyraanaloger.
ATC -kod: L01BA01.
Antireumatisk medicin för behandling av kroniska inflammatoriska reumatiska sjukdomar och polyartritiska former av juvenil idiopatisk artrit. Immunmodulerande och antiinflammatoriskt medel för behandling av Crohns sjukdom.
Handlingsmekanism
Metotrexat är en folsyraantagonist som tillhör klassen av cytotoxiska medel som kallas antimetaboliter och verkar genom konkurrenskraftig hämning av dihydrofolatreduktasenzymet och hämmar därmed DNA -syntes. Det är dock ännu inte klarlagt om metotrexats effekt vid behandling av psoriasis, psoriasisartrit, kronisk polyartrit och Crohns sjukdom beror på en antiinflammatorisk eller immunsuppressiv effekt och i vilken utsträckning en ökning av koncentrationen av extracellulär adenosin inducerad med metotrexat vid inflammationsställena bidrar till att uppnå dessa effekter.
Internationella kliniska riktlinjer indikerar användning av metotrexat som en andrahandsbehandling för patienter med Crohns sjukdom som är intoleranta eller inte har svarat på förstahandsbehandling med immunmodulerande medel som azatioprin (AZA) eller 6-merkaptopurin (6- MP).
Biverkningar observerade i studier utförda med metotrexat för Crohns sjukdom vid kumulativa doser visade inte en annan säkerhetsprofil för metotrexat än den som redan är känd. Därför bör liknande försiktighetsåtgärder användas vid användning av metotrexat för behandling av Crohns sjukdom som för andra indikationer på metotrexat vid reumatiska och icke-reumatiska sjukdomar (se avsnitt 4.4 och 4.6).
05.2 Farmakokinetiska egenskaper
Distribution
Administreras oralt, absorberas metotrexat från mag -tarmkanalen. Vid administrering av låga doser (doser mellan 7,5 mg / m2 och 80 mg / m2 kroppsyta) är den genomsnittliga biotillgängligheten cirka 70 %, men många inter- och intraindividuella variationer är möjliga (25- 100 %) . Maximal serumkoncentration uppnås efter 1-2 timmar.
Biotransformation
Biotillgängligheten för metotrexat administrerat subkutant, intravenöst och intramuskulärt är liknande och nära 100%.
Eliminering
Cirka 50% av metotrexatet är bundet till vassleproteiner. Efter att ha distribuerats i olika kroppsvävnader finns höga koncentrationer i form av polyglutamat främst i levern, njurarna och mjälten i synnerhet, där de kan stanna i veckor eller månader. När det ges i låga doser passerar endast små mängder metotrexat in i CSF. Halveringstiden för produkten är i genomsnitt 6 - 7 timmar, men med stor variation (3 - 17 timmar). Halveringstiden kan öka upp till 4 gånger hos patienter med ett "tredje utrymme" för distribution (pleural effusion, ascites).
Cirka 10% av den administrerade metotrexatdosen metaboliseras av levern. Huvudmetaboliten är 7-hydroximetotrexat.
Utsöndring sker främst via njuren som oförändrat metotrexat, via glomerulär filtrering och aktiv utsöndring i den proximala tubuli.
Cirka 5 - 20% av metotrexat och 1 - 5% av 7 -hydroximetotrexat elimineras via gallvägen Den enteropatiska cirkulationen är intensiv.
Eliminering försenas avsevärt vid nedsatt njurfunktion, medan den inte är känd vid leverinsufficiens.
05.3 Prekliniska säkerhetsdata
Djurstudier visar att metotrexat försämrar fertiliteten, är embryotoxiskt, foetotoxiskt och teratogent. Metotrexat är mutagent in vivo Och in vitro. Eftersom formella cancerframkallande studier inte har genomförts och studier av kronisk toxicitet hos gnagare inte är tillräckliga anses metotrexat vara oklassificerat med avseende på dess cancerframkallande egenskaper hos människor.
06.0 LÄKEMEDELSINFORMATION
06.1 Hjälpämnen
Natriumklorid
Natriumhydroxid för pH -reglering
Vatten för injektionsvätskor
06.2 Oförenlighet
I avsaknad av kompatibilitetsstudier får detta läkemedel inte blandas med andra läkemedel.
06.3 Giltighetstid
2 år.
06.4 Särskilda förvaringsanvisningar
Förvaras vid högst 25 ° C. Förvara de förfyllda sprutor i ytterkartongen för att skydda dem mot ljus.
06.5 Förpackningens innehåll och förpackningens innehåll
Behållarens art:
Förfyllda sprutor av färglöst glas (typ I) med 1 ml kapacitet med fast injektionsnål. Klorobutylgummiproppar (typ I) och polystyrenstavar införda i proppen för att bilda sprutkolven
eller
Förfyllda sprutor av färglöst glas (typ I) med 1 ml kapacitet med separat injektionsnål. Klorobutylgummiproppar (typ I) och polystyrenstavar införda över proppen för att bilda sprutkolven.
Förpackning:
Förfyllda sprutor innehållande 0,15 ml, 0,20 ml, 0,30 ml, 0,40 ml, 0,50 ml lösning, tillgängliga i förpackningar med 1, 4, 6, 12 och 24 förfyllda sprutor med fast subkutan nål och alkoholkuddar.
Och
Förfyllda sprutor innehållande 0,15 ml, 0,20 ml, 0,30 ml, 0,40 ml, 0,50 ml lösning, tillgängliga i förpackningar med 1, 4, 6, 12 och 24 förfyllda sprutor med separata subkutana nålar och alkoholkuddar.
För intramuskulär och intravenös användning måste en nål som är lämplig för dessa administreringssätt användas: nålen som ingår i förpackningen är endast lämplig för subkutan användning.
Alla förpackningar finns med betyg.
Alla förpackningsstorlekar kanske inte marknadsförs.
06.6 Anvisningar för användning och hantering
Hantering och avfallshantering bör ske på samma sätt som för andra cytotoxiska preparat i enlighet med lokala föreskrifter. Gravida vårdpersonal bör avstå från att hantera och / eller administrera Reumaflex.
Metotrexat får inte komma i kontakt med huden eller slemhinnorna. Vid förorening ska det drabbade området omedelbart sköljas med mycket vatten.
Endast för engångsbruk.
Oanvänd medicin eller avfall från detta läkemedel måste kasseras i enlighet med lokala föreskrifter.
Instruktioner för subkutan användning
De mest lämpliga injektionsställena är:
• lår,
• buken, exklusive periumbilikalområdet.
1. Rengör området kring det valda injektionsstället (t.ex. med användning av spritpinne).
2. Ta bort den skyddande plastkåpan genom att hålla den rak.
3. Vik huden genom att försiktigt nypa injektionsstället.
4. Vikningen måste bibehållas under hela injektionen.
5. För in nålen helt i huden i 90 graders vinkel.
6. Tryck långsamt på kolven och injicera vätskan under huden. Dra sprutan ur huden samtidigt som nålen hålls 90 grader.
07.0 INNEHAVARE AV GODKÄNNANDE FÖR FÖRSÄLJNING
ALFA WASSERMANN S.p.A.
Via Enrico Fermi n.1
65020 - ALANNO (PE)
08.0 NUMMER FÖR FÖRSÄLJNINGSTILLSTÅND
039153010-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 1 förfylld spruta med 0,15 ml med fast subkutan nål;
039153022-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 4 förfyllda sprutor med 0,15 ml med fast subkutan nål;
039153034-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 6 förfyllda sprutor med 0,15 ml med fast subkutan nål;
039153046-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 12 förfyllda sprutor med 0,15 ml med fast subkutan nål;
039153059-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 24 förfyllda sprutor med 0,15 ml med fast subkutan nål;
039153061-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 1 förfylld spruta med 0,15 ml med separat subkutan nål;
039153073-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 4 förfyllda sprutor med 0,15 ml med separat subkutan nål;
039153085-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 6 förfyllda sprutor med 0,15 ml med separat subkutan nål;
039153097-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 12 förfyllda sprutor med 0,15 ml med separat subkutan nål;
039153109-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 24 förfyllda sprutor med 0,15 ml med separat subkutan nål;
039153111-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 1 förfylld spruta med 0,20 ml med fast subkutan nål;
039153123-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 4 förfyllda sprutor med 0,20 ml med fast subkutan nål;
039153135-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 6 förfyllda sprutor med 0,20 ml med fast subkutan nål;
039153147-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 12 förfyllda sprutor med 0,20 ml med fast subkutan nål;
039153150-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 24 förfyllda sprutor med 0,20 ml med fast subkutan nål;
039153162-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 1 förfylld spruta med 0,20 ml med separat subkutan nål;
039153174-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 4 förfyllda sprutor med 0,20 ml med separat subkutan nål;
039153186-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 6 förfyllda sprutor med 0,20 ml med separat subkutan nål;
039153198-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 12 förfyllda sprutor med 0,20 ml med separat subkutan nål;
039153200-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 24 förfyllda sprutor med 0,20 ml med separat subkutan nål;
039153212-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 1 förfylld spruta med 0,30 ml med fast subkutan nål;
039153224-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 4 förfyllda sprutor med 0,30 ml med fast subkutan nål;
039153236-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 6 förfyllda sprutor om 0,30 ml med fast subkutan nål;
039153248-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 12 förfyllda sprutor med 0,30 ml med fast subkutan nål;
039153251-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 24 förfyllda sprutor med 0,30 ml med fast subkutan nål;
039153263-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 1 förfylld spruta med 0,30 ml med separat subkutan nål;
039153275-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 4 förfyllda sprutor med 0,30 ml med separat subkutan nål;
039153287-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 6 förfyllda sprutor med 0,30 ml med separat subkutan nål;
039153299-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 12 förfyllda sprutor med 0,30 ml med separat subkutan nål;
039153301-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 24 förfyllda sprutor med 0,30 ml med separat subkutan nål;
039153313-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 1 förfylld spruta med 0,40 ml med fast subkutan nål;
039153325-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 4 förfyllda sprutor med 0,40 ml med fast subkutan nål;
039153337-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 6 förfyllda sprutor med 0,40 ml med fast subkutan nål;
039153349-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 12 förfyllda sprutor med 0,40 ml med fast subkutan nål;
039153352-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 24 förfyllda sprutor med 0,40 ml med fast subkutan nål;
039153364-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 1 förfylld spruta med 0,40 ml med separat subkutan nål;
039153376-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 4 förfyllda sprutor med 0,40 ml med separat subkutan nål;
039153388-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 6 förfyllda sprutor med 0,40 ml med separat subkutan nål;
039153390-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 12 förfyllda sprutor med 0,40 ml med separat subkutan nål;
039153402-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 24 förfyllda sprutor med 0,40 ml med separat subkutan nål;
039153414-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 1 förfylld spruta med 0,50 ml med fast subkutan nål;
039153426-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 4 förfyllda sprutor med 0,50 ml med fast subkutan nål;
039153438-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 6 förfyllda sprutor med 0,50 ml med fast subkutan nål;
039153440-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 12 förfyllda sprutor med 0,50 ml med fast subkutan nål;
039153453-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 24 förfyllda sprutor med 0,50 ml med fast subkutan nål;
039153465-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 1 förfylld spruta med 0,50 ml med separat subkutan nål;
039153477-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 4 förfyllda sprutor med 0,50 ml med separat subkutan nål;
039153489-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 6 förfyllda sprutor med 0,50 ml med separat subkutan nål;
039153491-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 12 förfyllda sprutor med 0,50 ml med separat subkutan nål;
039153503-"50 mg / ml injektionsvätska, lösning, förfyllda sprutor" 24 förfyllda sprutor med 0,50 ml med separat subkutan nål.
09.0 DATUM FÖR FÖRSTA GODKÄNNANDE ELLER FÖRNYELSE AV GODKÄNNANDET
Datum för första godkännandet: 29.12.2009
Datum för senaste förnyelse: 29.12.2014
10.0 DATUM FÖR ÖVERSYN AV TEXTEN
16 februari 2015