Aktiva ingredienser: Fusidinsyra, hydrokortison (hydrokortisonacetat)
FUCIDIN H 20 mg / g + 10 mg / g grädde
Varför används Fucidin H? Vad är det för?
Fucidin H-kräm kombinerar antibakteriell aktivitet av fusidinsyra (antibiotikum) med den antiinflammatoriska effekten av hydrokortisonacetat (kortikosteroid).
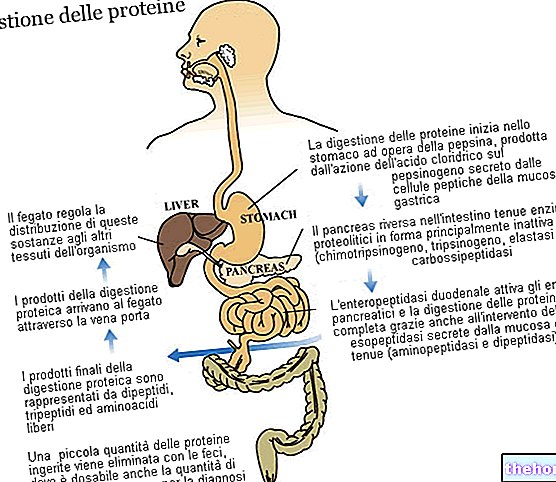
Det används för lokal behandling av infekterad atopisk dermatit (allmänt känd som eksem, en hudsjukdom som åtföljs av inflammation, rodnad, utsöndring eller sårskorpor och klåda, ofta av allergiskt ursprung).
Tala med din läkare om du inte mår bättre eller om du mår sämre.
Kontraindikationer När Fucidin H inte ska användas
Använd inte Fucidin H:
- om du är allergisk mot fusidinsyra, natriumfusidat, hydrokortisonacetat eller något annat innehållsämne i detta läkemedel (anges i avsnitt 6).
- om du har en "hudinfektion som främst orsakas av bakterier, svampar eller virus (som herpes eller vattkoppor)
- om du har tuberkulos
- om du har dermatit runt munnen
- om du har rosacea (svår rodnad i ansiktet).
Försiktighetsåtgärder för användning Vad du behöver veta innan du tar Fucidin H.
- Tala med din läkare eller apotekspersonal innan du använder Fucidin H.
- Fucidin H ska appliceras försiktigt på områden nära ögonen. Fucidin H får inte komma in i ögonen.
- Användningen av Fucidin H är begränsad till 2 veckor. Långvariga behandlingar kan öka risken för biverkningar och risken för antibiotikaresistens, till exempel kan din hud bli tunn.
- Fucidin H kan maskera symptom på en potentiell infektion
- Fucidin H kan öka sin mottaglighet för infektioner, förvärra befintliga infektioner och aktivera latenta infektioner.
Barn och ungdomar
Fucidin H ska användas med försiktighet till barn.
Interaktioner Vilka läkemedel eller livsmedel kan ändra effekten av Fucidin H
H Tala om för din läkare eller apotekspersonal om du tar eller nyligen har tagit eller kan tänkas ta andra läkemedel.
Varningar Det är viktigt att veta att:
Graviditet och amning
Om du är gravid eller ammar, tror att du kan vara gravid eller planerar att skaffa barn, rådfråga din läkare eller apotekspersonal innan du tar detta läkemedel.
Användning under graviditet och amning bör utvärderas och fastställas av en läkare.
Fucidin H ska användas med försiktighet under graviditet.
Fucidin H kan användas under amning men det rekommenderas att undvika att använda det på bröstet.
Effekter på förmågan att framföra fordon och använda maskiner
Behandling med Fucidin H -kräm påverkar inte körning och användning av maskiner.
Fucidin H innehåller butylhydroxianisol (E320), cetylalkohol och kaliumsorbat (E202)
Dessa komponenter kan orsaka lokala hudreaktioner (t.ex. kontaktdermatit). Butylhydroxianisol kan också orsaka irritation i ögon och slemhinnor (såsom näspassager och läppar).
Dos, metod och administreringstid Hur man använder Fucidin H: Dosering
Använd alltid detta läkemedel enligt läkarens anvisningar. Kontakta din läkare eller apotekspersonal om du är osäker.
Den rekommenderade dosen för barn, ungdomar och vuxna är: Applicera försiktigt ett tunt lager av krämen på det sjuka området i huden, tre gånger om dagen.Fucidin H ska inte användas på mer än 2 veckor.
Tvätta händerna noggrant efter varje applicering, såvida inte händerna är det område som ska behandlas.
Överdosering Vad du ska göra om du har tagit för mycket Fucidin H.
Om du har använt för stor mängd av Fucidin H
Kontakta din läkare eller apotekspersonal om du har använt mer grädde än du borde.
Om du har glömt att använda Fucidin H.
Om du glömmer att applicera krämen vid den schemalagda tiden, applicera den så snart som möjligt och fortsätt sedan behandlingen som vanligt.
Om du slutar att ta Fucidin H.
Om du glömmer att använda detta läkemedel, använd det så snart du kommer ihåg det. Använd sedan medicinen vid vanlig tidpunkt.
Om du har ytterligare frågor om användningen av Fucidin H, fråga din läkare eller apotekspersonal.
Biverkningar Vilka är biverkningarna av Fucidin H.
Liksom alla läkemedel kan Fucidin H orsaka biverkningar men alla användare behöver inte få dem.
Vanliga biverkningar (drabbar 1 till 10 användare av 100)
- reaktion på applikationsstället (t.ex. hudirritation, brännande hud eller klåda)
Mindre vanliga biverkningar (drabbar 1 till 10 användare av 1000)
- överkänslighet kontaktdermatit förvärring av eksemutslag
Andra biverkningar orsakade av långvarig behandling med milda kortikosteroider som hydrokortison inkluderar:
- gallring av huden (hudatrofi)
- dermatit
- bristningar (striae)
- utvidgning av små kärl på huden
- ihållande rodnad i ansiktet (rosacea)
- rodnad i huden (erytem)
- depigmentering
- överdriven hårväxt (hypertrikos)
- överdriven svettning (hyperhidros)
- blåmärken
- systemiska biverkningar orsakade av milda kortikosteroider som hydrokortison, inkluderar adrenal suppression särskilt vid långvarig topikal administrering
- komplikationer om de ges för nära ögonen (t.ex. ökat intraokulärt tryck och glaukom).
Tala med din läkare eller apotekspersonal om du får några biverkningar. Detta inkluderar eventuella biverkningar som inte nämns i denna bipacksedel.
Giltighetstid och lagring
Förvara detta läkemedel utom syn- och räckhåll för barn.
Använd inte detta läkemedel efter utgångsdatumet som anges på kartongen efter Utg.dat. Utgångsdatumet avser den sista dagen i månaden.
Detta läkemedel kräver inga särskilda förvaringsförhållanden.
Kasta inga läkemedel i avloppsvatten eller hushållsavfall. Fråga din apotekare om hur du ska kasta läkemedel som du inte längre använder. Detta hjälper till att skydda miljön.
Sammansättning och läkemedelsform
Vad Fucidin H
- De aktiva ingredienserna är fusidinsyra och hydrokortisonacetat. Varje gram grädde innehåller 20 mg fusidinsyra och 10 mg hydrokortisonacetat.
- Övriga innehållsämnen är butylhydroxianisol (E320), cetylalkohol, glycerol (85%), flytande paraffin, kaliumsorbat (E202), polysorbat 60, vit vaselin, all-rac-α-tokoferol, saltsyra och renat vatten.
Beskrivning av hur Fucidin H ser ut och förpackningens innehåll
Fucidin H är en vit kräm.
Varje förpackning innehåller en tub med 5, 15 eller 30 g grädde.
Alla förpackningsstorlekar kanske inte marknadsförs.
Bipacksedel: AIFA (Italian Medicines Agency). Innehåll publicerat i januari 2016. Den information som finns finns kanske inte uppdaterad.
För att få tillgång till den senaste versionen är det lämpligt att gå till AIFA (Italian Medicines Agency) webbplats. Ansvarsfriskrivning och användbar information.
01.0 LÄKEMEDLETS NAMN
FUCIDIN H, 20 MG / G + 10 MG / G CREAM
02.0 KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING
Fusidinsyra 20 mg / g och hydrokortisonacetat 10 mg / g.
Hjälpämnen med kända effekter:
Butylhydroxianisol E320 (40 mcg / g), cetylalkohol (111 mg / g) och kaliumsorbat E202 (2,7 mg / g).
För fullständig förteckning över hjälpämnen, se avsnitt 6.1.
03.0 LÄKEMEDELSFORM
Grädde.
Vit kräm blandbar i vatten.
04.0 KLINISK INFORMATION
04.1 Terapeutiska indikationer
Behandling av infekterad atopisk dermatit.
04.2 Dosering och administreringssätt
Vuxna och barnpopulation:
Fucidin H -kräm ska appliceras på drabbade hudområden 3 gånger om dagen, i upp till 2 veckor.
04.3 Kontraindikationer
Överkänslighet mot de aktiva substanserna eller mot något hjälpämne som anges i avsnitt 6.1.
På grund av kortikosteroiden som ingår är Fucidin H kontraindicerat under följande förhållanden:
Primära hudinfektioner orsakade av bakterier, svampar eller virus, antingen obehandlade eller inte kontrollerade med adekvat terapi (se avsnitt 4.4).
Hudmanifestationer relaterade till tuberkulösa processer antingen obehandlade eller inte kontrollerade av adekvat terapi. Perioral eller rosacea dermatit.
04.4 Särskilda varningar och lämpliga försiktighetsåtgärder vid användning
Långsiktig kontinuerlig lokal behandling med Fucidin H bör undvikas.
Beroende på applikationsstället bör man alltid tänka på eventuell förekomst av systemisk absorption av hydrokortisonacetat under behandling med Fucidin H.
Fucidin H ska användas med försiktighet i områden nära ögonen, på grund av kortikosteroiden det innehåller. Undvik att få Fucidin H i ögonen (se avsnitt 4.8).
Reversibelt undertryckande av hypothalamus-hypofys-adrenal (HPA) axel kan inträffa efter systemisk absorption av aktuella kortikosteroider.
Fucidin H ska användas med försiktighet till barn som som barn kan vara mer mottagliga för topisk kortikosteroidinducerad HPA-axelsuppression och Cushings syndrom än vuxna patienter (se avsnitt 4.8).
Fall av bakterieresistens har rapporterats i samband med användning av topisk fusidinsyra. Som med alla antibiotika kan långvarig eller återkommande användning av fusidinsyra öka risken för att utveckla antibiotikaresistens. Att begränsa fusidinsyra och aktuell hydrokortisonacetatbehandling till högst 14 dagar minskar risken för att utveckla resistens.
Detta kommer också att minska risken för att den immunsuppressiva effekten av kortikosteroiden kan dölja symtomen på en potentiell infektion orsakad av antibiotikaresistenta bakterier.
Fucidin H kan vara associerat med ökad känslighet för infektioner, förvärring av en befintlig infektion och aktivering av en latent infektion på grund av kortikosteroiders immunsuppressiva verkan. Att byta till systemisk behandling rekommenderas om infektion inte kan kontrolleras med lokal behandling (se avsnitt 4.3).
Fucidin H -kräm innehåller butylhydroxianisol, cetylalkohol och kaliumsorbat. Dessa hjälpämnen kan orsaka lokala hudreaktioner (t.ex. kontaktdermatit).
Butylhydroxianisol kan också orsaka irritation i ögon och slemhinnor.
Atrofiska förändringar kan uppstå i ansiktet och i mindre utsträckning i andra delar av kroppen efter långvarig behandling med aktuella kortikosteroider.
04.5 Interaktioner med andra läkemedel och andra former av interaktion
Inga interaktionsstudier har utförts. Interaktioner med systemiskt administrerade läkemedel anses vara minimala
04.6 Graviditet och amning
Graviditet
Fusidinsyra:
Inga effekter förväntas under graviditeten eftersom systemisk exponering för fusidinsyra är försumbar.
Hydrokortisonacetat:
En stor mängd data om gravida kvinnor (mer än 1000 graviditetsresultat) indikerar varken missbildningar eller foster- / neonatal toxicitet på grund av kortikosteroider.
Det finns otillräckliga kliniska data om behandling av gravida kvinnor med Fucidin H. Om det är kliniskt nödvändigt ska Fucidin H användas med försiktighet under graviditeten.
Matdags
Inga effekter på det nyfödda / spädbarnet som ammas förväntas eftersom systemisk exponering efter applicering av fusidinsyra och hydrokortisonacetat på ett begränsat område av den ammande kvinnans hud är försumbar.
Fucidin H kan användas under amning, men det rekommenderas att undvika att applicera Fucidin H på bröstet.
Fertilitet
Det finns inga kliniska studier med Fucidin H avseende fertilitet.
04.7 Effekter på förmågan att framföra fordon och använda maskiner
Fucidin H -kräm har ingen eller försumbar effekt på förmågan att framföra fordon eller använda maskiner.
04.8 Biverkningar
Uppskattningen av frekvensen av biverkningar är baserad på en "samlad analys av data från kliniska prövningar och spontana rapporter.
De vanligast rapporterade biverkningarna under behandlingen är reaktioner på applikationsstället inklusive klåda, sveda och irritation.
Biverkningar klassificeras med MedDRA System Organ Class (SOC) och enskilda biverkningar listas med början på de vanligaste rapporterade. Inom varje frekvensgrupp presenteras biverkningarna i fallande allvarlighetsgrad.
Mycket vanligt ≥ 1/10
Vanliga ≥ 1/100,
Mindre vanliga ≥ 1/1000,
Sällsynta ≥ 1/10 000,
Mycket sällsynt
Systemiska biverkningar relaterade till kortikosteroidklassen såsom hydrokortison inkluderar adrenal suppression särskilt vid långvarig topisk administrering (se avsnitt 4.4).
Ökat intraokulärt tryck och glaukom kan också uppstå efter topisk användning av kortikosteroider nära ögonen, särskilt vid långvarig användning och hos patienter som är predisponerade för att utveckla glaukom (se avsnitt 4.4).
Dermatologiska biverkningar relaterade till den lätta kortikosteroidklassen såsom hydrokortison inkluderar: atrofi, dermatit (inklusive kontaktdermatit, akneiform dermatit och perioral dermatit), hudstriae, telangiectasier, rosacea, erytem, depigmentering, hypertrichos och hyperhidros. Ekymi kan också uppstå med. långvarig användning av aktuella kortikosteroider.
Kortikosteroidrelaterade klasseffekter har ovanligt rapporterats för Fucidin H enligt beskrivning i frekvenstabellen ovan.
Pediatrisk population
Den observerade säkerhetsprofilen liknar barn och vuxna (se avsnitt 4.4).
04.9 Överdosering
För topiskt applicerad fusidinsyra finns ingen information tillgänglig om potentiella symtom och tecken på överdosering.Cushings syndrom och adrenal insufficiens kan utvecklas efter topisk applicering av stora mängder kortikosteroider i mer än tre veckor.
Systemiska konsekvenser av en överdos av de aktiva substanserna kommer sannolikt inte att inträffa efter oavsiktligt oralt intag Mängden fusidinsyra i ett rör Fucidin H överstiger inte den dagliga orala dosen av systemisk behandling. En enda oral överdos av kortikosteroider är sällan klinisk problem.
05.0 FARMAKOLOGISKA EGENSKAPER
05.1 Farmakodynamiska egenskaper
Farmakoterapeutisk grupp: Hydrokortison och antibiotika, ATC -kod: D07CA01
Fucidin H-kräm kombinerar fusidinsyras antibakteriella aktivitet med den antiinflammatoriska effekten av hydrokortisonacetat.
05.2 Farmakokinetiska egenskaper
Utbildning in vitro har visat att fusidinsyra kan tränga igenom intakt hud.Graden av penetration beror delvis på exponering och delvis på hudens skick.
Fusidinsyra utsöndras huvudsakligen i gallan och endast i liten utsträckning i urinen.
Hydrokortisonacetat absorberas efter topisk applicering. Absorptionsgraden beror dels på hudens skick och dels på appliceringsstället. Det absorberade hydrokortisonen metaboliseras snabbt och utsöndras i urinen.
05.3 Prekliniska säkerhetsdata
Bortsett från vad som beskrivs i de andra avsnitten av produktresumén finns inga andra prekliniska data som är relevanta för förskrivaren tillgängliga.
06.0 LÄKEMEDELSINFORMATION
06.1 Hjälpämnen
Butylhydroxianisol (E320), cetylalkohol, glycerol (85%), flytande paraffin, kaliumsorbat (E202), polysorbat 60, vit vaselin, all-rac-α-tokoferol, saltsyra och renat vatten.
06.2 Oförenlighet
Okänt.
06.3 Giltighetstid
3 år.
Giltighetstid efter första öppnandet: 3 månader.
06.4 Särskilda förvaringsanvisningar
Förvaras vid högst 30 ° C.
06.5 Förpackningens innehåll och förpackningens innehåll
Aluminiumrör med skruvlock av polyeten.
Förpackning: 5 g, 15 g och 30 g.
Alla förpackningsstorlekar kanske inte marknadsförs.
06.6 Anvisningar för användning och hantering
Inga speciella instruktioner.
Oanvänd medicin och avfall från detta läkemedel måste kasseras i enlighet med lokala föreskrifter.
07.0 INNEHAVARE AV GODKÄNNANDE FÖR FÖRSÄLJNING
LEO PharmaA / S
Industriparken 55
DK-2750 Ballerup
Danmark
Återförsäljare för Italien: LEO Pharma S.p.A. Via Amsterdam 125 00144 Rom.
08.0 NUMMER FÖR FÖRSÄLJNINGSTILLSTÅND
5 g rör - A.I.C. n. 034560033
15 g rör - A.I.C. n. 034560019
Rör 30 g - A.I.C. n. 034560021
09.0 DATUM FÖR FÖRSTA GODKÄNNANDE ELLER FÖRNYELSE AV GODKÄNNANDET
Datum för första godkännandet: 4 februari 2000
Datum för senaste förnyelse: 4 juni 2007
10.0 DATUM FÖR ÖVERSYN AV TEXTEN
4 september 2014