Aktiva ingredienser: Betahistine
Jarapp 24 mg tabletter
Indikationer Varför används Jarapp? Vad är det för?
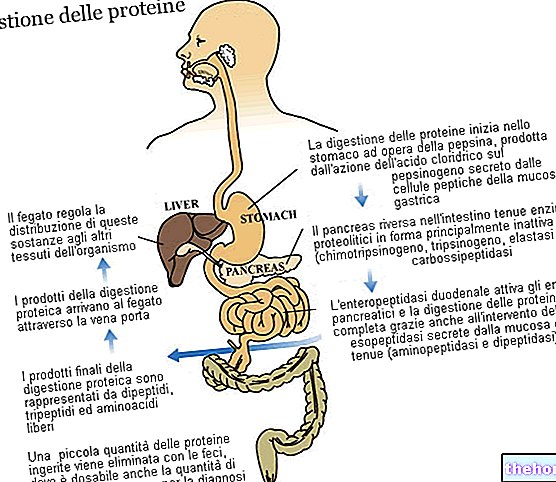
Jarapp är ett läkemedel som används för att behandla symptom på Ménières syndrom, såsom yrsel, ringningar i öronen, hörselnedsättning och illamående.
Kontraindikationer När Jarapp inte ska användas
Du använder inte Jarapp
- om du är allergisk mot betahistin eller något annat innehållsämne i detta läkemedel (anges i avsnitt 6)
- om du har feokromocytom, en sällsynt tumör i binjurarna
- om du är under 18 år
Försiktighetsåtgärder för användning Vad du behöver veta innan du tar Jarapp
Tala med din läkare eller apotekspersonal innan du tar Jarapp
- om du tidigare har eller har lidit av ett magsår (magsår)
- om du lider av astma
- om du har nässelfeber, utslag eller allergisk förkylning, eftersom dessa kan bli värre
- om du har lågt blodtryck
Om du har något av ovanstående tillstånd, kontakta din läkare för att ta reda på om du kan ta betahistin.
Dessa patientgrupper bör övervakas av en läkare under behandlingen.
Interaktioner Vilka droger eller livsmedel kan förändra effekten av Jarapp
En "interaktion innebär att läkemedel eller ämnen, när de tas samtidigt, kan påverka hur de fungerar eller deras biverkningar.
Hittills har inga interaktioner observerats mellan betahistin och andra läkemedel.
Betahistin kan påverka effekten av antihistaminer. Antihistaminer är läkemedel som används särskilt för att behandla allergier, såsom hösnuva och bilsjukdom. Rådgör med din läkare eller apotekspersonal om du tar antihistaminer (allergimedicin) samtidigt.
Försiktighet rekommenderas vid samtidig användning av betahistin och MAO -hämmare. MAO -hämmare är läkemedel som används särskilt för behandling av depression.
Tala om för din läkare eller apotekspersonal om du tar, nyligen har tagit eller kan tänkas ta andra läkemedel.
Varningar Det är viktigt att veta att:
Graviditet och amning
Det är inte känt om det är säkert att ta betahistin under graviditeten. Därför ska detta läkemedel inte användas under graviditet om det inte är absolut nödvändigt.
Det är inte känt om betahistin utsöndras i bröstmjölk. Därför bör du diskutera amning med din läkare som kan hjälpa dig att avgöra vad som är bäst för dig och ditt barn utifrån fördelarna och riskerna med detta läkemedel.
Fråga din läkare eller apotekspersonal om råd innan du tar detta eller något annat läkemedel.
Köra och använda maskiner
Betahistine har ingen eller försumbar effekt på förmågan att framföra fordon eller använda maskiner.
Jarapp innehåller laktosmonohydrat
Om din läkare har fått veta att du inte tål vissa sockerarter, kontakta din läkare innan du tar detta läkemedel.
Dos, metod och administreringstid Hur man använder Jarapp: Dosering
Ta alltid detta läkemedel enligt läkarens eller apotekspersonalens anvisningar. Kontakta din läkare eller apotekspersonal om du är osäker.
Rekommenderad dos är:
Vuxna
Från en halv tablett till en tablett, två gånger om dagen. Det kan ta upp till 2 veckor innan du märker någon förbättring.
Hur du tar Jarapp
Det är bäst att ta tabletterna med mat.
Om du har glömt att ta Jarapp
Vänta vid vanlig tid för att ta din nästa dos. Ta inte en dubbel dos för att kompensera för en glömd tablett.
Fråga din läkare eller apotekspersonal om du har ytterligare frågor om användningen av detta läkemedel.
Överdosering Vad du ska göra om du har tagit för mycket Jarapp
Kontakta din läkare om du har tagit mer än den föreskrivna dosen.
Symtom på en överdos av betahistin på upp till 640 mg kan vara milda till måttliga i intensitet, såsom illamående, dåsighet, kräkningar, matsmältningsstörningar, buksmärtor och koordinationsstörningar. Högre doser betahistin kan orsaka allvarligare symtom, såsom anfall, hjärt- och lungproblem och anfall.
Biverkningar Vilka är biverkningarna av Jarapp
Liksom alla läkemedel kan detta läkemedel orsaka biverkningar men alla användare behöver inte få dem. Följande biverkningar kan förekomma ofta (kan förekomma hos upp till 1 av 10 personer):
Gastrointestinala störningar
- Illamående och dyspepsi
Nervsystem
- Huvudvärk
Frekvensen av följande biverkningar är okänd:
Störningar i immunsystemet
- Överkänslighetsreaktioner såsom en allvarlig allergisk reaktion (anafylaksi).
Hudsjukdomar
- Överkänslighetsreaktioner (ibland svåra), särskilt svullnad i huden (angioneurotiskt ödem), nässelfeber, utslag, klåda
Gastrointestinala störningar
- Gastrointestinala störningar.
- Milda gastrointestinala störningar (t.ex. kräkningar, mag -tarmvärk, uppblåsthet, illamående, matsmältningsstörningar) försvinner vanligtvis genom att ta medicinen i samband med måltider. Alternativt, efter samråd med din läkare, kan dosen minskas.
Nervsystemet
- Dåsighet
Tala om för din läkare eller apotekspersonal om någon av biverkningarna blir allvarlig eller om du märker några biverkningar som inte nämns i denna bipacksedel.
Rapportering av biverkningar
Tala med din läkare eller apotekspersonal om du får några biverkningar. Detta inkluderar eventuella biverkningar som inte nämns i denna bipacksedel. Du kan också rapportera biverkningar direkt via det nationella rapporteringssystemet som anges i bilaga V. Genom att rapportera biverkningar kan du hjälpa till att ge mer information om läkemedlets säkerhet.
Giltighetstid och lagring
Förvara detta läkemedel utom syn- och räckhåll för barn.
Använd inte detta läkemedel efter utgångsdatumet som står på blister och kartong efter "EXP". Utgångsdatumet avser den sista dagen i månaden.
Förvara Jarapp vid 25 ° C på en torr plats och i originalförpackningen.
Kasta inga läkemedel i avloppsvatten eller hushållsavfall. Fråga din apotekare om hur du ska kasta läkemedel som du inte använder längre. Detta skyddar miljön.
Annan information
Vad Jarapp innehåller
Den aktiva ingrediensen är betahistindihydroklorid.
En tablett innehåller 24 mg betahistindihydroklorid.
Övriga innehållsämnen är povidon, mikrokristallin cellulosa, laktosmonohydrat, vattenfri kolloidal kiseldioxid, krospovidon och stearinsyra.
Beskrivning av Jarapps utseende och paketets innehåll
Rund, bikonvex, vit till benvit tablett, märkt på ena sidan.
Tabletten kan delas i lika stora halvor.
Finns i kartonger med 20, 30, 40, 50, 60 eller 100 tabletter förpackade i blister.
Alla förpackningsstorlekar kanske inte marknadsförs.
Bipacksedel: AIFA (Italian Medicines Agency). Innehåll publicerat i januari 2016. Den information som finns finns kanske inte uppdaterad.
För att få tillgång till den senaste versionen är det lämpligt att gå till AIFA (Italian Medicines Agency) webbplats. Ansvarsfriskrivning och användbar information.
01.0 LÄKEMEDLETS NAMN
JARAPP 24 MG -TABLETTER
02.0 KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING
En tablett innehåller 24 mg betahistindihydroklorid.
Hjälpämne med kända effekter:
En tablett innehåller 210 mg laktosmonohydrat.
För fullständig förteckning över hjälpämnen, se avsnitt 6.1
03.0 LÄKEMEDELSFORM
Läsplatta.
Vit till benvit, rund, bikonvex tablett, på ena sidan. Tabletten kan delas i lika stora halvor.
04.0 KLINISK INFORMATION
04.1 Terapeutiska indikationer
Betahistine är indicerat för behandling av Ménières syndrom, vars symtom kan innefatta yrsel, tinnitus, hörselnedsättning och illamående.
04.2 Dosering och administreringssätt
Dosering
Vuxna (inklusive äldre):
12-24 mg två gånger om dagen, med måltider.
Doseringen kan justeras efter den enskilda patientens behov. Ibland är det möjligt att observera förbättringar först efter ett par veckors behandling.
Pediatrisk population:
För barn under 18 år rekommenderas inte användning av Jarapp -tabletter på grund av otillräckliga data om säkerhet och effekt.
04.3 Kontraindikationer
Överkänslighet mot den aktiva substansen eller mot något hjälpämne som anges i avsnitt 6.1.
Feokromocytom.
Eftersom betahistin är en syntetisk analog av histamin kan det orsaka frisättning av katekolaminer från tumören, vilket resulterar i svår hypertoni.
04.4 Särskilda varningar och lämpliga försiktighetsåtgärder vid användning
Försiktighet iakttas vid behandling av patienter med magsår eller som tidigare har haft magsår på grund av då och då dyspepsi som ses hos patienter behandlade med betahistin.
Patienter med bronkial astma och en historia av magsår bör övervakas noggrant under behandlingen.
Försiktighet iakttas vid förskrivning av betahistin till patienter med urtikaria, utslag eller allergisk rinit, på grund av risken för att dessa symtom försämras.
Försiktighet rekommenderas hos patienter med svår hypotoni.
Patienter med sällsynta ärftliga problem med galaktosintolerans, Lapp-laktasbrist eller glukos-galaktosmalabsorption bör inte ta detta läkemedel.
04.5 Interaktioner med andra läkemedel och andra former av interaktion
Det finns inga kända fall av farliga interaktioner.
Det finns en rapport om en "interaktion med etanol och en förening som innehåller pyrimetamin och dapson och en annan om att förstärka effekterna av betahistin med salbutamol."
Inga interaktionsstudier har utförts in vivo. Baserat på data in vitro inte väntad, in vivo, en "hämning av cytokrom P450 -enzymer.
Uppgifterna in vitro indikerar en "hämning av betahistinmetabolism av läkemedel som hämmar monoaminoxidas (MAO), inklusive MAO-B-undertypen (t.ex. selegilin). Försiktighet rekommenderas vid användning av betahistin- och MAO-hämmare (inklusive hämmare) samtidigt. selektiv MAO-B).
Eftersom betahistin är en histaminanalog kan Jarapps interaktion med antihistaminer teoretiskt påverka effekten av ett av dessa läkemedel.
04.6 Graviditet och amning
Graviditet:
Det finns inga adekvata data om användning av betahistin under graviditet.
Djurstudier är otillräckliga för att påvisa effekter på graviditet, embryonal / fosterutveckling, förlossning och postnatal utveckling (se avsnitt 5.3). Den potentiella risken för människor är okänd. Jarapp ska inte användas under graviditet om det inte är absolut nödvändigt.
Matdags:
Det är inte känt om betahistin utsöndras i bröstmjölk. Det finns inga djurstudier avseende utsöndring av betahistin i mjölk. Läkemedlets betydelse för modern måste vägas mot fördelarna med amning och de potentiella riskerna för barnet.
04.7 Effekter på förmågan att framföra fordon och använda maskiner
Betahistine är indicerat för Ménières sjukdom och symtomatisk yrsel. Båda sjukdomarna kan påverka förmågan att framföra fordon och använda maskiner negativt. I kliniska studier specifikt genomförda för att undersöka förmågan att framföra fordon och använda maskiner hade betahistin ingen eller försumbar effekt.
04.8 Biverkningar
Följande biverkningar observerades vid de frekvenser som anges nedan hos patienter som behandlats med betahistin under placebokontrollerade kliniska prövningar [mycket vanligt (≥ 1/10); vanliga (≥ 1/100,
Gastrointestinala störningar
Vanliga: illamående och dyspepsi
Nervsystemet
Vanlig: huvudvärk
Utöver de händelser som rapporterats i kliniska studier har följande biverkningar spontant rapporterats under marknadsföring och i litteraturen. En exakt frekvens kan inte uppskattas utifrån tillgängliga data och klassificeras därför som "okänd".
Störningar i immunsystemet
Överkänslighetsreaktioner såsom anafylaksi.
Gastrointestinala störningar
Magtarmkanalen har rapporterats.
Milda magstörningar (t.ex. kräkningar, mag -tarmvärk, uppblåsthet i buken och uppblåsthet). Dessa kan vanligtvis lösas genom att ta läkemedlet med måltider eller genom att minska dosen.
Hud och subkutan vävnad
Överkänslighetsreaktioner i huden och subkutan, särskilt angioneurotiskt ödem, urtikaria, utslag och klåda.
Nervsystemet
Somnolens har rapporterats.
Rapportering av misstänkta biverkningar
Rapportering av misstänkta biverkningar som inträffar efter godkännande av läkemedlet är viktigt eftersom det möjliggör kontinuerlig övervakning av nytta / riskbalansen för läkemedlet.Hälso- och sjukvårdspersonal uppmanas att rapportera alla misstänkta biverkningar via det nationella rapporteringssystemet *.
04.9 Överdosering
Få fall av överdosering har rapporterats. Vissa patienter har upplevt milda till måttliga symtom (t.ex. illamående, somnolens, buksmärtor) vid doser upp till 640 mg. Mer allvarliga komplikationer (t.ex. kramper, lung- eller hjärtkomplikationer) har rapporterats vid avsiktlig överdos av betahistin, särskilt i kombination med andra överdoserade läkemedel. Behandling av överdos bör inkludera standardstödjande åtgärder.
05.0 FARMAKOLOGISKA EGENSKAPER
05.1 Farmakodynamiska egenskaper
Farmakoterapeutisk grupp: antivertigo -preparat, ATC -kod: N07C A01
Betahistines H1-agonistaktivitet på histaminerga receptorer i perifera blodkärl har påvisats hos människor genom inhibering av betahistininducerad vasodilatation av histaminantagonisten difenhydramin. Betahistine har minimala effekter på magsyrasekretion (ett svar). Medierat av H2-receptorn).
Betahistins verkningsmekanism vid Ménières syndrom är oklart.Effekten av betahistin vid behandling av yrsel kan bero på dess förmåga att modifiera cirkulationen i innerörat eller på en direkt effekt på neuroner i vestibulära kärnor.
Enstaka orala doser av betahistin, upp till 32 mg hos normala patienter, resulterade i maximal undertryckning av inducerad vestibulär nystagmus 3 till 4 timmar efter dosering; högre doser visade sig vara mer effektiva för att minska varaktigheten av nystagmus.
Lungepitelets permeabilitet hos människor ökas med betahistin. Detta berodde på en minskning av clearance -tiden för en radioaktiv markör från lungan till blodet. Denna åtgärd förhindras genom oral förbehandling med terfenadin, en känd H1 -receptorblockerare.
Medan histamin har positiva inotropa effekter på hjärtat, är det inte känt om betahistin ökar hjärtoutflödet och dess vasodilaterande effekt kan orsaka en mild sänkning av blodtrycket hos vissa patienter.
Betahistin har liten effekt på de exokrina körtlarna hos människor.
05.2 Farmakokinetiska egenskaper
Absorption
Betahistin absorberas helt efter oral administrering och maximala plasmakoncentrationer av 14C-märkt betahistin uppnås hos fastande patienter cirka 1 timme efter oralt intag.
Eliminering
Eliminering av betahistin sker främst genom metabolism och metaboliterna elimineras därefter främst genom renal utsöndring. 85-90% av radioaktiviteten för en 8 mg dos uppträder i urinen under 56 timmar, med en maximal utsöndring som uppnås inom 2 timmar efter intag. Efter oral administrering av betahistin är dess plasmanivåer mycket låga. Därför är utvärderingen av de farmakokinetiska parametrarna för betahistin baserad på data avseende plasmakoncentrationen av metaboliten 2-pyridylättiksyra enbart.
Biotransformation
Det finns inga tecken på presystemisk metabolism och biliär utsöndring anses inte vara en viktig väg för eliminering av läkemedlet eller en av dess metaboliter. Det finns ingen eller nästan ingen bindning till humana plasmaproteiner, men betahistin utsätts för metabolism i levern. Ungefär 80-90% av den dos som tas tas ut i urinen.
05.3 Prekliniska säkerhetsdata
Studier av toxicitet vid upprepade doser hos hundar som varade 6 månader och 18 månader hos albinoråttor avslöjade inga kliniskt relevanta biverkningar vid doser från 2,5 till 120 mg / kg. Betahistin har ingen mutagen potential och det finns inga tecken på cancerframkallande egenskaper hos råttor. Tester utförda på dräktiga kaniner avslöjade inga tecken på teratogena effekter.
06.0 LÄKEMEDELSINFORMATION
06.1 Hjälpämnen
Povidon K90,
Mikrokristallin cellulosa,
Laktosmonohydrat,
Vattenfri kolloidal kiseldioxid,
Crospovidon,
Stearinsyra.
06.2 Oförenlighet
Inte relevant.
06.3 Giltighetstid
3 år
06.4 Särskilda förvaringsanvisningar
Förvaras vid högst 25 ° C i originalförpackningen.
06.5 Förpackningens innehåll och förpackningens innehåll
Aluminium / PVC / PVDC blister.
Finns i förpackningar med 20, 30, 40, 50, 60 och 100 tabletter.
Alla förpackningsstorlekar kanske inte marknadsförs.
06.6 Anvisningar för användning och hantering
Inga speciella instruktioner.
07.0 INNEHAVARE AV GODKÄNNANDE FÖR FÖRSÄLJNING
Alfa Wassermann S.p.A. Via E. Fermi 1, 65020 - Alanno (PE) - Italien
08.0 NUMMER FÖR FÖRSÄLJNINGSTILLSTÅND
24 mg tabletter 20 tabletter i PVC / PVDC / AL -blister - AIC 038836019
24 mg tabletter 30 tabletter i PVC / PVDC / AL -blister - AIC 038836021
24 mg tabletter 40 tabletter i PVC / PVDC / AL -blister - AIC 038836033
24 mg tabletter 50 tabletter i PVC / PVDC / AL -blister - AIC 038836045
24 mg tabletter 60 tabletter i PVC / PVDC / AL -blister - AIC 038836058
24 mg tabletter 100 tabletter i PVC / PVDC / AL -blister - AIC 038836060
09.0 DATUM FÖR FÖRSTA GODKÄNNANDE ELLER FÖRNYELSE AV GODKÄNNANDET
Datum för första godkännandet: 10 april 2009
Datum för senaste förnyelse: 31 augusti 2012