Aktiva ingredienser: Ticagrerol
Brilique 90 mg filmdragerade tabletter
Varför används Brilique? Vad är det för?
Vad är Brilique
Brilique innehåller den aktiva substansen som kallas ticagrelor, som tillhör en grupp läkemedel som kallas trombocythämmande medel.
Hur Brilique fungerar
Brilique fungerar på celler som kallas "trombocyter" (även kallade trombocyter). Dessa mycket små blodkroppar hjälper till att stoppa blödning genom att klumpa ihop sig för att stänga de små hålen i avskurna eller skadade blodkärl.
Trombocyter kan dock också bilda blodproppar i de sjuka blodkärlen i hjärtat och hjärnan. Detta kan vara mycket farligt eftersom:
- blodproppen kan helt stänga av blodtillförseln - detta kan orsaka hjärtinfarkt (hjärtinfarkt) eller stroke, eller
- blodproppen kan delvis blockera blodkärlen som försörjer hjärtat - detta minskar blodflödet till hjärtat och kan orsaka bröstsmärta som kommer och går (kallas "instabil angina"). Brilique hjälper till att blockera att blodplättar klumpas ihop, vilket minskar risken för blodpropp som kan minska blodflödet.
Vad är Brilique för
Brilique i kombination med acetylsalicylsyra (ett annat trombocythämmande medel) ska endast användas hos vuxna patienter.
Hon ordinerades Brilique eftersom hon hade:
- en hjärtinfarkt, eller
- instabil angina (angina eller bröstsmärta som inte är välkontrollerad).
Brilique minskar risken för att du får en annan hjärtinfarkt eller stroke eller dör av hjärt- eller blodkärlsrelaterad sjukdom.
Kontraindikationer När Brilique inte ska användas
Ta inte Brilique om:
- Du är allergisk mot ticagrelor eller något annat innehållsämne i Brilique
- Han har pågående blödningar
- Han fick en stroke orsakad av blödning i hjärnan.
- Du har måttliga till svåra leverproblem.
- Du tar något av följande läkemedel: ketokonazol (används för att behandla svampinfektioner), klaritromycin (används för att behandla bakterieinfektioner), nefazodon (ett antidepressivt medel), ritonavir och atazanavir (används för att behandla HIV -infektion och aids)).
Ta inte Brilique om något av ovanstående gäller dig. Om du är osäker, tala med din läkare eller apotekspersonal innan du tar Brilique
Försiktighetsåtgärder vid användning Vad du behöver veta innan du tar Brilique
Innan du tar Brilique, kontakta din läkare, apotekspersonal eller tandläkare om:
- Du har en ökad risk för blödning på grund av:
- en allvarlig skada nyligen
- en ny operation (inklusive tandkirurgi)
- en sjukdom som påverkar blodpropp - nyligen blödning från magen eller tarmarna (t.ex. på grund av magsår eller "polyper" i tjocktarmen)
- Du planerar att opereras (inklusive tandvård) när som helst medan du tar Brilique, eftersom det är en ökad risk för blödning. Din läkare kan berätta att du ska sluta ta Brilique 7 dagar före operationen.
- Din puls är ovanligt låg (vanligtvis mindre än 60 slag per minut) och du har inte redan implanterat ett instrument som reglerar hjärtrytmen (pacemaker).
- Du har astma eller annat lungproblem eller andningssvårigheter.
- Han har redan tagit blodprov som visade mer urinsyra än normalt. Om något av ovanstående gäller dig (eller om du är osäker), tala med din läkare, apotekspersonal eller tandläkare innan du tar Brilique.
Barn och ungdomar
Brilique rekommenderas inte för barn och ungdomar under 18 år.
Interaktioner Vilka mediciner eller livsmedel kan förändra effekten av Brilique
Tala om för din läkare eller apotekspersonal om du tar, nyligen har tagit eller kan tänkas ta andra läkemedel. Detta beror på att Brilique kan påverka hur vissa läkemedel fungerar, och vissa läkemedel kan påverka Brilique.
Tala om för din läkare eller apotekspersonal om du tar något av följande läkemedel:
- mer än 40 mg simvastatin eller lovastatin per dag (läkemedel som används för att behandla högt kolesterol)
- rifampicin (ett antibiotikum), fenytoin, karbamazepin och fenobarbital (används för att kontrollera anfall), digoxin (används för att behandla hjärtsvikt), cyklosporin (används för att sänka kroppens försvar), kinidin och diltiazem (används för att behandla hjärtsvikt) onormal hjärtrytm ), betablockerare och verapamil (används för att behandla högt blodtryck).
Tala särskilt om för din läkare eller apotekspersonal om du tar något av följande läkemedel som ökar risken för blödning:
- "orala antikoagulantia" kallas ofta "blodförtunnare", som inkluderar warfarin.
- icke-steroida antiinflammatoriska läkemedel (förkortas som NSAID), används ofta som smärtstillande medel, såsom ibuprofen och naproxen.
- selektiva serotoninåterupptagshämmare (förkortade som SSRI) som antidepressiva medel, såsom paroxetin, sertralin och citalopram.
- andra läkemedel som ketokonazol (används för att behandla svampinfektioner), klaritromycin (används för att behandla bakterieinfektioner), nefazodon (ett antidepressivt medel), ritonavir och atazanavir (används för att behandla HIV -infektion och aids), cisaprid (används för att behandla halsbränna) eller ergot alkaloider (används för att behandla migrän och huvudvärk).
Tala också om för din läkare att eftersom du tar Brilique kan du ha en ökad risk för blödning om din läkare ordinerar fibrinolytika, ofta kallade 'trombolytika', såsom streptokinas eller alteplas.
Varningar Det är viktigt att veta att:
Graviditet och amning
Användning av Brilique rekommenderas inte om du är gravid eller misstänker graviditet. Kvinnor bör använda lämpliga preventivmetoder för att undvika att bli gravida när de tar detta läkemedel. Tala med din läkare innan du tar Brilique om du ammar. Din läkare kommer att diskutera fördelar och risker med Brilique -behandling med dig under denna tid.
Om du är gravid eller ammar, tror att du kan vara gravid eller planerar att skaffa barn, rådfråga din läkare eller apotekspersonal innan du tar detta läkemedel.
Köra och använda maskiner
Det är osannolikt att Brilique påverkar din förmåga att framföra fordon eller använda maskiner. Om du känner dig yr när du tar Brilique, var försiktig när du kör eller använder maskiner
Dos, metod och administreringstid Hur man använder Brilique: Dosering
Ta alltid detta läkemedel enligt läkarens eller apotekspersonalens anvisningar. Kontakta din läkare eller apotekspersonal om du är osäker.
Hur mycket Brilique att ta
- Startdosen är två tabletter samtidigt (180 mg laddningsdos). Denna dos kommer normalt att ges till dig på sjukhuset.
- Efter denna startdos är den vanliga dosen en 90 mg tablett två gånger om dagen i upp till 12 månader, såvida inte din läkare säger till dig något annat. Ta Brilique vid ungefär samma tid varje dag (till exempel en tablett på morgonen och en på kvällen).
Din läkare brukar säga till dig att ta acetylsalicylsyra också. Detta är ett ämne som finns i många läkemedel som används för att förhindra blodproppar. Din läkare kommer att berätta hur mycket du ska ta (vanligtvis mellan 75 och 150 mg per dag).
Hur du tar Brilique
- Du kan ta tabletten med eller utan måltider.
- Du kan kontrollera när du har tagit din senaste Brilique -tablett genom att titta på blisteret. Det finns en sol (för morgonen) och en måne (för kvällen). Detta kommer att berätta om du har tagit dosen.
Om du har svårt att svälja tabletten
Om du har svårt att svälja tabletten kan du krossa den och blanda den med vatten enligt följande:
- Krossa tabletten / tabletterna till ett fint pulver
- Häll pulvret i ett halvt glas vatten
- Rör om och drick omedelbart
- Skölj det tomma glaset med ett halvt glas vatten och drick för att vara säker på att du inte har lämnat någon medicin.
Överdosering Vad du ska göra om du har tagit för mycket Brilique
Om du har tagit mer Brilique än du borde
Om du har tagit mer Brilique än du borde, kontakta din läkare eller gå till sjukhuset omedelbart. Ta med dig medicinförpackningen. Du kan ha ökad risk för blödning.
Om du har glömt att ta Brilique
- Om du glömmer att ta en dos, ta bara nästa dos som vanligt.
- Ta inte en dubbel dos (två doser samtidigt) för att kompensera för en glömd dos.
Om du slutar att ta Brilique
Sluta inte ta Brilique utan att först tala med din läkare. Ta Brilique regelbundet och så länge din läkare ordinerar det åt dig.
Om du slutar att ta Brilique kan det öka risken för att du får en annan hjärtinfarkt eller stroke eller att du dör av en sjukdom relaterad till hjärt- eller blodkärlsproblem.
Om du har ytterligare frågor om användningen av detta läkemedel, fråga din läkare eller apotekspersonal
Biverkningar Vilka är biverkningarna av Brilique
Liksom alla läkemedel kan detta läkemedel orsaka biverkningar men alla användare behöver inte få dem.
Följande biverkningar kan uppstå med detta läkemedel:
Kontakta en läkare omedelbart om du märker något av följande symptom - du kan behöva akut läkarvård:
- Blödning i hjärnan eller inuti skallen är en ovanlig biverkning och kan orsaka tecken på stroke, såsom:
- plötslig domningar eller svaghet i armar, ben eller ansikte, särskilt om det bara är på ena sidan av kroppen
- plötslig förvirring, svårigheter att tala eller förstå andra
- plötsliga svårigheter att gå eller förlora balans eller koordination - plötslig yrsel eller plötslig intensiv huvudvärk utan känd orsak
- Blödning - viss blödning är vanlig. Men allvarliga blödningar är inte vanligt, men det kan vara livshotande. Olika typer av blödningar kan ökas, till exempel:
- blödning som är svår eller inte kan kontrolleras
- oväntade blödningar eller blödningar som varar länge
- förekomst av blod i urinen
- produktion av svart avföring eller rött blod i avföringen
- synstörningar orsakade av närvaron av blod i ögonen
- blodproppar frigörs genom hosta eller kräkningar
- blödning inuti lederna som resulterar i svullnad och smärta
Kontakta din läkare om du märker något av följande symtom:
- Känner andfådd - denna förekomst är vanlig. Det kan bero på din hjärtsjukdom eller någon annan orsak, eller det kan vara en bieffekt av Brilique. Om din väsande andning blir värre eller varar med tiden, tala om för din läkare. Din läkare kommer att avgöra om du behöver behandling eller fortsätta med ytterligare undersökningar .
Andra möjliga biverkningar
Vanliga (kan förekomma hos upp till 1 av 10 personer)
- Blåmärken
- Näsblod
- Mer riklig blödning från operation, skärsår eller sår
Mindre vanliga (kan förekomma hos upp till 1 av 100 personer)
- Allergisk reaktion - utslag, klåda eller svullnad i ansikte eller läppar / tunga kan vara tecken på en allergisk reaktion
- Huvudvärk
- Yrsel eller som om rummet snurrar
- Buksmärtor
- Diarré eller matsmältningsbesvär
- Mår eller mår dåligt
- Utslag
- Klåda
- Inflammation i magen (gastrit)
- Vaginal blödning som är mer intensiv eller inträffar vid andra tillfällen än normal menstruationsblödning
- Blödning från magväggarna (sår)
- Blödning från tandköttet
Sällsynta (kan förekomma hos upp till 1 av 1000 personer)
- Förstoppning
- Kittlande känsla
- förvirring
- Blod i öronen
- Inre blödning
Rapportering av biverkningar
Tala med din läkare eller apotekspersonal om du får några biverkningar. Detta inkluderar eventuella biverkningar som inte nämns i denna bipacksedel. Du kan också rapportera biverkningar direkt via det nationella rapporteringssystemet som anges i bilaga V.
Genom att rapportera biverkningar kan du hjälpa till att ge mer information om säkerheten för detta läkemedel.
Giltighetstid och lagring
Använd inte detta läkemedel efter utgångsdatum som anges på blister och kartong efter förkortningen EXP / EXP. Utgångsdatumet avser den sista dagen i den månaden. Kasta inga läkemedel via avloppsvatten eller hushållsavfall. Fråga din apotekare hur du ska kasta mediciner som du inte längre använder. Detta kommer att bidra till att skydda miljön.
Förpackningens innehåll och annan information
Vad Brilique innehåller
- Den aktiva ingrediensen är ticagrelor. Varje filmdragerad tablett innehåller 90 mg ticagrelor.
- Övriga ingredienser är:
Kärnan på surfplattan: mannitol (E421), kalciumvätefosfatdihydrat, natriumstärkelseglykolat, hydroxipropylcellulosa (E463), magnesiumstearat (E470b)
Tabletbeläggning: hypromellos (E464), titandioxid (E171), talk, polyetylenglykol 400 och gul järnoxid (E172).
Beskrivning av hur Brilique ser ut och förpackningens innehåll
Filmdragerad tablett (tablett): Tabletterna är runda, bikonvexa, gula, filmdragerade, präglade med "90" över ett "T" på ena sidan.
Brilique finns i:
- standardblister (med sol / mån -symboler) i kartonger med 60 och 180 tabletter
- kalenderblister (med sol / mån -symboler) i kartonger med 14, 56 och 168 tabletter
- endos perforerade blåsor i en kartong med 100x1 tabletter.
Alla förpackningsstorlekar kanske inte marknadsförs.
Bipacksedel: AIFA (Italian Medicines Agency). Innehåll publicerat i januari 2016. Den information som finns finns kanske inte uppdaterad.
För att få tillgång till den senaste versionen är det lämpligt att gå till AIFA (Italian Medicines Agency) webbplats. Ansvarsfriskrivning och användbar information.
01.0 LÄKEMEDLETS NAMN
BRILIQUE 90 MG TABLETTER TÄCKADE MED FILM
02.0 KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING
Varje filmdragerad tablett innehåller 90 mg ticagrelor.
För fullständig förteckning över hjälpämnen, se avsnitt 6.1.
03.0 LÄKEMEDELSFORM
Filmdragerad tablett (tablett).
Runda, bikonvexa, gula tabletter präglade med "90" över ett "T" på ena sidan och släta på andra sidan.
04.0 KLINISK INFORMATION
04.1 Terapeutiska indikationer
Brilique, administrerat samtidigt med acetylsalicylsyra (ASA), är indicerat för förebyggande av aterotrombotiska händelser hos vuxna patienter med akut koronarsyndrom (instabil angina, hjärtinfarkt utan ST-segmenthöjning [NSTEMI] eller ST-segmenthöjning hjärtinfarkt [STEMI] ), inklusive farmakologiskt behandlade patienter och de som genomgår perkutan koronar intervention (PCI) eller koronar bypass -transplantation (CABG).
För mer information, se avsnitt 5.1.
04.2 Dosering och administreringssätt
Dosering
Behandlingen med Brilique bör inledas med en enda 180 mg laddningsdos (två 90 mg tabletter) och sedan fortsätta med 90 mg två gånger dagligen.
Patienter som behandlas med Brilique ska också ta ASA dagligen, såvida det inte är specifikt kontraindicerat. Efter en startdos av ASA ska Brilique tas med en underhållsdos av ASA mellan 75 och 150 mg (se avsnitt 5.1).
Behandling rekommenderas i upp till 12 månader om inte behandlingen med Brilique är kliniskt indicerad (se avsnitt 5.1) Erfarenheten efter 12 månader är begränsad.
Hos patienter med akut koronarsyndrom (ACS) kan för tidigt avbrott av eventuell trombocythämmande behandling, inklusive behandling med Brilique, resultera i en ökad risk för kardiovaskulär död eller hjärtinfarkt på grund av patientens underliggande sjukdom. Därför bör behandling avbrytas i förtid.
Avbrott i behandlingens kontinuitet bör också undvikas. Patienten som missar en dos Brilique ska endast ta en 90 mg tablett (nästa dos) vid schemalagd tid.
Om det behövs kan patienter som behandlas med klopidogrel bytas direkt till Brilique (se avsnitt 5.1). Att byta från prasugrel till Brilique har inte studerats.
Särskilda populationer
Pensionärer
Ingen dosjustering krävs hos äldre patienter (se avsnitt 5.2).
Patienter med nedsatt njurfunktion
Ingen dosjustering krävs hos patienter med nedsatt njurfunktion (se avsnitt 5.2). Det finns ingen information om behandling av dialyspatienter och därför rekommenderas inte Briliquen till dessa patienter.
Patienter med nedsatt leverfunktion
Brilique har inte studerats hos patienter med måttligt eller allvarligt nedsatt leverfunktion. Därför är dess användning kontraindicerad hos patienter med måttligt till allvarligt nedsatt leverfunktion (se avsnitt 4.3, 4.4 och 5.2). Ingen dosjustering krävs hos patienter med lätt nedsatt leverfunktion.
Pediatrisk population
Säkerhet och effekt för Brilique hos barn under 18 år för de godkända indikationerna hos vuxna har inte fastställts. Inga data finns tillgängliga.
Administreringssätt
För oral användning.
Brilique kan ges till måltider eller mellan måltiderna.
För patienter som inte kan svälja tabletten (erna) hela kan Brilique -tabletter krossas till ett fint pulver, blandas i ett halvt glas vatten och drickas omedelbart. Glaset ska sköljas med ytterligare ett halvt glas. D "vatten och innehållet berusat. Blandningen kan också administreras genom ett nasogastriskt rör (CH8 eller större). Efter administrering av blandningen är det viktigt att skölja det nasogastriska röret med vatten.
04.3 Kontraindikationer
• Överkänslighet mot den aktiva substansen eller mot något hjälpämne som anges i avsnitt 6.1 (se avsnitt 4.8).
• Patologisk blödning pågår.
• Tidigare intrakraniell blödning (se avsnitt 4.8).
• Måttligt till svårt nedsatt leverfunktion (se avsnitt 4.2, 4.4 och 5.2).
• Samtidig administrering av ticagrelor med starka CYP3A4-hämmare (t.ex. ketokonazol, klaritromycin, nefazodon, ritonavir och atazanavir) är kontraindicerat, eftersom samtidig administrering kan leda till en väsentlig ökning av ticagrelorexponeringen (se avsnitt 4.5).
04.4 Särskilda varningar och lämpliga försiktighetsåtgärder vid användning
Risk för blödning
I den avgörande fas 3 -kliniska prövningen (PLATO [PLATelet Inhibition and Patient Outcomes], 18 624 patienter) inkluderade de viktigaste uteslutningskriterierna en ökad risk för blödning, kliniskt relevant trombocytopeni eller anemi, tidigare intrakraniell blödning, gastrointestinal blödning under de senaste 6 månaderna eller större operation under de senaste 30 dagarna. Patienter med akut koronarsyndrom som behandlats med Brilique och ASA visade en ökad risk för icke-CABG-relaterade större blödningar och mer allmänt för blödning som krävde medicinsk övervakning, dvs större + mindre blödningar enligt PLATO-kriterier, men inte dödliga blödningar eller liv som var liv hotande (se avsnitt 4.8).
Därför bör användningen av Brilique hos patienter med känd ökad risk för blödning balanseras mot nyttan när det gäller förebyggande av aterotrombotiska händelser.Om kliniskt indikerat bör Brilique användas med försiktighet i följande patientgrupper:
• Patienter med anlag för blödning (t.ex. på grund av trauma, nyligen opererad, blödningsstörningar, aktiv eller nyligen gastrointestinal blödning). Användning av Brilique är kontraindicerad hos patienter med aktiv patologisk blödning, hos personer som tidigare haft intrakraniell blödning och hos patienter med måttligt till allvarligt nedsatt leverfunktion (se avsnitt 4.3).
• Patienter med samtidig administrering av läkemedel som kan öka risken för blödning (t.ex. icke-steroida antiinflammatoriska läkemedel (NSAID), orala antikoagulantia och / eller fibrinolytika) inom 24 timmar efter dosen av Brilique.
Det finns inga data med ticagrelor om en hemostatisk fördel av trombocytransfusioner; den cirkulerande mängden ticagrelor kan hämma transfunderade blodplättar. Eftersom samtidig administrering av ticagrelor och desmopressin inte minskade standardblödningstiden är det osannolikt att desmopressin kommer att vara effektivt vid klinisk behandling av blödningar (se avsnitt 4.5).
Antifibrinolytisk behandling (aminokapronsyra eller tranexaminsyra) och / eller rekombinant faktor VIIa kan öka hemostasen Ticagrelor kan återupptas när orsaken till blödningen har identifierats och kontrollerats.
Kirurgiska ingrepp
Patienter bör uppmanas att informera läkare och tandläkare om att de tar Brilique innan de planerar en operation och innan de tar något nytt läkemedel.
Bland PLATO -patienterna som genomgick koronar bypass -transplantation (CABG) hade Brilique -armen mer blödning än klopidogrel när behandlingen avbröts inom 1 dag före operationen, men en liknande frekvens av större blödningar jämfört med klopidogrel när behandlingen stoppades 2 eller fler dagar före operationen (se avsnitt 4.8). Om en patient är på väg att genomgå elektiv kirurgi och en trombocythämmande effekt inte önskas, ska Brilique avbrytas 7 dagar före operationen (se avsnitt 5.1).
Patienter med risk för bradykardi
Efter observationer av mestadels asymptomatiska ventrikulära pauser i en tidigare klinisk studie, exkluderades patienter med ökad risk för bradykardi (t.ex. patienter utan pacemaker med sjukt sinus syndrom, 2: a eller 3: e grad AV-block eller bradykardirelaterat synkope) från den avgörande PLATO studie som utvärderar säkerheten och effekten av ticagrelor. Med tanke på den begränsade kliniska erfarenheten bör ticagrelor därför användas med försiktighet hos dessa patienter (se avsnitt 5.1).
Dessutom bör försiktighet iakttas vid administrering av ticagrelor samtidigt med läkemedel som är kända för att framkalla bradykardi. Inga kliniskt relevanta bevis på biverkningar observerades dock i PLATO -studien efter samtidig administrering med ett eller flera läkemedel som är kända för att inducera bradykardi (t.ex. 96% betablockerare, 33% kalciumkanalblockerare diltiazem och verapamil och 4% digoxin) ( se avsnitt 4.5).
Under delstudien med PLATO Holter -övervakning upplevde fler patienter ventrikulära pauser ≥3 sekunder med ticagrelor än med klopidogrel under den akuta fasen av ACS. Ökningen av ventrikulära pauser observerade på Holter med ticagrelor var större hos patienter med kronisk hjärtsvikt (CHF) än i den totala studiepopulationen under den akuta fasen av ACS, men inte efter en månad på ticagrelor eller i jämförelse med klopidogrel. Det fanns inga negativa kliniska konsekvenser förknippade med denna obalans (inklusive synkope eller pacemakerapplikation) i denna patientpopulation (se avsnitt 5.1).
Dyspné
Episoder av dyspné rapporterades av 13,8% av patienterna som behandlades med Brilique och av 7,8% av patienterna som behandlades med klopidogrel. Hos 2,2% av patienterna ansåg utredarna att dyspné hade orsakssamband med behandling med Brilique. Dyspné är vanligtvis mild till måttlig i intensitet och försvinner ofta utan att behandlingen behöver avbrytas.Patienter med astma / KOL kan ha en absolut ökad risk att utveckla dyspné med Brilique (se avsnitt 4.8) .Ticagrelor ska användas med försiktighet hos patienter med historia av astma och / eller KOL. Mekanismen har inte belysts. Om en patient utvecklar ny, långvarig eller förvärrad dyspné bör detta undersökas noggrant och om det inte tolereras bör behandlingen med Brilique avbrytas.
Höjning av kreatinin
Kreatininnivåerna kan öka under behandling med ticagrelor (se avsnitt 4.8). Mekanismen har inte klargjorts. Njurfunktionen bör övervakas efter en månad och därefter enligt standardiserad klinisk praxis, med särskild uppmärksamhet åt patienter ≥ 75 år, till patienter med måttligt / svårt nedsatt njurfunktion och till dem som får samtidig behandling med angiotensin II -antagonister.
Ökad urinsyra
I PLATO -studien hade patienter som tog ticagrelor en högre risk för hyperurikemi än de som fick klopidogrel (se avsnitt 4.8). Försiktighet bör iakttas när ticagrelor administreras till patienter som tidigare haft hyperurikemi eller giktartrit. Som en försiktighetsåtgärd rekommenderas inte användning av ticagrelor till patienter med urinsyra nefropati.
Övrig
Baserat på sambandet som observerades i PLATO-studien mellan underhållsdos av ASA och relativ effekt av ticagrelor jämfört med klopidogrel, rekommenderas inte samtidig administrering av ticagrelor och höga underhållsdoser av ASA (> 300 mg) (se avsnitt 5.1).
04.5 Interaktioner med andra läkemedel och andra former av interaktion
Ticagrelor är främst ett substrat för CYP3A4 och en mild hämmare av CYP3A4. Ticagrelor är också ett substrat för P-glykoprotein (P-gp) och en svag hämmare av P-gp och kan öka exponeringen för P-gp-substrat.
Andra läkemedels effekter på Brilique
Läkemedel som metaboliseras av CYP3A4
CYP3A4 -hämmare
• Starka CYP3A4-hämmare-Samtidig administrering av ketokonazol och ticagrelor ökade Cmax och AUC för ticagrelor med 2,4 respektive 7,3 gånger. Cmax och AUC för den aktiva metaboliten minskade med 89% respektive 56%. Andra starka CYP3A4 -hämmare (klaritromycin, nefazodon, ritonavir och atazanavir) kan ge liknande effekter och därför är samtidig användning av starka CYP3A4 -hämmare med Brilique kontraindicerad (se avsnitt 4.3).
• Måttliga CYP3A4-hämmare-Samtidig administrering av diltiazem och ticagrelor ökade Cmax för ticagrelor med 69% och AUC med 2,7 gånger och minskade Cmax för den aktiva metaboliten med 38%, medan AUC var oförändrat. Det finns ingen effekt av ticagrelor på plasmanivåerna av diltiazem. Andra måttliga CYP3A4 -hämmare (t.ex. amprenavir, aprepitant, erytromycin och flukonazol) kan ge en liknande effekt och kan administreras tillsammans med Brilique.
CYP3A -inducerare
Samtidig administrering av rifampicin och ticagrelor minskade Cmax och AUC för ticagrelor med 73%respektive 86%. Cmax för den aktiva metaboliten var oförändrad och AUC minskades med 46%respektive. Andra CYP3A-inducerare (t.ex. fenytoin, karbamazepin och fenobarbital) kan minska exponeringen av ticagrelor. Samtidig administrering av ticagrelor med potenta CYP3A-inducerare kan minska ticagrelor-exponering och effekt, därför rekommenderas inte samtidig användning med Brilique.
Ciklosporin (hämmare av P-gp och CYP3A)
Samtidig administrering av cyklosporin (600 mg) och ticagrelor ökade Cmax och AUC för ticagrelor med 2,3 respektive 2,8 gånger. AUC för den aktiva metaboliten ökade med 32% och Cmax minskade. 15% i närvaro av cyklosporin.
Det finns inga data om samtidig användning av ticagrelor och andra aktiva substanser som också är potenta hämmare av P-glykoprotein (P-gp) och måttliga hämmare av CYP3A4 (t.ex. verapamil, kinidin) som också kan orsaka ökad exponering för ticagrelor. Om denna förening inte kan undvikas, bör deras samtidig användning göras med försiktighet.
Andra
Kliniska läkemedelsinteraktionsstudier har visat att samtidig administrering av ticagrelor med heparin, enoxaparin och ASA eller desmopressin inte hade någon effekt på den farmakokinetiska profilen för ticagrelor eller den aktiva metaboliten eller på ADP-inducerad trombocytaggregation jämfört med enbart ticagrelor. Kliniskt indicerade läkemedel att alter hemostas bör användas med försiktighet i kombination med ticagrelor.
En tvåfaldig ökning av exponeringen för ticagrelor har observerats efter daglig konsumtion av stora mängder grapefruktjuice (3 x 200 ml) per dag. Denna omfattning av exponeringsökningen anses inte vara kliniskt relevant för de flesta patienter. .
Effekter av Brilique på andra läkemedel
Läkemedel som metaboliseras av CYP3A4
• Simvastatin -Samtidig administrering av ticagrelor och simvastatin ökade simvastatin Cmax med 81% och AUC med 56% och resulterade i en ökning av simvastatinsyra Cmax med 64% och AUC med 52%, med vissa individuella steg större än 2 till 3 gånger. Samtidig administrering av ticagrelor och simvastatindoser större än 40 mg dagligen kan orsaka biverkningar på grund av simvastatin och bör vägas mot de potentiella fördelarna. Det fanns ingen effekt av simvastatin på plasmanivåerna av ticagrelor. Ticagrelor kan orsaka liknande effekter på lovastatin Samtidig användning av ticagrelor och doser av simvastatin eller lovastatin över 40 mg rekommenderas inte.
• Atorvastatin -Samtidig administrering av atorvastatin och ticagrelor ökade Cmax för atorvastatinsyra med 23% och AUC med 36%. Liknande ökningar av AUC och Cmax observerades för alla metaboliter av atorvastatinsyra Dessa ökningar anses inte vara kliniskt signifikanta.
• En liknande effekt på andra statiner som metaboliseras av CYP3A4 kan inte uteslutas. PLATO -patienterna som fick ticagrelor tog olika statiner, utan problem med statinsäkerhet hos 93% av PLATO -kohorten av patienter som tog dessa läkemedel.
Ticagrelor är en mild hämmare av CYP3A4. Samtidig administrering av ticagrelor- och CYP3A4-substrat med låga terapeutiska index (dvs. cisaprid eller ergotalkaloider) rekommenderas inte, eftersom ticagrelor kan öka exponeringen för dessa läkemedel.
P-glykoproteinsubstrat (P-gp) (inklusive digoxin, cyklosporin)
Samtidig administrering av Brilique ökade Cmax för digoxin med 75% och "AUC med 28%. De genomsnittliga" nedströms "digoxinnivåerna ökade med cirka 30% vid samtidig administrering av ticagrelor, med två gånger maximala individuella ökningar i närvaro av digoxin , Cmax och AUC för ticagrelor och dess aktiva metabolit påverkades inte.
Därför rekommenderas lämplig klinisk och / eller laboratorieövervakning vid administrering av läkemedel med lågt terapeutiskt index beroende på P-gp, såsom digoxin, samtidigt med ticagrelor.
Det fanns ingen effekt av ticagrelor på blodnivåerna av cyklosporin.Ticagrelors effekt på andra P-gp-substrat har inte studerats.
Läkemedel som metaboliseras av CYP2C9
Samtidig administrering av ticagrelor och tolbutamid resulterade i ingen förändring av plasmanivåerna för något av läkemedlen, vilket tyder på att ticagrelor inte är en CYP2C9 -hämmare och inte kommer att påverka den CYP2C9 -medierade metabolism av läkemedel som warfarin och tolbutamid.
Orala preventivmedel
Samtidig administrering av ticagrelor och levonorgestrel och etinylestradiol ökade exponeringen för etinylestradiol med cirka 20%, men förändrade inte den farmakokinetiska profilen för levonorgestrel. En kliniskt relevant effekt på effekten av det orala preventivmedlet förväntas inte efter samtidig användning av levonorgestrel och etinylestradiol och ticagrelor.
Läkemedel som är kända för att framkalla bradykardi
Efter observation av mestadels asymptomatiska ventrikulära pauser och bradykardi bör försiktighet iakttas vid administrering av Brilique samtidigt med andra bradykardiinducerande läkemedel (se avsnitt 4.4) Men inga tecken på kliniskt biverkningar observerades i PLATO-studien. Signifikant efter samtidig administrering med ett eller flera läkemedel som är kända för att framkalla bradykardi (t.ex. 96% betablockerare, 33% kalciumkanalblockerare diltiazem och verapamil och 4% digoxin).
Andra samtidiga terapier
I PLATO -studien administrerades Brilique vanligen tillsammans med ASA, protonpumpshämmare, statiner, betablockerare, angiotensinomvandlande enzymhämmare och angiotensinreceptorantagonister, som krävs vid samtidiga kliniska tillstånd, under lång tid och även med heparin, lågmolekylära vikt heparin och kortsiktiga intravenösa GpIIb / IIIa-hämmare (se avsnitt 5.1) Inga tecken på kliniskt relevanta interaktioner observerades med dessa läkemedel.
Samtidig administrering av ticagrelor och heparin, enoxaparin eller desmopressin har ingen effekt på aktiverad partiell tromboplastintid (aPTT), aktiverad koaguleringstid (ACT) eller faktor Xa-doser. På grund av potentiella farmakodynamiska interaktioner bör försiktighet iakttas vid samtidig administrering av Brilique med läkemedel som är kända för att försämra hemostas.
Efter rapporter om onormala hudblödningar med SSRI (t.ex. paroxetin, sertralin och citalopram) bör försiktighet iakttas vid administrering av SSRI med ticagrelor eftersom detta kan leda till ökad blödningsrisk.
04.6 Graviditet och amning
Kvinnor i fertil ålder
Kvinnor i fertil ålder måste vidta lämpliga preventivmedel för att undvika eventuell graviditet medan de tar Brilique.
Graviditet
Det finns inga eller begränsade data om användning av ticagrelor hos gravida kvinnor.
Djurstudier har visat reproduktionstoxicitet (se avsnitt 5.3). Brilique rekommenderas inte under graviditeten.
Matdags
Farmakodynamiska / toxikologiska data från djur har visat att ticagrelor och dess aktiva metaboliter utsöndras i mjölk (se avsnitt 5.3). En risk för de nyfödda / spädbarnen kan inte uteslutas. Beslut måste fattas om amning eller amning ska avbrytas. Avbryta / avstå från Brilique -terapi med hänsyn till nyttan av amning för barnet och nyttan av terapi för mamman.
Fertilitet
Ticagrelor har ingen effekt på manlig eller kvinnlig fertilitet hos djur (se avsnitt 5.3).
04.7 Effekter på förmågan att framföra fordon och använda maskiner
Brilique har ingen eller försumbar påverkan på förmågan att framföra fordon eller använda maskiner. Yrsel har rapporterats under behandling av akut koronarsyndrom. Av denna anledning bör patienter som upplever yrsel vara försiktiga när de kör bil eller använder maskiner.
04.8 Biverkningar
Sammanfattning av säkerhetsprofilen
De vanligaste rapporterade biverkningarna hos patienter som behandlats med ticagrelor var dyspné, kontusion och epistaxis, som inträffade vid en högre förekomst än i klopidogrelgruppen.
Tabell över biverkningar
Säkerheten för Brilique hos patienter med akut koronarsyndrom (instabil angina, NSTEMI och STEMI) utvärderades i den stora fas 3 -studien PLATO ([PLATelet Hämning och patient ELLERutfall], 18 624 patienter), som jämförde patienter som behandlats med Brilique (180 mg laddningsdos Brilique och underhållsdos på 90 mg två gånger dagligen) och patienter som behandlats med klopidogrel (300-600 mg laddningsdos följt av 75 mg en gång dagligen som underhåll dos), båda ges i kombination med acetylsalicylsyra (ASA) och andra standardterapier.
Följande biverkningar har identifierats efter studier som utförts med Brilique eller har rapporterats efter marknadsföring (tabell 1).
Biverkningar klassificeras efter frekvens och organklass. Frekvensklasser definieras enligt följande konventioner: Mycket vanliga (≥1 / 10), Vanliga (≥1 / 100,
Flera korrelerade biverkningsterminologier har grupperats i tabell e
inkludera medicinska termer som beskrivs nedan:
till hyperurikemi, ökad serumurinsyra
b cerebral blödning, intrakraniell blödning, hemorragisk stroke
c dyspné, dyspné från ansträngning, dyspné i vila, nattlig dyspné
d gastrointestinal blödning, rektal blödning, tarmblödning, melaena, ockult blod
och gastrointestinal sårblödning, magsårblödning, duodenalsårblödning, magsårblödning
f subkutant hematom, kutan blödning, subkutan blödning, petechiae
g kontusion, hematom, blåmärken, ökad tendens till blåmärken, traumatiskt hematom
h hematuri, blod i urinen, urinvägsblödning
blödning på punkteringsstället, hematom på kärlpunktionsstället, blödning vid injektionsstället, blödning på punkteringsstället, blödning vid kateterplatsen
# Inga biverkningar av hemartros rapporterades i ticagrelor -armen (n = 9 235) i PLATO -studien; frekvensen beräknades med hjälp av den övre gränsen för 95% konfidensintervall för punktuppskattningen (baserat på 3 / X, där X representerar det totala urvalet, dvs 9 235 patienter). Detta beräknas som 3 /9 235, vilket motsvarar det "sällsynta "frekvensklass
## Dödliga intrakraniella blödningar har rapporterats efter marknadsföring
Beskrivning av utvalda biverkningar
Blödning
De övergripande resultaten av PLATO -studiens blödningshastigheter visas i tabell 2.
Tabell 2 - Kaplan -Meier bedömning av blödningshastigheter som en funktion av behandlingen
Definitioner av blödningskategorier:
Dödlig / livshotande större blödning: Kliniskt uppenbar med minskat hemoglobin> 50 g / l eller transfusion ≥ 4 enheter röda blodkroppar; eller dödlig; eller intrakraniell; o intraperikardial med hjärttamponad; eller med hypovolemisk chock eller svår hypotoni som kräver hypertensiv behandling eller kirurgi.
Andra större blödningar: Kliniskt uppenbar med hemoglobinminskning på 30-50 g / l eller transfusion av 2-3 enheter röda blodkroppar; elleravsevärt inaktiverande.
Mindre blödning: Kräver medicinsk intervention för att stoppa eller behandla blödningen.
TIMI större blödning: Kliniskt uppenbart med minskat hemoglobin> 50 g / l eller intrakraniell blödning.
TIMI Mindre blödning: Kliniskt uppenbar med 30-50 g / l minskning av hemoglobin.
Brilique och klopidogrel skilde sig inte från frekvensen av större dödlig / livshotande blödning enligt PLATO-kriterier, större total blödning enligt PLATO-kriterier, större blödningar enligt TIMI-skala eller mindre enligt TIMI-skala (tabell 2). Men fler PLATO kombinerade större + mindre blödningar inträffade med ticagrelor än med klopidogrel. Få patienter i PLATO -studien fick dödlig blödning: 20 (0,2%) för ticagrelor och 23 (0,3%) för klopidogrel (se avsnitt 4.4).
Faktorer som ålder, kön, vikt, ras, geografisk region, samtidig fysiskt tillstånd, samtidig behandling och sjukdomshistoria, inklusive tidigare stroke eller övergående ischemisk attack, var inte förutsägande för vare sig total eller icke-procedurrelaterad större blödning, definierad enligt PLATO -kriterier. Följaktligen identifierades ingen särskild grupp med risk för en specifik blödningskategori.
CABG-relaterad blödning: I PLATO-studien hade 42% av 1 584 patienter (12% av kohorten) som genomgick koronar bypass-transplantation (CABG) kirurgi dödlig / livshotande större blödning enligt PLATO-kriterierna, utan skillnad mellan behandlingsgrupper. CABG-relaterad dödlig blödning inträffade hos 6 patienter i varje behandlingsgrupp (se avsnitt 4.4).
Blödning inte relaterad till CABG och blödning inte relaterad till någon procedur: Brilique och klopidogrel skiljer sig inte åt i icke-CABG-relaterad större dödlig / livshotande blödning, definierad enligt PLATO-kriterier, medan Total major blödning enligt PLATO-kriterier, större enligt TIMI-skala och större + mindre enligt TIMI-skala, var vanligare med ticagrelor. På samma sätt, när man eliminerade procedurrelaterade blödningar, observerades fler blödningar med ticagrelor än med klopidogrel (tabell 2). Avbrytande av behandlingen på grund av icke-procedurell blödning var vanligare för ticagrelor (2,9%) än för klopidogrel (1,2%; p
Intrakraniell blödning: Fler icke-procedurella intrakraniella blödningar inträffade med ticagrelor (n = 27 blödningar hos 26 patienter, 0,3%) än med klopidogrel (n = 14 blödningar, 0,2%), inklusive 11 blödningar med ticagrelor och 1 med klopidogrel hade ett dödligt resultat. Det fanns inga skillnader i total dödlig blödning.
Dyspné
Dyspné, en känsla av andfåddhet, har rapporterats hos patienter som behandlats med Brilique. Dyspniska biverkningar (dyspné, dyspné i vila, dyspné vid ansträngning, paroxysmal nattlig dyspné och nattlig dyspné) rapporterades, när de var associerade, av 13,8% av patienterna som behandlades med ticagrelor och av 7,8% av patienterna som behandlades med klopidogrel. Hos 2,2% av patienterna som tog ticagrelor och 0,6% av patienterna som behandlades med klopidogrel ansåg utredare att dyspné var orsakssammanhängande behandling i PLATO -studien och några få fall var allvarliga (0,14% för ticagrelor; 0,02% för klopidogrel), (se avsnitt 4.4). De vanligaste rapporterade symtomen på dyspné var milda till måttliga i intensitet, och de flesta rapporterades som en enda episod strax efter behandlingens början.
Jämfört med klopidogrel kan astma / KOL-patienter som behandlas med ticagrelor ha en ökad risk att utveckla icke-svår dyspné (3,29% för ticagrelor mot 0,53% för klopidogrel) och svår dyspné (0,38% för ticagrelor mot 0,00% för klopidogrel). I absoluta tal var denna risk större än den totala PLATO -studiepopulationen. Ticagrelor ska administreras med försiktighet till patienter med tidigare astma och / eller KOL (se avsnitt 4.4).
Ungefär 30% av alla episoder av dyspné försvann inom 7 dagar. PLATO -studien omfattade patienter som hade kongestivt hjärtsvikt, kronisk obstruktiv lungsjukdom eller astma vid baslinjen; dessa patienter och äldre rapporterade mer sannolikt episoder av dyspné. I Brilique -gruppen avbröt 0,9% av patienterna den aktiva substansen som studerades på grund av dyspné jämfört med 0,1% av patienterna som fick klopidogrel. Den högre förekomsten av dyspné som observerats med Brilique är inte associerad med början eller förvärring av hjärt- eller lungsjukdom (se avsnitt 4.4). Brilique påverkar inte lungfunktionstester.
Diagnostiska tester
Kreatininhöjningar: I PLATO-studien ökade serumkreatininkoncentrationen signifikant med mer än 30% hos 25,5% av patienterna som tog ticagrelor jämfört med 21,3% av patienterna som tog klopidogrel och mer än 50% hos patienter som tog ticagrelor. 8,3% av ticagrelor- behandlade patienter kontra 6,7% av klopidogrelbehandlade patienter Ökningar av kreatinin> 50% var mer uttalade hos patienter över 75 år (ticagrelor 13,6% kontra klopidogrel 8, 8%), hos patienter med allvarligt nedsatt njurfunktion vid baslinjen (ticagrelor 17,8 % kontra klopidogrel 12,5%) och hos patienter som samtidigt behandlas med angiontensin II -receptorantagonister (ticagrelor 11,2% kontra klopidogrel 7, 1%). Inom dessa undergrupper var svåra njurbiverkningar och biverkningar som ledde till att läkemedelsavbrott var likartade i de två behandlingsgrupperna. Totalt rapporterade njurbiverkningar var 4,9% för ticagrelor mot 3,8% för klopidogrel, men en liknande andel av patienterna rapporterade händelser som av utredare ansågs ha orsakssamband med behandlingen: 54 (0,6%) för ticagrelor och 43 (0,5%) för klopidogrel.
Urinsyrahöjningar: I PLATO -studien ökade koncentrationerna av urinsyra i serum över normalgränsen hos 22% av patienterna som behandlades med ticagrelor jämfört med 13% av patienterna som tog klopidogrel. Den genomsnittliga koncentrationen av serumurinsyra ökade med cirka 15% med ticagrelor jämfört med 7,5% med klopidogrel och minskade till cirka 7% med ticagrelor efter avslutad behandling, medan ingen minskning observerades med klopidogrel. Hyperurikemi-biverkningen rapporterades hos 0,5% för ticagrelor kontra 0,2% för klopidogrel. Av dessa biverkningar ansågs 0,05% för ticagrelor kontra 0,02% för klopidogrel ha samband med utredarstyrd kausalitet. För giktartrit rapporterades biverkningar 0,2% för ticagrelor kontra 0,1% för klopidogrel; ingen av dessa biverkningar ansågs ha orsakssamband med behandling av utredarna.
Rapportering av misstänkta biverkningar
Rapportering av misstänkta biverkningar som uppstår efter godkännande av läkemedlet är viktigt eftersom det möjliggör kontinuerlig övervakning av nytta / riskbalansen för läkemedlet.Hälso- och sjukvårdspersonal uppmanas att rapportera alla misstänkta biverkningar via det nationella rapporteringssystemet. "Adress" www .agenziafarmaco.gov.it/it/responsabili ".
04.9 Överdosering
Ticagrelor tolereras väl i enstaka doser upp till 900 mg. Gastrointestinal toxicitet var dosbegränsande i en eskaleringsstudie med en enda dos. Andra kliniskt relevanta biverkningar som kan uppstå efter överdosering inkluderar dyspné och ventrikelpauser (se avsnitt 4.8).
Vid överdosering kan ovanstående potentiella biverkningar inträffa och EKG -övervakning bör övervägas.
Hittills finns det ingen känd motgift för att motverka effekterna av ticagrelor, och det antas att ticagrelor inte är dialyserbart (se avsnitt 4.4). Behandling av överdos bör följa standarderna för lokal medicinsk praxis. Den förväntade effekten av för mycket Brilique är förlängningen av blödningsrisken i samband med trombocythämning.Om blödning uppstår bör lämpliga stödjande åtgärder vidtas.
05.0 FARMAKOLOGISKA EGENSKAPER
05.1 Farmakodynamiska egenskaper
Farmakoterapeutisk grupp: trombocythämmande medel, exklusive heparin.
ATC -kod: B01AC24.
Handlingsmekanism
Brilique innehåller ticagrelor, som tillhör den kemiska klassen cyklopentyltriazolopyrimidiner
(CPTP), som är en oral, direkt, selektiv och reversibel P2Y12 -receptorantagonist och förhindrar adenosindifosfat (ADP) -medierad P2Y12 -beroende trombocytaktivering och aggregering.
Ticagrelor förhindrar inte ADP-bindning, men när den binder till P2Y12-receptorn förhindrar den ADP-inducerad signaltransduktion. Eftersom trombocyter spelar en roll vid uppkomsten och / eller utvecklingen av trombotiska komplikationer av aterosklerotisk sjukdom, har hämning av trombocytfunktionen visat sig minska risken för kardiovaskulära händelser som död, hjärtinfarkt eller stroke.
Ticagrelor ökar också lokala endogena nivåer av adenosin genom hämning av den jämviktiga nukleosidtransportören -1 (ENT -1).
Ticagrelor har visat sig öka följande adenosininducerade effekter hos friska försökspersoner och hos patienter med ACS: vasodilatation (mätt som ökat koronar blodflöde hos friska frivilliga och hos ACS-patienter; huvudvärk), hämning av trombocytfunktionen (i helblod) in vitro) och dyspné. Kopplingen mellan den observerade ökningen av adenosin och kliniska resultat (t.ex. sjuklighet-dödlighet) har emellertid inte belysts.
Farmakodynamiska effekter
Åtgärdens början (Onset)
Hos patienter med stabil kranskärlssjukdom som behandlas med ASA inducerar ticagrelor en snabb inverkan av läkemedelseffekt, vilket demonstreras genom medelvärde "trombocytaggregation (PAH) -hämning" för ticagrelor, 0,5 timmar efter en 180 mg laddningsdos på cirka 41% med ett maximalt effekt på PAH på 89% inom 2-4 timmar efter dos och upprätthålls mellan 2 och 8 timmar. 90% av patienterna hade en slutlig PAH> 70% inom 2 timmar efter dos.
Åtgärdens reversibilitet (förskjutning)
Om ett CABG -ingrepp planerades ökar risken för blödning med ticagrelor jämfört med klopidogrel när det stoppas mindre än 96 timmar före operationen.
Data om förändring av terapi
Byte från klopidogrel till ticagrelor resulterar i en absolut ökning av PAH på 26,4%, medan byte från ticagrelor till klopidogrel resulterar i en absolut minskning av PAH med 24,5%. Patienter kan bytas från klopidogrel till ticagrelor -terapi utan att avbryta trombocythämmande effekten (se avsnitt 4.2).
Klinisk effekt och säkerhet
PLATO-studien omfattade 18 624 patienter som presenterade inom 24 timmar efter uppkomsten av symtom på instabil angina (UA), icke-ST-segmenthöjt myokardinfarkt (NSTEMI) eller ST-segmenthöjningshjärtinfarkt (STEMI), och som hade behandlats inledningsvis farmakologiskt med antingen perkutan koronar intervention (PCI) eller koronar bypass -transplantation (CABG) (se avsnitt 4.1).
Vid samma dagliga dos av ASA var ticagrelor 90 mg två gånger dagligen överlägsen klopidogrel 75 mg / dag för att förebygga den sammansatta slutpunkten för kardiovaskulär död [CV], hjärtinfarkt [MI] eller stroke, med skillnaden styrd av minskningen av CV- och MI -dödsfall Patienterna fick antingen en laddningsdos på 300 mg klopidogrel (600 mg dos möjlig för PCI) eller 180 mg ticagrelor.
Resultatet uppnåddes tidigt (absolut riskreduktion [ARR] 0,6% och relativ riskreduktion [RRR] med 12% efter 30 dagar), med en behandlingseffekt som förblev konstant under 12 månader och fick en "ARR" på 1,9% per år och en RRR på 16%. Dessa data tyder på att det är lämpligt att behandla patienter med ticagrelor i upp till 12 månader (se avsnitt 4.2) Behandling av 54 ACS -patienter med ticagrelor istället för att med klopidogrel skulle det undvika att en aterotrombotisk händelse uppstår ; behandling av 91 patienter skulle undvika 1 CV -död (tabell 3).
Effekten av ticagrelorbehandling jämfört med klopidogrel är konsekvent i alla undergrupper av patienter efter egenskaper, inklusive vikt, kön, diabetes mellitus, övergående ischemisk attack eller icke-hemorragisk stroke, revaskularisering, samtidig behandling inklusive hepariner, GpIIb / IIIa-hämmare och protonpump hämmare (se avsnitt 4.5), slutlig diagnos av händelsen (STEMI, NSTEMI eller UA) och behandlingsväg tilldelad randomisering (invasiv eller medicinsk).
En svagt signifikant interaktion observerades mellan behandling och geografisk region, där Hazard Ratio (HR) för den primära slutpunkten gynnar ticagrelor i resten av världen, medan den gynnar klopidogrel i Nordamerika, som står för cirka 10%av den globala. populationsstudie (p-värde av interaktionen = 0,045).
Undersökande analyser tyder på en möjlig koppling till ASA -dos, eftersom minskad effekt observerades med ticagrelor i samband med ökande doser av ASA Den dagliga kroniska dosen av ASA, givet tillsammans med Brilique, bör vara mellan 75 och 150 mg (se avsnitt 4.2 och 4.4) .
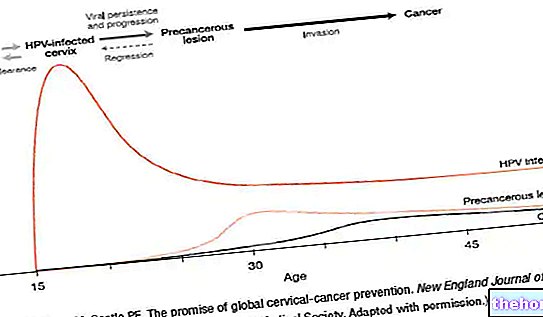
Figur 1 visar den uppskattade risken för första händelse av en händelse som bedöms i den sammansatta effekt -slutpunkten.
Brilique reducerade början av den primära sammansatta slutpunkten jämfört med klopidogrel i både UA / NSTEMI- och STEMI -populationerna (tabell 3).
Tabell 3 - Kliniska resultat i PLATO -studien
a ARR = absolut riskminskning; RRR = relativ riskreduktion = (1-riskförhållande) x 100%. En negativ RRR indikerar en ökad relativ risk.
b exklusive tyst hjärtinfarkt.
c SRI = svår återkommande ischemi; RI = återkommande ischemi; TIA = övergående ischemisk attack; ATE = aterotrombotisk händelse. Totalt MI inkluderar tyst MI, med händelsedatum som diagnosdatum.
d värde av nominell betydelse; alla andra värden är formellt statistiskt signifikanta baserat på ett fördefinierat hierarkiskt test.
Holter delstudie
För att studera uppkomsten av ventrikulära pauser och andra arytmiska episoder under PLATO -studien utförde utredarna Holter -övervakning i en undergrupp på nästan 3000 patienter, varav cirka 2 000 hade uppgifter om både den akuta fasen av koronarsyndrom. Akut, antingen efter en månad. Den primära variabeln av intresse var början av ventrikulära pauser ≥3 sekunder. Fler patienter fick ventrikulära pauser med ticagrelor (6,0%) än med klopidogrel (3,5%) i den akuta fasen; och 2,2% respektive 1,6% efter 1 månad (se avsnitt 4.4). Ökningen av ventrikulära pauser i den akuta fasen av ACS var mer uttalad hos tikagrelorbehandlade patienter med CHF-historia (9,2% mot 5,4% hos patienter utan CHF-historia; för klopidogrelbehandlade patienter, 4,0% hos patienter med en historia av CHF jämfört med 3,6% hos dem utan en historia av CHF) .Denna skillnad observerades inte efter en månad: 2,0% mot 2,1% för tikagrelorbehandlade patienter med respektive utan CHF respektive 3,8% mot 1,4% med klopidogrel Inga negativa kliniska konsekvenser förknippade med denna skillnad (inklusive pacemakerapplikationer) hittades i denna patientpopulation.
Genetisk delstudie av PLATO -studien
Genotypningen av CYP2C19 och ABCB1 av 10 285 patienter från PLATO -studien gjorde det möjligt att associera de kliniska resultaten av studien med den genotypiska spridningen. Ticagrelors överlägsenhet gentemot klopidogrel för att minska stora kardiovaskulära händelser påverkades inte av patientens CYP2C19- eller ABCB1 -genotyp.Liknande som de totala uppgifterna från PLATO -studien skilde incidensen av totala större blödningar av PLATO -kriterier inte mellan ticagrelor och klopidogrel, oavsett av CYP2C19- eller ABCB1 -genotypen. Förekomsten av PLATO Non-CABG-relaterade större blödningar ökade med ticagrelor jämfört med klopidogrel hos patienter med en eller flera CYP2C19-funktionsalleler, men liknande klopidogrel hos patienter utan reducerade funktionsalleler.
Kompositförening av effekt och säkerhet
Den sammansatta kombinationen av effekt och säkerhet (CV -död, hjärtinfarkt, stroke eller PLATO Total större blödning) indikerar att effektfördelarna med Brilique jämfört med klopidogrel inte uppvägs av större blödningar (ARR 1, 4%; RRR 8%; HR 0,92 ; p = 0,0257) under 12 månader efter SCA.
Pediatrisk population
Europeiska läkemedelsmyndigheten har avstått från skyldigheten att lämna resultaten av studier med Brilique i alla undergrupper av den pediatriska populationen i den godkända indikationen (se avsnitt 4.2 och 5.2).
05.2 Farmakokinetiska egenskaper
Ticagrelor uppvisar linjär farmakokinetik och exponering för ticagrelor och den aktiva metaboliten (AR-C124910XX) är ungefär dosproportionella upp till 1260 mg.
Absorption
Absorptionen av ticagrelor är snabb, med ett medelvärde på cirka 1,5 timmar. Bildandet av den stora cirkulerande metaboliten, AR-C124910XX (även aktiv), härledd från ticagrelor, är snabb, med en t
median på cirka 2,5 timmar. Efter oral administrering av 90 mg ticagrelor under fastande förhållanden är Cmax 529 ng / ml och AUC är 3 451 ng xh / ml.Prekursormetabolitförhållandet är 0,28 för Cmax och 0,42 för AUC.
Den genomsnittliga absoluta biotillgängligheten för ticagrelor uppskattades till 36%. Förtäring av en fettrik måltid orsakade 21% ökning av AIC för ticagrelor och 22% minskning av Cmax för den aktiva metaboliten, men hade ingen effekt på Cmax för ticagrelor eller AUC för ticagrelor. Aktiv metabolit. Dessa små förändringar anses vara av minimal klinisk relevans, därför kan ticagrelor administreras både med och utan måltider. Ticagrelor och dess aktiva metabolit är substrat för P-gp.
Ticagrelor som krossade tabletter blandade i vatten, administrerade oralt eller genom ett nasogastriskt rör i magen, har en jämförbar biotillgänglighet för hela tabletter för AUC och Cmax för både ticagrelor och den aktiva metaboliten. Initial exponering (0, 5 och 1 timme efter dos) för krossade ticagrelor -tabletter blandade i vatten var högre än för hela tabletter, med en koncentrationsprofil i allmänhet identisk därefter (2 till 48 timmar).
Distribution
Distributionsvolymen för steady-state för ticagrelor är 87,5 L. Ticagrelor och dess aktiva metabolit är i stor utsträckning bundna till plasmaproteiner (> 99,0%).
Biotransformation
CYP3A4 är det huvudsakliga enzymet som ansvarar för metabolismen av ticagrelor och bildandet av den aktiva metaboliten, och deras interaktioner med andra CYP3A -substrat sträcker sig från aktivering till hämning.
Ticagrelors huvudmetabolit är AR-C124910XX, som också har farmakologisk aktivitet, vilket visats in vitro genom bindning till trombocyt P2Y12-receptorn i ADP Systemisk exponering för den aktiva metaboliten är cirka 30-40% av den som observerats med ticagrelor.
Eliminering
Den primära elimineringsvägen för ticagrelor är via hepatisk metabolism. När radiomärkt ticagrelor administreras är den genomsnittliga återhämtningen av radioaktivitet cirka 84% (57,8% i avföring, 26,5% i urinen). De återvunna mängderna av både ticagrelor och den aktiva metaboliten, som finns i urinen, var mindre än 1% av dos.
Den primära elimineringsvägen för den aktiva metaboliten är sannolikt gallsekretion. Den genomsnittliga t1 / 2 var cirka 7 timmar för ticagrelor och 8,5 timmar för den aktiva metaboliten.
Särskilda populationer
Pensionärer
Högre exponering för ticagrelor (cirka 25% för både Cmax och AUC) och den aktiva metaboliten observerades hos äldre patienter (≥75 år) med ACS jämfört med yngre patienter, via en "populationsfarmakokinetisk analys. Anses vara kliniskt signifikant (se avsnitt 4.2 ).
Pediatrisk population
Ticagrelor har inte utvärderats i den pediatriska populationen (se avsnitt 4.2 och 5.1).
Sex
Högre exponeringar av ticagrelor och den aktiva metaboliten observerades hos kvinnor än hos män. Dessa skillnader anses inte vara kliniskt signifikanta.
Nedsatt njurfunktion
Exponeringen för ticagrelor var cirka 20% lägre och exponeringen för aktiv metabolit var cirka 17% högre hos patienter med svårt nedsatt njurfunktion (kreatininclearance).
Nedsatt leverfunktion
Cmax och AUC för ticagrelor var 12% och 23% högre hos patienter med lätt nedsatt leverfunktion jämfört med ett jämförbart urval av friska försökspersoner (se avsnitt 4.2). Ticagrelor har inte studerats hos patienter med måttligt eller svårt nedsatt leverfunktion, och dess användning hos dessa patienter är kontraindicerad (se avsnitt 4.3 och 4.4).
Etnicitet
Patienter av asiatisk härkomst visar en genomsnittlig biotillgänglighet som är 39% högre än kaukasiska patienter. Patienter som själv identifierades som svarta hade en 18% lägre biotillgänglighet för ticagrelor än kaukasiska patienter. I kliniska farmakologiska studier var exponeringen (Cmax och AUC) för ticagrelor hos japanska patienter cirka 40% (20% efter justering för kroppsvikt) högre än hos kaukasiska patienter.
05.3 Prekliniska säkerhetsdata
Prekliniska data om ticagrelor och dess huvudmetabolit visade inte en oacceptabel risk för negativa effekter för människor baserat på konventionella studier av säkerhetsfarmakologi, toxicitet vid enstaka eller upprepade doser och genotoxisk potential.
Gastrointestinal irritation observerades hos flera djurarter för kliniskt relevanta exponeringsnivåer (se avsnitt 4.8).
Hos honråttor visade ticagrelor vid höga doser en ökad förekomst av livmodertumörer (adenokarcinom) och en ökad förekomst av leveradenom. Mekanismen för uppkomsten av livmodertumörer är förmodligen relaterad till en hormonell obalans som kan leda till tumörbildning hos råttor. Mekanismen bakom bildandet av hepatiska adenom beror troligen på en gnagarspecifik hepatisk enzyminduktion. Därför anses observationerna avseende den cancerframkallande potentialen vara av osannolik relevans för människor.
Mindre utvecklingsavvikelser observerades hos råttor vid en maternellt toxisk dos (säkerhetsmarginal 5.1). Hos kaniner observerades en liten fördröjning av levermognad och skelettutveckling hos foster från mödrar som utsatts för höga doser, utan tecken på maternell toxicitet (säkerhetsmarginal 4.5).
Studier på råttor och kaniner har visat reproduktionstoxicitet, med en liten minskning av moderns kroppsviktökning, minskad livskraft hos nyfödda och minskad födelsevikt, med tillväxthämning. Ticagrelor orsakade oregelbundna cykler (främst längre cykler) hos honråttor, men påverkade inte totalt sett fertilitet hos han- och honråttor Farmakokinetiska studier utförda med radiomärkt ticagrelor visade att moderföreningen och dess metaboliter utsöndras i mjölk från råttor (se avsnitt 4.6).
06.0 LÄKEMEDELSINFORMATION
06.1 Hjälpämnen
Kärnan på surfplattan
Mannitol (E421)
Kalciumvätefosfatdihydrat
Magnesiumstearat (E470b)
Natriumstärkelseglykolat
Hydroxipropylcellulosa (E463)
Tabletbeläggning
Talk
Titandioxid (E171)
Gul järnoxid (E172)
Polyetylenglykol 400
Hypromellos (E464)
06.2 Oförenlighet
Inte relevant.
06.3 Giltighetstid
3 år.
06.4 Särskilda förvaringsanvisningar
Detta läkemedel kräver inga särskilda förvaringsförhållanden.
06.5 Förpackningens innehåll och förpackningens innehåll
• Genomskinlig blister (med sol / månesymboler) i PVC-PVDC / Al på 10 tabletter; kartonger med 60 tabletter (6 blister) och 180 tabletter (18 blister).
• Genomskinlig kalenderblister (med sol / månesymboler) i PVC-PVDC / Al med 14 tabletter; kartonger med 14 tabletter (1 blister), 56 tabletter (4 blister) och 168 tabletter (12 blister).
• Transparent endos perforerad blister i PVC-PVDC / Al om 10 tabletter; kartonger med 100 x 1 tabletter (10 blister).
Alla förpackningsstorlekar kanske inte marknadsförs.
06.6 Anvisningar för användning och hantering
Inga speciella instruktioner.
07.0 INNEHAVARE AV GODKÄNNANDE FÖR FÖRSÄLJNING
AstraZeneca AB
SE-151 85
Södertälje
Sverige
08.0 NUMMER FÖR FÖRSÄLJNINGSTILLSTÅND
EU / 1/10/655 / 001-006
040546018
040546020
040546032
040546044
040546057
040546069
09.0 DATUM FÖR FÖRSTA GODKÄNNANDE ELLER FÖRNYELSE AV GODKÄNNANDET
Datum för det första godkännandet: 3 december 2010
Datum för senaste förnyelse: 17 juli 2015
10.0 DATUM FÖR ÖVERSYN AV TEXTEN
Juli 2015