Aktiva ingredienser: Calcipotriol
CALCIPOTRIOL SANDOZ 0,05 mg / g salva
Varför används Calcipotriol - generiskt läkemedel? Vad är det för?
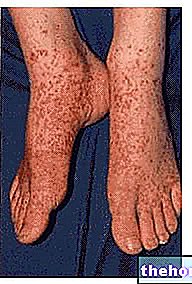
Calcipotriol Sandoz används på huden för lokal behandling av mild till måttligt svår form av psoriasis (psoriasis vulgaris).
Psoriasis är ett tillstånd som uppstår när hudceller produceras för snabbt, vilket orsakar skalning och rodnad. Denna salva hjälper till att återställa hastigheten med vilken hudceller produceras till normala värden.
Kontraindikationer När Calcipotriol inte ska användas - Generiskt läkemedel
Använd inte Calcipotriol Sandoz:
- Om du är allergisk (överkänslig) mot den aktiva substansen kalcipotriol eller mot något av innehållsämnena (se avsnitt 6 för en fullständig lista över hjälpämnen).
- Om du har en störning av kalciummetabolismen eller om kalciumnivån i din kropp är för hög. Denna salva kan öka kalciumnivåerna i blodet.
Försiktighetsåtgärder för användning Vad du behöver veta innan du tar Calcipotriol - Generiskt läkemedel
- Användning av denna salva för barn och ungdomar (under 18 år) rekommenderas inte, eftersom klinisk erfarenhet inte är tillräcklig för att motivera dess användning hos dessa patienter.
- Denna salva kan orsaka hudirritation. Tvätta händerna efter applicering av salvan. Ta också bort alla produkter som kan ha spridit sig till friska delar av huden.
- Applicera det inte på ansiktet.
- Om du använder mycket kalcipotriol Sandoz under en längre tid eller mer än 100 g på en vecka kan du uppleva en ökning av kalciumhalten i blodet. Detta kan till exempel orsaka trötthet, illamående, aptitlöshet och förstoppning (se även avsnitt 3).
- Applicera det inte samtidigt med topiskt applicerad salicylsyra
- Täck inte över det behandlade området med ett vattentätt bandage
- Om du använder det i samband med UV -terapi kan det uppstå mörka områden på huden (hyperpigmentering), som dock försvinner när behandlingen är klar.
Interaktioner Vilka läkemedel eller livsmedel kan ändra effekten av Calcipotriol - Generic drug
Om du använder Calcipotriol Sandoz samtidigt med andra former av psoriasisbehandling (fototerapi, aktuella kortikosteroider, cyklosporin eller acitretin) kommer din läkare att råda dig när du ska använda salvan.
Applicera inte en kräm eller salva som innehåller salicylsyra på de delar av huden där salvan har applicerats, eftersom den bryter ner den aktiva ingrediensen i denna salva.
Tala om för din läkare eller apotekspersonal om du tar eller nyligen har tagit andra läkemedel, även receptfria sådana.
Varningar Det är viktigt att veta att:
Graviditet och amning
På grund av bristen på tillgänglig information, undvik att använda den under graviditeten. Det är inte känt om kalcipotriol utsöndras i bröstmjölk, därför bör dess användning också undvikas under amning. Om du är gravid eller ammar, eller om du blir gravid när du använder denna salva, informera din läkare.
Fråga din läkare eller apotekspersonal om råd innan du tar något läkemedel.
Köra och använda maskiner
Ingen effekt på förmågan att framföra fordon och använda maskiner förväntas.
Viktig information om några av innehållsämnena i Calcipotriol Sandoz
Denna salva innehåller propylenglykol, ett ämne som kan orsaka hudirritation.
Dos, metod och administreringstid Hur man använder Calcipotriol - Generiskt läkemedel: Dosering
Vuxna
Dosering:
Applicera alltid denna salva enligt läkarens instruktioner exakt. Om du är osäker bör du rådfråga din läkare eller apotekspersonal.
Applicera inte mer än 100 g av denna salva per vecka. Om du applicerar det samtidigt med en kräm eller lösning som innehåller kalcipotriol, bör den totala mängden kalcipotriol per vecka inte överstiga 5 mg
Metod och administreringssätt:
Calcipotriol Sandoz är avsett för användning på huden (kutan användning).
Tvätta händerna innan du använder denna salva. Ta sedan bort skruvlocket och kontrollera att tätningen är intakt innan du använder salvan för första gången. Vid ett 30g eller 120g rör måste du bryta tätningen med spetsen på lockets baksida. "Salva på ett finger eller på en del av huden som påverkas av psoriasis. Applicera salvan genom att sprida ett tunt lager av den på de drabbade områdena i huden.Gnugga den lätt tills hela området är täckt. Applicera inte denna salva på ditt ansikte (se även avsnitt 4).
Efter applicering av denna salva, tvätta händerna noggrant, såvida du inte behandlar en form av psoriasis som påverkar dina händer. Försök att inte överföra salvan från de behandlade områdena till andra delar av kroppen, särskilt ansiktet.
Om du använder en fuktkräm, applicera den först och vänta tills den är helt absorberad innan du applicerar denna salva.
Administreringsfrekvens:
Som monoterapi:
För bästa resultat, applicera denna salva två gånger om dagen, en gång på morgonen och en gång på kvällen. Beroende på ditt svar på behandlingen kan din läkare förskriva endast en applikation per dag.
Som kombinationsterapi:
Om du använder Calcipotriol Sandoz samtidigt med andra former av psoriasisbehandling, kommer din läkare att råda dig när och hur ofta du ska använda denna salva.
Behandlingstid:
En första förbättring kan uppstå efter cirka två veckors behandling. De första symptomen som försvinner är vanligtvis flagnande eller flagnande. Detta kommer att göra psoriasisplåsterna tunnare vid beröring. Försvinnandet av hudrödhet tar längre tid. I allmänhet uppnås maximal effekt efter 4-8 veckor.
Barn under 18 år
Calcipotriol Sandoz rekommenderas inte för barn och ungdomar (under 18 år), eftersom det finns begränsad erfarenhet av denna salva hos dessa patienter.
Om du har glömt att använda Calcipotriol Sandoz
Om du glömmer att använda denna salva vid föreskriven tid, gör det så snart du kommer ihåg, fortsätt sedan behandlingen enligt föreskrivet.
Använd inte mer än vanlig salva för att kompensera för en glömd dos.
Om du vill avbryta behandlingen med Calcipotriol Sandoz
Kontakta din läkare först om du tänker avbryta behandlingen.
Fråga din läkare eller apotekspersonal om du har ytterligare frågor om användningen av detta läkemedel
Överdosering Vad du ska göra om du har tagit en överdos av Calcipotriol - Generic Drug
Informera din läkare om du har applicerat mer salva än den föreskrivna dosen (mer än 100 g per vecka). Överdriven dosering kan leda till att kalciumhalten i blodet stiger, vilket i sin tur kan orsaka symtom som illamående, aptitlöshet, förstoppning, kräkningar, muskelsvaghet, energiförlust, trötthet och medvetslöshet.
Biverkningar Vilka är biverkningarna av Calcipotriol - Generic drug
Liksom alla läkemedel kan Calcipotriol Sandoz orsaka biverkningar men alla användare behöver inte få dem.
Biverkningar förekommer hos cirka 15% av patienterna. De vanligaste biverkningarna är övergående hudreaktioner av olika slag.
Vanliga biverkningar (drabbar fler än 1 av 100 men färre än 1 av 10 patienter) är: klåda, hudirritation, sveda och sveda, torr hud, rodnad och utslag.
Mindre vanliga biverkningar (dvs. drabbar fler än en av 1000 men färre än en av 100 patienter) är: kontaktdermatit, eksem och förvärrade former av psoriasis.
Mycket sällsynta biverkningar (drabbar färre än 1 av 10 000 patienter) är: hög kalciumhalt i blod och urin, allergiska reaktioner inklusive nässelutslag, svullnad i ansiktet, ögonlock, händer, fötter eller hals, övergående förändringar i hudfärg, övergående ökning i hudens känslighet för ljus.
Appliceras av misstag i ansiktet, kan salvan orsaka rodnad eller hudirritation i ansiktet eller runt munnen.
Om någon av biverkningarna blir allvarlig eller varar länge, eller om du märker några biverkningar som inte nämns i denna bipacksedel, kontakta din läkare eller apotekspersonal.
Giltighetstid och lagring
Förvara detta läkemedel utom syn- och räckhåll för barn.
Använd det inte efter utgångsdatumet som anges på tuben och kartongen. Utgångsdatumet avser den sista dagen i månaden.
Efter 3 månader från den första öppningen av röret får innehållet inte längre användas.
Förvaras vid högst 25 ° C. Förvara inte i kyl eller frys. Förvara produkten i originalförpackningen.
Läkemedel ska inte kastas i avloppsvatten eller hushållsavfall. Fråga din apotekare hur du ska kasta läkemedel som du inte använder längre. Detta hjälper till att skydda miljön.
Annan information
Vad Calcipotriol Sandoz innehåller
Den aktiva ingrediensen är kalcipotriol. Ett gram salva innehåller 0,05 mg kalcipotriol (en mängd motsvarande 50 mikrogram).
Ingredienserna är: makrogolstearyleter, dinatriumedetat, dinatriumfosfatdihydrat, alfa-tokoferylacetat, propylenglykol (E 490), lätt flytande paraffin, renat vatten och vitt mjukt paraffin.
Hur Calcipotriol Sandoz ser ut och förpackningens innehåll
Dess salva är vit till pärlgrå i färgen. Salvan finns i rör på 30 och 120 gram.
Alla förpackningsstorlekar kanske inte marknadsförs.
Bipacksedel: AIFA (Italian Medicines Agency). Innehåll publicerat i januari 2016. Den information som finns finns kanske inte uppdaterad.
För att få tillgång till den senaste versionen är det lämpligt att gå till AIFA (Italian Medicines Agency) webbplats. Ansvarsfriskrivning och användbar information.
01.0 LÄKEMEDLETS NAMN
CALCIPOTRIOLO SANDOZ
02.0 KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING
Ett gram salva innehåller 0,05 mg (motsvarande 50 mcg) kalcipotriol.
Hjälpämne: propylenglykol 10 mg / g.
För fullständig förteckning över hjälpämnen, se avsnitt 6.1.
03.0 LÄKEMEDELSFORM
Vit till pärlgrå salva.
04.0 KLINISK INFORMATION
04.1 Terapeutiska indikationer
Calcipotriol Sandoz är indicerat för lokal behandling av psoriasis (psoriasis vulgaris) i milda till måttligt svåra former.
04.2 Dosering och administreringssätt
Vuxna
Som monoterapi
Calcipotriol Sandoz ska appliceras på den drabbade delen av huden en eller två gånger om dagen. I början av behandlingen rekommenderas att applicera salvan två gånger om dagen. För underhållsterapi kan frekvensen av applikationer reduceras till en gång om dagen, beroende på svaret.
Den maximala mängden applicerad salva bör inte överstiga 100 g per vecka. Om Calcipotriol Sandoz används tillsammans med en annan kräm eller lösning som innehåller kalcipotriol, bör den totala veckodosen av kalcipotriol inte överstiga 5 mg.
Som kombinationsterapi
Terapier baserade på två dagliga applikationer av Calcipotriol Sandoz i kombination med fototerapi, acitretin och cyklosporin, och de som är baserade på en enda daglig applicering av Calcipotriol Sandoz tillsammans med aktuella kortikosteroider (bestående av exempelvis applicering av Calcipotriol Sandoz) är effektiva och tolereras väl. på morgonen och steroid på kvällen).
Behandlingslängden beror på den kliniska aspekten.I allmänhet uppstår en särskilt relevant terapeutisk effekt efter max 4-8 veckor.Terapin kan upprepas.
Nedsatt njur- och / eller leverfunktion
Patienter med känd allvarligt nedsatt njur- och / eller leverfunktion ska inte behandlas med kalcipotriol.
Barn och ungdomar (under 18 år)
Det finns begränsad erfarenhet av användning av Calcipotriol Sandoz till barn och ungdomar (under 18 år). Hos barn och ungdomar är den långsiktiga effekten och säkerheten för den dosering som anges ovan (i punkt Vuxna) har inte bevisats. Därför rekommenderas inte användning i denna population.
04.3 Kontraindikationer
• Överkänslighet mot den aktiva substansen (kalcipotriol) eller mot något hjälpämne.
• Kända störningar i kalciummetabolismen.
• Hyperkalcemi.
04.4 Särskilda varningar och lämpliga försiktighetsåtgärder vid användning
Calcipotriol Sandoz ska inte användas i ansiktet.
Patienter bör instrueras att tvätta händerna efter applicering för att undvika oavsiktlig överföring av salvan till andra områden, särskilt ansiktet.
Den långsiktiga effekten och säkerheten för denna salva hos barn har inte bevisats.
Vid vanliga doser (upp till 100 g per vecka) förekommer inte hyperkalcemi. Överdriven användning (50-100 g salva per dag) kan orsaka ökningar av kalciumhalten i serum, en trend som snabbt vänds i slutet av behandlingen. En serie studier som utförts på vuxna under ett år har inte gett några bevis för förekomsten av risken för hyperkalcemi, men för långvariga behandlingar med applikationer på stora hudområden är det nödvändigt att övervaka kalciumhalten i serum.
Med tanke på de möjliga effekterna på kalciummetabolismen bör patienter rådas att inte överskrida den föreskrivna dosen (se avsnitt 4.2), och att tillsatsen av penetrerande ämnen (t.ex. salicylsyra) till salvan inte är av samma anledning, ocklusion bör också undvikas.
Beroende på intensitet och varaktighet kan de kliniska symtomen på hyperkalcemi - till exempel hyperkalcemiskt syndrom eller kalciumförgiftning (se avsnitt 4.9) - likna symptom på en överdos av kolekalciferol.
En ihållande form av hyperkalcemi kan orsaka ektopisk kalciumavlagring på blodkärlens väggar, ledkapslar, magslemhinna, hornhinna och njurparenkym.
Enligt vissa data kan kombinationen av kalcipotriol med UV -ljus ge upphov till mörka områden med hyperpigmentering, en effekt som dock är reversibel. Om kalcipotriol startas under UV-B-behandling kan en form av ljuskänsligt eksem utvecklas.
Med tanke på den begränsade erfarenheten ska patienter med känd allvarligt nedsatt njur- och / eller leverfunktion inte behandlas med Calcipotriol Sandoz.
Calcipotriol Sandoz innehåller propylenglykol. Det kan orsaka hudirritation.
04.5 Interaktioner med andra läkemedel och andra former av interaktion
Även om hittills genomförda studier har visat att samtidig användning av Calcipotriol Sandoz med UVA -behandling eller med cyklosporin eller acitretin är effektivt och tolereras väl, finns det inte tillräckligt med data för att visa att kombinationen är mer effektiv eller att dosen av andra läkemedel kan minskas .
Salvan ökar inte den totala effektiviteten av UV-B-behandlingen. När den används tillsammans med en UV-B-behandling på vuxna patienter minskar den mängden bestrålning som krävs, vilket möjliggör ett kliniskt svar på lägre mängder UV-B. Calcipotriol Sandoz ska appliceras minst två timmar före UV-B-behandling. Kombinationen av kalcipotriol med UV-B-ljus kan resultera i mörka områden med hyperpigmentering samt ljuskänsligt eksem (se avsnitt 4.4). Salvan ska inte användas om patienten redan får en erytemogen eller suberytemogen dos av UV-B. Samtidig administrering av kalcipotriol och andra salicylsyra-läkemedel kan leda till inaktivering av kalcipotriol. Det finns ingen erfarenhet av samtidig behandling av kalcipotriol och andra antipsoriatiska produkter som appliceras samtidigt i samma hudområde.
04.6 Graviditet och amning
Graviditet
För kalcipotriol finns inga data tillgängliga för gravida patienter. Efter lokal applicering av Calcipotriol Sandoz på begränsade hudområden kan begränsad absorption förväntas.Om salvan används enligt instruktionerna förväntas ingen form av störning av kalciumhomeostas. När det gäller reproduktionstoxicitet indikerar djurstudier inga direkta eller indirekta skadliga effekter. Som en försiktighetsåtgärd är det att föredra att undvika användning av kalcipotriol under graviditeten.
Matdags
Det är inte känt om kalcipotriol utsöndras i bröstmjölk eller inte. Utsöndring av kalcipotriol i mjölk har inte studerats hos djur. Som en försiktighetsåtgärd är det att föredra att undvika användning av kalcipotriol under amning.
04.7 Effekter på förmågan att framföra fordon och använda maskiner
På grund av produktens art och indikationer för dess användning påverkar det inte förmågan att framföra fordon och använda maskiner.
04.8 Biverkningar
Mot bakgrund av tillgängliga kliniska data uppstår biverkningar hos cirka 15% av patienterna.
De vanligast observerade biverkningarna består av övergående hudreaktioner av olika slag, som uppträder särskilt på applikationsstället och som sällan kräver behandlingavbrott.
Biverkningar listas nedan efter systemorganklass (SOC) enligt MedDra -terminologi; enskilda biverkningar indikeras från och med de som oftast rapporteras.
Hud och subkutan vävnad
Vanliga (> 1/100 e: klåda, hudbrännande känsla, stickande känsla, hudirritation, torr hud, erytem, utslag *
Mindre vanliga (> 1/1000 och: eksem, kontaktdermatit, förvärrad psoriasis.
* Olika former av hudutslag har observerats, till exempel skivepitel, erytematös, makulopapulär och pustulär typ.
Metabolism och näringsstörningar
Mycket sällsynta (: hyperkalcemi, hyperkalciuri.
Följande biverkningar orsakade av kalcipotriol i form av hårbottenkräm, salva och lösning har observerats efter marknadsföring: övergående förändringar i hudpigmentering, övergående ljuskänslighet och överkänslighetsreaktioner, inklusive urtikaria, angioödem, periorbital eller ansiktsödem (mycket sällan I sällsynta fall kan perioral dermatit inträffa. Baserat på data efter marknadsföring anses den totala rapporterade biverkningsfrekvensen på cirka 1: 10 000 behandlingscykler vara mycket sällsynt.
04.9 Överdosering
Hittills vid normal dosering (upp till 100 g salva per vecka) har ingen form av hyperkalcemi observerats hos patienter med psoriasis vulgaris, även om möjligheten att hyperkalcemi uppträder vid denna dosering inte kan uteslutas helt. Överdriven användning (50-100 g per dag) kan orsaka en ökning av kalciumnivån, som snabbt minskar när behandlingen avslutas; vid lägre doser har fall av hyperkalcemi observerats hos patienter med generaliserad pustulär eller erytrodermal exfoliativ psoriasis. Symtom på hyperkalcemi inkluderar anorexi, illamående, kräkningar, förstoppning, hypotoni, depression, slöhet och koma.
05.0 FARMAKOLOGISKA EGENSKAPER
05.1 Farmakodynamiska egenskaper
Farmakoterapeutisk grupp: andra antipsoriatiska läkemedel för lokal användning, ATC -kod D05AX02
Calcipotriol är ett derivat av vitamin D. -studier in vitro visa att kalcipotriol inducerar differentiering och stoppar spridningen av keratinocyter. Kalcipotriols effekt på psoriasis beror främst på dessa två egenskaper.
De första effekterna, först och främst på desquamation, sedan på infiltration och slutligen på erytem, är synliga efter en behandlingsperiod som sträcker sig från två till fyra veckor. Den maximala effekten uppnås vanligtvis efter sex veckor.
05.2 Farmakokinetiska egenskaper
Data från en enda studie på fem psoriasispatienter behandlade med 0,3-1,7 g av en 50 mcg / g tritiummärkt kalcipotriol salva tyder på att mindre än 1% av den angivna dosen absorberades.
Den totala återhämtningen av det märkta tritium under en period av 96 timmar varierar emellertid från 6,7 till 32,6%, siffror maximerade med fel kemiluminescens. Det fanns inga tecken på vävnadsfördelning eller lungutsöndring.
05.3 Prekliniska säkerhetsdata
Det finns inga andra prekliniska data som anses relevanta för klinisk säkerhet än de som ingår i andra avsnitt i produktresumén.
06.0 LÄKEMEDELSINFORMATION
06.1 Hjälpämnen
• Makrogolstearyleter.
• Dinatriumedetat.
• Dinatriumfosfatdihydrat.
• Alfa-tokoferylacetat.
• Propylenglykol (E 490).
• Lätt flytande paraffin.
• Renat vatten.
• Vit mjuk paraffin.
06.2 Oförenlighet
Inte relevant.
06.3 Giltighetstid
2 år.
Efter första öppnandet: 3 månader.
06.4 Särskilda förvaringsanvisningar
Förvaras vid högst 25 ° C.
Förvara inte i kyl eller frys.
Förvaras i originalförpackningen.
06.5 Förpackningens innehåll och förpackningens innehåll
Aluminiumrör stängt av ett membran med ett skruvlock av polyeten.
Förpackningsstorlekar: 30, 120 gram.
Alla förpackningsstorlekar kanske inte marknadsförs.
06.6 Anvisningar för användning och hantering
Inga speciella instruktioner.
07.0 INNEHAVARE AV GODKÄNNANDE FÖR FÖRSÄLJNING
Sandoz S.p.A. - Largo U. Boccioni, 1 - 21040 Origgio (VA)
08.0 NUMMER FÖR FÖRSÄLJNINGSTILLSTÅND
0,05 mg / g salva, 1 tub med 30 g - A.I.C. n. 037726015 / M
0,05 mg / g salva, 1 rör på 120 g - A.I.C. n. 037726027 / M
09.0 DATUM FÖR FÖRSTA GODKÄNNANDE ELLER FÖRNYELSE AV GODKÄNNANDET
Augusti 2007
10.0 DATUM FÖR REVISION AV TEXTEN
Februari 2008